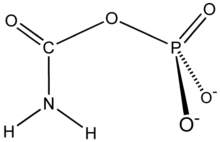
La carbamoil fosfato sintetasa cataliza la síntesis dependiente de ATP de carbamoil fosfato a partir de glutamina ( EC 6.3.5.5) o amoníaco ( EC 6.3.4.16) y bicarbonato. [1] Esta enzima que capta ATP cataliza la reacción de ATP y bicarbonato para producir carboxifosfato y ADP . El carboxifosfato reacciona con amoníaco para dar ácido carbámico . A su vez, el ácido carbámico reacciona con un segundo ATP para dar carbamoil fosfato más ADP .
Representa el primer paso comprometido en la biosíntesis de pirimidina y arginina en procariotas y eucariotas, y en el ciclo de la urea en la mayoría de los vertebrados terrestres . [2] La mayoría de los procariotas tienen una forma de CPSasa que participa en la biosíntesis de arginina y pirimidina, sin embargo ciertas bacterias pueden tener formas separadas.
Hay tres formas diferentes que cumplen funciones muy diferentes:
La carbamoil fosfato sintetasa tiene tres pasos principales en su mecanismo y es, en esencia, irreversible. [4]
Se sabe que la actividad de la enzima se inhibe tanto con tampones Tris como HEPES . [5]
La carbamoil fosfato sintasa (CPSasa) es una enzima heterodímera compuesta por una subunidad pequeña y una grande (con excepción de la CPSasa III, que está compuesta por un único polipéptido que puede haber surgido de la fusión génica de los dominios glutaminasa y sintetasa ). [2] [3] [6] La CPSasa tiene tres sitios activos , uno en la subunidad pequeña y dos en la subunidad grande. La subunidad pequeña contiene el sitio de unión de la glutamina y cataliza la hidrólisis de la glutamina a glutamato y amoníaco , que a su vez es utilizado por la cadena grande para sintetizar carbamoil fosfato. La subunidad pequeña tiene una estructura beta/beta/alfa de 3 capas y se cree que es móvil en la mayoría de las proteínas que la llevan. El dominio C-terminal de la subunidad pequeña de la CPSasa tiene actividad de glutamina amidotransferasa. La subunidad grande tiene dos dominios carboxifosfato homólogos , ambos con sitios de unión de ATP ; Sin embargo, el dominio carboxifosfato N-terminal cataliza la fosforilación del biocarbonato, mientras que el dominio C-terminal cataliza la fosforilación del intermedio carbamato . [7] El dominio carboxifosfato que se encuentra duplicado en la subunidad grande de la CPSasa también está presente como una sola copia en las enzimas dependientes de biotina acetil-CoA carboxilasa (ACC), propionil-CoA carboxilasa (PCCase), piruvato carboxilasa (PC) y urea carboxilasa .
La subunidad grande de la CPSasa bacteriana tiene cuatro dominios estructurales : el dominio de carboxifosfato 1, el dominio de oligomerización, el dominio de carbamoilfosfato 2 y el dominio alostérico. [8] Los heterodímeros de la CPSasa de Escherichia coli contienen dos túneles moleculares: un túnel de amoníaco y un túnel de carbamato. Estos túneles entre dominios conectan los tres sitios activos distintos y funcionan como conductos para el transporte de intermediarios de reacción inestables (amoníaco y carbamato) entre sitios activos sucesivos . [9] El mecanismo catalítico de la CPSasa implica la difusión del carbamato a través del interior de la enzima desde el sitio de síntesis dentro del dominio N-terminal de la subunidad grande hasta el sitio de fosforilación dentro del dominio C-terminal.