La transposición de Fries , llamada así por el químico alemán Karl Theophil Fries , es una reacción de transposición de un éster fenólico a una hidroxiarilcetona por catálisis de ácidos de Lewis . [1] [2] [ 3] [4]
Implica la migración de un grupo acilo del éster fenólico al anillo arílico . La reacción es selectiva en sentido orto y para y uno de los dos productos puede verse favorecido si se modifican las condiciones de reacción, como la temperatura y el disolvente .
A pesar de los muchos esfuerzos, no se ha determinado un mecanismo de reacción definitivo para la transposición de Fries. Se han obtenido pruebas de mecanismos intermoleculares e intramoleculares mediante experimentos cruzados con reactivos mixtos. [ cita requerida ] El progreso de la reacción no depende del disolvente o del sustrato . Un mecanismo ampliamente aceptado implica un carbocatión intermedio.

En el primer paso de reacción se utiliza un ácido de Lewis , por ejemplo cloruro de aluminio AlCl
3coordina con el átomo de oxígeno del carbonilo del grupo acilo . Este átomo de oxígeno es más rico en electrones que el átomo de oxígeno fenólico y es la base de Lewis preferida . Esta interacción polariza el enlace entre el residuo de acilo y el átomo de oxígeno fenólico y el grupo cloruro de aluminio se reorganiza en el átomo de oxígeno fenólico. Esto genera un carbocatión de acilo libre que reacciona en una sustitución aromática electrofílica clásica con el anillo aromático. El protón extraído se libera como ácido clorhídrico donde el cloro se deriva del cloruro de aluminio. La orientación de la reacción de sustitución depende de la temperatura. Una temperatura de reacción baja favorece la sustitución para y con temperaturas altas prevalece el producto orto , esto se puede racionalizar como una exhibición de control de reacción termodinámico clásico versus cinético ya que el producto orto puede formar un complejo bidentado más estable con el aluminio. [5] La formación del producto orto también se favorece en disolventes no polares; a medida que aumenta la polaridad del disolvente, también aumenta la proporción del producto para. [6]
Los fenoles reaccionan para formar ésteres en lugar de hidroxiarilcetonas cuando reaccionan con haluros de acilo en condiciones de acilación de Friedel-Crafts . Por lo tanto, esta reacción es de importancia industrial para la síntesis de hidroxiarilcetonas, que son intermediarios importantes para varios productos farmacéuticos. Como alternativa al cloruro de aluminio , también se pueden utilizar otros ácidos de Lewis como el trifluoruro de boro y el triflato de bismuto o ácidos próticos fuertes como el fluoruro de hidrógeno y el ácido metanosulfónico . [ cita requerida ] Para evitar por completo el uso de estos catalizadores corrosivos y nocivos para el medio ambiente, se realiza activamente la investigación de catalizadores heterogéneos alternativos .
En todos los casos, solo se pueden utilizar ésteres con componentes acilo estables que puedan soportar las duras condiciones de la transposición de Fries. Si el componente aromático o acilo está muy sustituido, el rendimiento químico disminuirá debido a las restricciones estéricas . La desactivación de los grupos directores meta en el grupo benceno también tendrá un efecto adverso, como se puede esperar de una acilación de Friedel-Crafts .
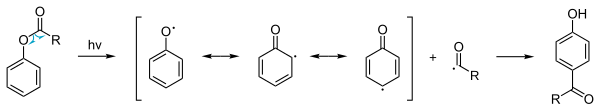
Además de la reacción térmica habitual de éster de fenilo, es posible una variante fotoquímica . La fototransformación de Fries también puede dar productos [1,3] y [1,5], [7] [8] que implica un mecanismo de reacción radical . Esta reacción también es posible con sustituyentes desactivantes en el grupo aromático. Debido a que los rendimientos son bajos, este procedimiento no se utiliza en la producción comercial. Sin embargo, la fototransformación de Fries puede ocurrir de forma natural, por ejemplo, cuando un objeto de plástico hecho de policarbonato aromático , poliéster o poliuretano se expone al sol (los carbonilos alifáticos experimentan reacciones de Norrish , que son algo similares). En este caso, la fotólisis de los grupos éster conduciría a la lixiviación de ftalato del plástico. [9]
En la transposición aniónica de Fries, la ortometalación de ésteres arílicos, carbamatos y carbonatos con una base fuerte da como resultado una transposición para dar especies ortocarbonílicas. [10]
