El reformado con vapor o reformado de metano con vapor (SMR) es un método para producir gas de síntesis ( hidrógeno y monóxido de carbono ) mediante la reacción de hidrocarburos con agua. Normalmente, el gas natural es la materia prima. El objetivo principal de esta tecnología es la producción de hidrógeno . La reacción está representada por este equilibrio: [1]
La reacción es fuertemente endotérmica (Δ H SR = 206 kJ/mol).
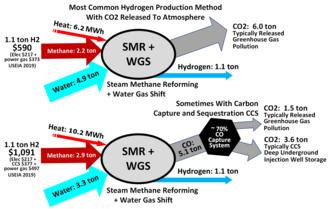
El hidrógeno producido mediante reformado con vapor se denomina hidrógeno "gris" cuando el dióxido de carbono residual se libera a la atmósfera e hidrógeno "azul" cuando el dióxido de carbono se captura y almacena (en su mayor parte) geológicamente (véase captura y almacenamiento de carbono) . El hidrógeno "verde" sin emisiones de carbono se produce mediante la división termoquímica del agua , utilizando energía solar térmica, electricidad con bajas emisiones de carbono o sin emisiones de carbono o calor residual, [2] o electrólisis , utilizando electricidad con bajas emisiones de carbono o sin emisiones de carbono. El hidrógeno "turquesa" con cero emisiones de carbono se produce mediante la pirólisis de metano de un solo paso del gas natural. [3]
El reformado con vapor del gas natural produce la mayor parte del hidrógeno del mundo. El hidrógeno se utiliza en la síntesis industrial de amoníaco y otros productos químicos. [4]
La cinética de la reacción de reformado con vapor, en particular utilizando catalizadores de níquel - alúmina , se ha estudiado en detalle desde la década de 1950. [5] [6] [7]
_Process_Flow.jpg/440px-Steam_Reforming_(SMR)_Process_Flow.jpg)
El propósito del prereformado es descomponer los hidrocarburos superiores como el propano , el butano o la nafta en metano (CH4 ) , lo que permite un reformado más eficiente aguas abajo.
La reacción que le da nombre es la reacción de reformado con vapor (SR) y se expresa mediante la ecuación:
A través de la reacción de desplazamiento de agua-gas (WGSR), se libera hidrógeno adicional por la reacción del agua con el monóxido de carbono generado según la ecuación [1]:
Se han estudiado algunas reacciones adicionales que ocurren dentro de los procesos de reformado con vapor. [6] [7] Comúnmente, también se incluye la reacción de reformado con vapor directo (DSR):
Como estas reacciones son altamente endotérmicas por sí mismas (a excepción de la WGSR, que es levemente exotérmica), se necesita agregar una gran cantidad de calor al reactor para mantener una temperatura constante. Las condiciones óptimas de operación del reactor SMR se encuentran dentro de un rango de temperatura de 800 °C a 900 °C a presiones medias de 20-30 bar. [8] Se requiere un alto exceso de vapor, expresado por la relación (molar) vapor-carbono (S/C). Los valores típicos de la relación S/C se encuentran dentro del rango de 2,5:1 - 3:1. [8]
La reacción se lleva a cabo en reactores de lecho empacado multitubular , un subtipo de la categoría de reactores de flujo pistón . Estos reactores consisten en una serie de tubos largos y estrechos [10] que están situados dentro de la cámara de combustión de un gran horno industrial , proporcionando la energía necesaria para mantener el reactor a una temperatura constante durante el funcionamiento. Los diseños de los hornos varían, dependiendo de la configuración del quemador, normalmente se clasifican en: de combustión superior, de combustión inferior y de combustión lateral. Un diseño notable es el reformador de pared de terraza Foster-Wheeler .
Dentro de los tubos, una mezcla de vapor y metano se pone en contacto con un catalizador de níquel . [10] Los catalizadores con una alta relación superficie-volumen son los preferidos debido a las limitaciones de difusión debido a la alta temperatura de funcionamiento . Ejemplos de formas de catalizador utilizadas son ruedas de radios, ruedas dentadas y anillos con agujeros ( ver: anillos Raschig ). Además, estas formas tienen una baja caída de presión , lo que es ventajoso para esta aplicación. [11]
El reformado con vapor de gas natural tiene una eficiencia del 65 al 75 %. [12]
Estados Unidos produce entre 9 y 10 millones de toneladas de hidrógeno al año, principalmente mediante reformado con vapor de gas natural. [13] La producción mundial de amoníaco, utilizando hidrógeno derivado del reformado con vapor, fue de 144 millones de toneladas en 2018. [14] El consumo de energía se ha reducido de 100 GJ/tonelada de amoníaco en 1920 a 27 GJ en 2019. [15]
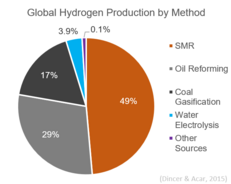
A nivel mundial, casi el 50% del hidrógeno se produce mediante reformado con vapor. [9] Actualmente es el método menos costoso para la producción de hidrógeno disponible en términos de su costo de capital. [16]
En un esfuerzo por descarbonizar la producción de hidrógeno, se están implementando métodos de captura y almacenamiento de carbono (CCS) dentro de la industria, que tienen el potencial de eliminar hasta el 90% del CO2 producido en el proceso. [16] A pesar de esto, la implementación de esta tecnología sigue siendo problemática, costosa y aumenta significativamente el precio del hidrógeno producido. [16] [17]
El reformado autotérmico (ATR) utiliza oxígeno y dióxido de carbono o vapor en una reacción con metano para formar gas de síntesis . La reacción tiene lugar en una sola cámara donde el metano se oxida parcialmente. La reacción es exotérmica. Cuando el ATR utiliza dióxido de carbono, la relación H2:CO producida es 1:1; cuando el ATR utiliza vapor, la relación H2 : CO producida es 2,5:1. La temperatura de salida del gas de síntesis está entre 950 y 1100 °C y la presión de salida puede ser de hasta 100 bar . [18]
Además de las reacciones [1] – [3], ATR introduce la siguiente reacción: [19]
La principal diferencia entre la SMR y la ATR es que la SMR solo utiliza aire para la combustión como fuente de calor para crear vapor, mientras que la ATR utiliza oxígeno purificado. La ventaja de la ATR es que se puede variar la relación H2 : CO, lo que puede resultar útil para producir productos especiales. Debido a la naturaleza exotérmica de algunas de las reacciones adicionales que ocurren dentro de la ATR, el proceso se puede realizar esencialmente a una entalpía neta de cero (Δ H = 0). [20]
La oxidación parcial (POX) ocurre cuando una mezcla de aire y combustible subestequiométrica se quema parcialmente en un reformador, creando un gas de síntesis rico en hidrógeno. La POX es típicamente mucho más rápida que el reformado con vapor y requiere un reactor más pequeño. La POX produce menos hidrógeno por unidad de combustible de entrada que el reformado con vapor del mismo combustible. [21]
El costo de capital de las plantas de reformado con vapor se considera prohibitivo para aplicaciones de tamaño pequeño a mediano. Los costos de estas instalaciones complejas no se reducen fácilmente. Las plantas de reformado con vapor convencionales operan a presiones de entre 200 y 600 psi (14–40 bar) con temperaturas de salida en el rango de 815 a 925 °C.
El gas quemado y los compuestos orgánicos volátiles (COV) ventilados son problemas conocidos en la industria offshore y en la industria del petróleo y el gas en tierra, ya que ambos liberan gases de efecto invernadero a la atmósfera. [22] El reformado para motores de combustión utiliza tecnología de reformado con vapor para convertir los gases residuales en una fuente de energía. [23]
El reformado para motores de combustión se basa en el reformado con vapor, donde los hidrocarburos no metánicos ( NMHC ) de gases de baja calidad se convierten en gas de síntesis (H 2 + CO) y finalmente en metano (CH 4 ), dióxido de carbono (CO 2 ) e hidrógeno (H 2 ), mejorando así la calidad del gas combustible (número de metano). [24]
También existe interés en el desarrollo de unidades mucho más pequeñas basadas en tecnología similar para producir hidrógeno como materia prima para celdas de combustible . [25] Las unidades de reformado con vapor a pequeña escala para abastecer celdas de combustible son actualmente objeto de investigación y desarrollo, que generalmente implican el reformado de metanol , pero también se están considerando otros combustibles como el propano , la gasolina , el autogás , el combustible diésel y el etanol . [26] [27]
El reformador, el sistema de celdas de combustible, aún se encuentra en investigación, pero en el corto plazo, los sistemas seguirían funcionando con los combustibles existentes, como el gas natural, la gasolina o el diésel. Sin embargo, existe un debate activo sobre si el uso de estos combustibles para producir hidrógeno es beneficioso mientras que el calentamiento global es un problema. El reformado de combustibles fósiles no elimina la liberación de dióxido de carbono a la atmósfera, pero reduce las emisiones de dióxido de carbono y casi elimina las emisiones de monóxido de carbono en comparación con la quema de combustibles convencionales debido al aumento de la eficiencia y las características de las celdas de combustible. [28] Sin embargo, al convertir la liberación de dióxido de carbono en una fuente puntual en lugar de una liberación distribuida, la captura y el almacenamiento de carbono se convierten en una posibilidad, lo que evitaría la liberación de dióxido de carbono a la atmósfera, al tiempo que aumentaría el costo del proceso.
El costo de producir hidrógeno reformando combustibles fósiles depende de la escala en que se realiza, del costo de capital del reformador y de la eficiencia de la unidad, de modo que, si bien puede costar solo unos pocos dólares por kilogramo de hidrógeno a escala industrial, podría ser más caro en la escala más pequeña necesaria para las celdas de combustible. [29] [ ¿ Fuente autopublicada? ]
Hay varios desafíos asociados con esta tecnología:
{{cite book}}: CS1 maint: location missing publisher (link){{cite journal}}: Requiere citar revista |journal=( ayuda )