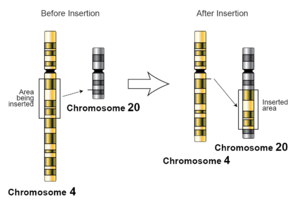
En genética , una inserción (también llamada mutación por inserción ) es la adición de uno o más pares de bases de nucleótidos en una secuencia de ADN . Esto a menudo puede ocurrir en regiones microsatélites debido al deslizamiento de la ADN polimerasa . Las inserciones pueden ser de cualquier tamaño, desde un par de bases insertado incorrectamente en una secuencia de ADN hasta una sección de un cromosoma insertada en otro. Se cree que el mecanismo de las mutaciones de inserción de una sola base más pequeñas es a través de la separación de pares de bases entre las cadenas de plantilla y cebador seguida de un apilamiento de bases no vecinas, que puede ocurrir localmente dentro del sitio activo de la ADN polimerasa. [1] A nivel cromosómico , una inserción se refiere a la inserción de una secuencia más grande en un cromosoma. Esto puede suceder debido a un entrecruzamiento desigual durante la meiosis .
La adición de la región N es la adición de nucleótidos no codificados durante la recombinación por la desoxinucleotidil transferasa terminal .
La inserción del nucleótido P es la inserción de secuencias palindrómicas codificadas por los extremos de los segmentos genéticos recombinantes.
Las repeticiones de trinucleótidos se clasifican como mutaciones de inserción [2] [3] y, a veces, como una clase separada de mutaciones. [4]
La nucleasa de dedo de zinc (ZFN) , las nucleasas efectoras de tipo activador de la transcripción (TALEN) y la edición genética CRISPR son los tres métodos principales utilizados en la investigación anterior para lograr la inserción genética. Y las herramientas CRISPR/Cas ya se han convertido en uno de los métodos más utilizados para presentar investigaciones.
Basándose en las herramientas CRISPR/Cas , ya se han desarrollado diferentes sistemas para lograr funciones específicas. Por ejemplo, una estrategia es el sistema de corte por nucleasas de doble cadena, utilizando la proteína Cas9 normal con ARN guía simple (sgRNA) y luego logrando la inserción del gen mediante la unión de extremos o la división de células con el sistema de reparación del ADN . [5] Otro ejemplo es el sistema de edición primaria , que utiliza la nickasa Cas9 y el ARN guía de edición primaria (pegRNA) que lleva los genes objetivo. [5]
Una limitación de la tecnología actual es que el tamaño para la inserción precisa del ADN no es lo suficientemente grande [6] como para satisfacer la demanda de investigación genómica. La transposición de ADN guiada por ARN es un área emergente para resolver este problema. [7] Se espera que se desarrollen y apliquen métodos más eficientes en el área de ingeniería genómica.
Las inserciones pueden ser particularmente peligrosas si ocurren en un exón , la región codificante de aminoácidos de un gen . Una mutación por desplazamiento del marco , una alteración en el marco de lectura normal de un gen, resulta si el número de nucleótidos insertados no es divisible por tres, es decir, el número de nucleótidos por codón . Las mutaciones por desplazamiento del marco alterarán todos los aminoácidos codificados por el gen después de la mutación. Por lo general, las inserciones y la posterior mutación por desplazamiento del marco harán que la traducción activa del gen encuentre un codón de terminación prematuro , lo que dará como resultado el final de la traducción y la producción de una proteína truncada. Las transcripciones que llevan la mutación por desplazamiento del marco también pueden degradarse a través de la descomposición mediada por sinsentidos durante la traducción, por lo que no dan como resultado ningún producto proteico. Si se traducen, las proteínas truncadas con frecuencia no pueden funcionar correctamente o no funcionan en absoluto y pueden dar como resultado cualquier número de trastornos genéticos dependiendo del gen en el que se produce la inserción. [8]
Las inserciones en el marco de lectura se producen cuando el marco de lectura no se altera como resultado de la inserción; el número de nucleótidos insertados es divisible por tres. El marco de lectura permanece intacto después de la inserción y la traducción probablemente se completará si los nucleótidos insertados no codifican un codón de terminación. Sin embargo, debido a los nucleótidos insertados, la proteína terminada contendrá, dependiendo del tamaño de la inserción, múltiples aminoácidos nuevos que pueden afectar la función de la proteína.