Un defecto de Schottky es una excitación de las ocupaciones de sitio en una red cristalina que conduce a defectos puntuales que llevan el nombre de Walter H. Schottky . En los cristales iónicos , este defecto se forma cuando iones con carga opuesta abandonan sus sitios de red y se incorporan, por ejemplo, en la superficie, creando vacantes con carga opuesta . Estas vacantes se forman en unidades estequiométricas para mantener una carga neutra general en el sólido iónico.
Los defectos de Schottky consisten en sitios de aniones y cationes desocupados en una proporción estequiométrica. Para un cristal iónico simple de tipo A − B + , un defecto de Schottky consta de una única vacante aniónica (A) y una única vacante catiónica (B), o v•
A+v
B siguiendo la notación de Kröger-Vink . Para un cristal más general con fórmula A x B y , un grupo Schottky está formado por x vacantes de A e y vacantes de B, por lo que se conservan la estequiometría general y la neutralidad de carga. Conceptualmente, se genera un defecto de Schottky si el cristal se expande en una celda unitaria, cuyos sitios vacíos previos se llenan con átomos que se difunden fuera del interior, creando así vacantes en el cristal.
Los defectos de Schottky se observan con mayor frecuencia cuando existe una pequeña diferencia de tamaño entre los cationes y aniones que componen un material.
Ecuaciones químicas en notación de Kröger-Vink para la formación de defectos Schottky en TiO 2 y BaTiO 3 .
Esto se puede ilustrar esquemáticamente con un diagrama bidimensional de una red cristalina de cloruro de sodio :


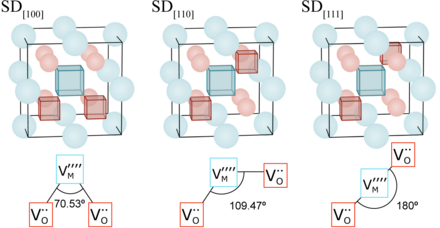
Las vacantes que constituyen los defectos de Schottky tienen carga opuesta, por lo que experimentan una fuerza de Coulomb mutuamente atractiva . A baja temperatura, pueden formar racimos unidos.
Los grupos unidos suelen ser menos móviles que sus homólogos diluidos, ya que varias especies necesitan moverse en un movimiento concertado para que todo el grupo migre. Esto tiene implicaciones importantes para numerosas cerámicas funcionales utilizadas en una amplia gama de aplicaciones, incluidos conductores iónicos , pilas de combustible de óxido sólido y combustible nuclear . [1]
Este tipo de defecto se observa típicamente en compuestos altamente iónicos , compuestos altamente coordinados y donde solo hay una pequeña diferencia en los tamaños de los cationes y aniones que componen la red compuesta. Las sales típicas donde se observa el trastorno de Schottky son NaCl , KCl , KBr , CsCl y AgBr . [ cita necesaria ] Para aplicaciones de ingeniería, los defectos Schottky son importantes en óxidos con estructura de fluorita , como CeO 2 , ZrO 2 cúbico , UO 2 , ThO 2 y PuO 2 . [ cita necesaria ]
Normalmente, el volumen de formación de una vacante es positivo: la contracción de la red debido a las tensiones alrededor del defecto no compensa la expansión del cristal debido al número adicional de sitios. Por tanto, la densidad del cristal sólido es menor que la densidad teórica del material.