La ADN girasa , o simplemente girasa , es una enzima dentro de la clase de topoisomerasa y es una subclase de topoisomerasas de tipo II [1] que reduce la tensión topológica de una manera dependiente de ATP mientras el ADN bicatenario se desenrolla mediante la elongación de la ARN polimerasa [2] o mediante la helicasa delante de la horquilla de replicación progresiva . [3] [4] Es la única enzima conocida que contribuye activamente al superenrollamiento negativo del ADN, mientras que también es capaz de relajar los superenrollamientos positivos. Lo hace enrollando la plantilla para formar un cruce, luego cortando una de las dobles hélices y pasando la otra a través de ella antes de liberar la ruptura, cambiando el número de enlace por dos en cada paso enzimático. Este proceso ocurre en las bacterias , cuyo ADN circular simple es cortado por la ADN girasa y luego los dos extremos se retuercen uno alrededor del otro para formar superenrollamientos. La girasa también se encuentra en plástidos eucariotas : se ha encontrado en el apicoplasto del parásito de la malaria Plasmodium falciparum [5] [6] y en los cloroplastos de varias plantas. [7] La ADN girasa bacteriana es el objetivo de muchos antibióticos , incluidos el ácido nalidíxico , la novobiocina , la albicidina y la ciprofloxacina .
La capacidad única de la girasa para introducir superenrollamientos negativos en el ADN a expensas de la hidrólisis de ATP [1] es lo que permite que el ADN bacteriano tenga superenrollamientos negativos libres. La capacidad de la girasa para relajar los superenrollamientos positivos entra en juego durante la replicación del ADN y la transcripción procariota . La naturaleza helicoidal del ADN hace que los superenrollamientos positivos se acumulen por delante de una enzima translocadora, en el caso de la replicación del ADN, una ADN polimerasa . La capacidad de la girasa (y la topoisomerasa IV ) para relajar los superenrollamientos positivos permite que se libere la tensión superhelicoidal por delante de la polimerasa para que la replicación pueda continuar.
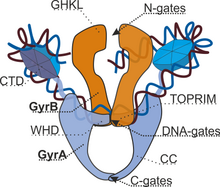
La ADN girasa es una enzima tetramérica que consta de 2 subunidades GyrA ("A") y 2 subunidades GyrB ("B"). [8] Estructuralmente, el complejo está formado por 3 pares de "puertas", cuya apertura y cierre secuencial da como resultado la transferencia directa de segmentos de ADN y la introducción de 2 superenrollamientos negativos. Las puertas N están formadas por dominios ATPasa de las subunidades GyrB. La unión de 2 moléculas de ATP conduce a la dimerización y, por lo tanto, al cierre de las puertas. La hidrólisis, por el contrario, las abre. La escisión y reunión del ADN se realiza mediante un centro catalítico ubicado en las puertas de ADN construidas por todas las subunidades de la girasa. Las puertas C están formadas por subunidades GyrA. [9]

Un estudio de una sola molécula [10] ha caracterizado la actividad de la girasa como una función de la tensión del ADN (fuerza aplicada) y el ATP , y ha propuesto un modelo mecanoquímico. Tras la unión al ADN (el estado "Girasa-ADN"), hay una competencia entre la envoltura del ADN y la disociación, donde el aumento de la tensión del ADN aumenta la probabilidad de disociación. Según el ciclo catalítico propuesto, la unión de 2 moléculas de ATP provoca la dimerización de los dominios de ATPasa de las subunidades GyrB y la captura de un segmento T de ADN (T- de transferring ) en una cavidad entre las subunidades GyrB. En un siguiente paso, la enzima escinde un segmento G de ADN (G- de gate ) haciendo una rotura de doble cadena . Luego, el segmento T se transfiere a través de la rotura, lo que va acompañado de la hidrólisis de la primera molécula de ATP. La ADN-girasa liga la rotura en un segmento G de nuevo y el segmento T finalmente abandona el complejo enzimático. La hidrólisis del segundo ATP devuelve el sistema al paso inicial de un ciclo. [11] Como resultado de un ciclo catalítico, se hidrolizan dos moléculas de ATP y se introducen dos superenrollamientos negativos en la plantilla de ADN. Se ha calculado que el número de vueltas superhelicoidales introducidas en un ADN circular inicialmente relajado es aproximadamente igual al número de moléculas de ATP hidrolizadas por la girasa. [12] Por lo tanto, se puede sugerir que se hidrolizan dos moléculas de ATP por ciclo de reacción por la girasa, lo que conduce a la introducción de una diferencia de enlace de -2. [13]
La girasa tiene una especificidad pronunciada para los sustratos de ADN. Se encontraron fuertes sitios de unión de girasa (SGS) en algunos fagos ( grupo Mu del bacteriófago ) y plásmidos ( pSC101 , pBR322 ). Recientemente, el mapeo de alto rendimiento de los sitios de girasa de ADN en el genoma de Escherichia coli utilizando el enfoque Topo-Seq [2] reveló un motivo de unión largo (≈130 pb) y degenerado que puede explicar la existencia de SGS. El motivo de girasa refleja la envoltura del ADN alrededor del complejo enzimático y la flexibilidad del ADN. Contiene dos regiones periódicas en las que las islas ricas en GC se alternan con parches ricos en AT por un período cercano al período de la doble hélice del ADN (≈10,5 pb). Las dos regiones corresponden a la unión del ADN por los dominios C-terminales de las subunidades GyrA y se asemejan al motivo de unión del nucleosoma eucariota. [2]
La girasa está presente en procariotas y algunos eucariotas, pero las enzimas no son completamente similares en estructura o secuencia y tienen diferentes afinidades para diferentes moléculas. Esto hace que la girasa sea un buen objetivo para los antibióticos . Dos clases de antibióticos que inhiben la girasa son:
La subunidad A se inactiva selectivamente con antibióticos como los ácidos oxolínico y nalidíxico. La subunidad B se inactiva selectivamente con antibióticos como la cumermicina A 1 y la novobiocina. La inhibición de cualquiera de las subunidades bloquea la actividad de supertorsión. [16]
Los genes 39, 52 y 60 del fago T4 codifican proteínas que forman una ADN girasa que se emplea en la replicación del ADN del fago durante la infección del huésped bacteriano E. coli . [17] La proteína del gen 52 del fago comparte homología con la subunidad gyrA de la girasa bacteriana [18] y la proteína del gen 39 del fago comparte homología con la subunidad gyrB. [19] Dado que la ADN girasa del huésped E. coli puede compensar parcialmente la pérdida de los productos del gen del fago, los mutantes defectuosos en los genes 39, 52 o 60 no eliminan por completo la replicación del ADN del fago, sino que retrasan su inicio. [17] Los mutantes defectuosos en los genes 39, 52 o 60 muestran una mayor recombinación genética , así como una mayor mutación por sustitución de bases y deleción , lo que sugiere que la síntesis de ADN compensada del huésped es menos precisa que la dirigida por el fago de tipo salvaje. [20] Un mutante defectuoso en el gen 39 también muestra una mayor sensibilidad a la inactivación por irradiación ultravioleta durante la etapa de infección del fago después del inicio de la replicación del ADN cuando hay múltiples copias del cromosoma del fago. [21]