La hipoglicina A es un derivado de aminoácido natural que se encuentra en el fruto inmaduro del árbol Ackee ( Blighia sapida ) [1] y en las semillas del saúco ( Acer negundo ). [2] Es tóxico si se ingiere y es el agente causante de la enfermedad del vómito jamaicano . [1] Un informe de Lancet de 2017 estableció un vínculo entre el consumo de lichis verdes (que contienen hipoglicina A o metilenciclopropilglicina (MCPG)), que provoca hipoglucemia y muerte por encefalopatía tóxica aguda. [3]
La totalidad de la fruta inmadura de Ackee es tóxica y contiene grandes cantidades de hipoglicina. La fruta es segura para comer solo cuando se le permite abrirse completamente y exponer las grandes semillas negras mientras está en el árbol. Sin embargo, los niveles de toxina disminuyen con el tiempo desde aproximadamente 1000 ppm a alrededor de 0,1 ppm en la fruta madura. [4]
Los parientes del Ackee, incluidos el lichi , el longan y el rambután , pueden contener suficiente α-(metilenciclopropil)glicina, un homólogo de la hipoglicina A, en su fruta para causar encefalopatía hipoglucémica en niños desnutridos, cuando se consumen en grandes cantidades. [5]
La hipoglicina A es una protoxina , lo que significa que la molécula no es tóxica en sí misma, pero se descompone en productos tóxicos cuando se ingiere. El complejo alfa-cetoácido deshidrogenasa de cadena ramificada , que normalmente convierte leucina , isoleucina o valina en derivados de acil-CoA , convierte la hipoglicina A en MCPA - CoA altamente tóxica . El cofactor FAD necesario para la beta oxidación de los ácidos grasos se asocia con el carbono alfa de MCPA-CoA creando un complejo irreversible que desactiva la enzima. Además, MCPA-CoA bloquea algunas enzimas necesarias para la gluconeogénesis . [4]
Se cree que la reducción de la gluconeogénesis y la reducción de la oxidación de los ácidos grasos son la causa de la mayoría de los síntomas de la enfermedad del vómito de Jamaica. El bloqueo del metabolismo de los ácidos grasos hace que las células comiencen a utilizar glucógeno para obtener energía. Una vez que se agota el glucógeno, el cuerpo no puede producir más, lo que provoca una hipoglucemia grave. Estos efectos bioquímicos se detectan por un exceso de ácidos grasos de cadena media en la orina y acidosis . Los tratamientos clave tienen como objetivo evitar o contrarrestar los cambios bioquímicos e incluyen líquidos y glucosa por vía intravenosa , y hemodiálisis en el caso de insuficiencia renal . [6]
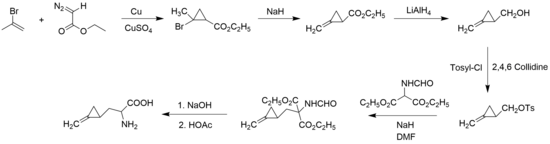
En 1958, John Carbon, William Martin y Leo Swett fueron los primeros en sintetizar hipoglicina A, en forma racémica , a partir de 2-bromopropeno y diazoacetato de etilo para formar el anillo de ciclopropano . [7]
En 1992, Jack Baldwin , Robert Adlington, David Bebbington y Andrew Russell lograron la primera síntesis total asimétrica de los diastereoisómeros individuales de la hipoglicina A, utilizando la epoxidación Sharpless para permitir una síntesis asimétrica de metileno ciclopropano. [8] [9] Los estudios de 1 H NMR y dicroísmo circular identifican el diastereoisómero mayor de la hipogicina A natural como (2 S , 4 R ) y el diastereoisómero menor como (2 S , 4 S ).