El óxido de trifenilfosfina (abreviado frecuentemente como TPPO) es un compuesto organofosforado con la fórmula OP(C 6 H 5 ) 3 , también escrito como Ph 3 PO o PPh 3 O (Ph = C 6 H 5 ). Es uno de los óxidos de fosfina más comunes . Este compuesto cristalino incoloro es un producto de desecho común pero potencialmente útil en reacciones que involucran trifenilfosfina . Es un reactivo popular para inducir la cristalización de compuestos químicos.
El Ph 3 PO está estructuralmente relacionado con el POCl 3 . [2] Como se estableció mediante cristalografía de rayos X , la geometría alrededor de P es tetraédrica y la distancia de PO es de 1,48 Å. [3] Se han encontrado otras modificaciones del Ph 3 PO: por ejemplo, una forma monoclínica cristaliza en el grupo espacial P 2 1 / c con Z = 4 y a = 15,066(1) Å, b = 9,037(2) Å, c = 11,296(3) Å y β = 98,47(1)°. La modificación ortorrómbica cristaliza en el grupo espacial Pbca con Z = 4 y 29,089(3) Å, b = 9,1347(9), c = 11,261(1) Å. [4]
El centro de oxígeno es relativamente básico. La rigidez de la cadena principal y la basicidad del centro de oxígeno hacen de esta especie un agente popular para cristalizar moléculas que de otro modo serían difíciles de cristalizar. Este truco es aplicable a moléculas que tienen átomos de hidrógeno ácidos, por ejemplo, los fenoles . [5]
El Ph3PO es un subproducto de muchas reacciones útiles en la síntesis orgánica, incluidas las reacciones de Wittig , Staudinger y Mitsunobu . También se forma cuando se emplea PPh3Cl2 para convertir alcoholes en cloruros de alquilo:
La trifenilfosfina se puede regenerar a partir del óxido mediante tratamiento con una variedad de agentes desoxigenantes, como fosgeno o triclorosilano /trietilamina: [6]
El óxido de trifenilfosfina puede ser difícil de eliminar de las mezclas de reacción por medio de cromatografía. Es poco soluble en hexano y éter dietílico frío . La trituración o cromatografía de productos crudos con estos solventes a menudo conduce a una buena separación del óxido de trifenilfosfina. Su eliminación se facilita mediante la conversión a su complejo Mg(II), que es poco soluble en tolueno o diclorometano y se puede filtrar. [7] Un método de filtración alternativo donde se forma ZnCl2 (TPPO)2 tras la adición de ZnCl2 se puede utilizar con solventes más polares como etanol, acetato de etilo y tetrahidrofurano. [8]
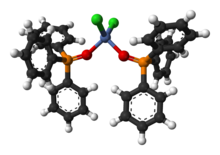
El Ph3PO forma una variedad de complejos . Un complejo representativo es la especie tetraédrica NiCl2 ( OPPh3 ) 2 . [ 9]
El pH 3 PO es una impureza común en el PPh 3 . La oxidación del PPh 3 por el oxígeno, incluido el aire, está catalizada por muchos iones metálicos:
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )