Los ácidos docosapentaenoicos epóxicos ( ácidos epoxidocosapentaenoicos , EDP o EpDPE ) son metabolitos del ácido graso omega-3 de cadena lineal de 22 carbonos , ácido docosahexaenoico (DHA). Los tipos de células que expresan ciertas epoxigenasas del citocromo P450 (CYP) metabolizan los ácidos grasos poliinsaturados (PUFA) convirtiendo uno de sus dobles enlaces en un epóxido . En la más conocida de estas vías metabólicas, las CYP epoxigenasas celulares metabolizan el ácido graso omega-6 de cadena lineal de 20 carbonos , ácido araquidónico , en ácidos epoxieicosatrienoicos (EET); otra vía de la CYP epoxigenasa metaboliza el ácido graso omega-3 de 20 carbonos, ácido eicosapentaenoico (EPA), en ácidos epoxieicosatetraenoicos (EEQ). Las epoxigenasas CYP convierten de manera similar otros PUFA en epóxidos (ver Epoxigenasa ). Estos metabolitos de epóxido tienen una variedad de actividades. Sin embargo, esencialmente todos ellos se convierten rápidamente en sus correspondientes, pero en general mucho menos activos, ácidos grasos dihidroxi vecinales por la ubicua hidrolasa de epóxido soluble celular (sEH; también denominada hidrolasa de epóxido 2). En consecuencia, estos epóxidos, incluidos los EDP, funcionan como agentes de señalización de corta duración que regulan la función de sus células madre o cercanas. La característica particular de los EDP (y EEQ) que los distingue de los EET es que derivan de los ácidos grasos omega-3 y se sugiere que son responsables de algunos de los efectos beneficiosos atribuidos a los ácidos grasos omega-3 y a los alimentos ricos en omega-3, como el aceite de pescado . [1]
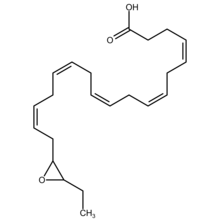
Los EDP son metabolitos del ácido eicosapentaenoico epóxido del DHA. El DHA tiene 6 enlaces dobles cis (ver isomería cis-trans ) , cada uno de los cuales se encuentra entre los carbonos 4-5, 7-8, 10-11, 13-14, 16-17 o 19-20. Las epoxigenasas del citocromo P450 atacan cualquiera de estos enlaces dobles para formar un regioisómero de epóxido de ácido docosapentaenoico (DPA) respectivo (ver Isómero estructural § Isomería de posición (regioisomería) ). Por lo tanto, una epoxigenasa dada puede convertir DHA en 4,5-EDP (es decir, 4,5-epoxi-7 Z ,10 Z , 13 Z ,16 Z , 19 Z -DPA), 7,8-EDP (es decir, 7,8-epoxi-4 Z ,10 Z , 13 Z ,16 Z , 19 Z -DPA), 10,11-EDP (es decir, 10,11-epoxi-4 Z ,7 Z ,13 Z ,16 Z ,19 Z -DPA), 13,14-EDP (es decir, 13,14-epoxi-4 Z ,7 Z ,10 Z ,16 Z ,19 Z -DPA), 16,17-EDP (es decir, 16,17-epoxi-4 Z ,7 Z ,10 Z ,13 Z ,19 Z -DPA, o 19,20-EDP (es decir, 19,20-epoxi-4 Z , 7 Z , 10 Z , 13 Z , 16 Z -DPA. Las enzimas epoxigenasas generalmente forman ambos enantiómeros R / S en cada posición de doble enlace anterior; por ejemplo, las epoxidasas del citocromo P450 atacan al DHA en la posición del doble enlace 16,17 para formar dos enantiómeros epóxidos, 16 R , 17 S -EDP y 16 S , 17 S -EDP. [2] El metabolito 4,5-EDP es inestable y generalmente no se detecta entre el EDP formado por las células. [3]
Las enzimas de la superfamilia del citocromo P450 (CYP) que se clasifican como epoxigenasas en función de su capacidad para metabolizar los PUFA, en particular el ácido araquidónico, a epóxidos incluyen: CYP1A, CYP2B, CYP2C, CYP2E, CYP2J y, dentro de la subfamilia CYP3A, CYP3A4. En los seres humanos, las isoformas CYP2C8 , CYP2C9 , CYP2C19 , CYP2J2 y posiblemente CYP2S1 parecen ser las principales epoxigenasas responsables de metabolizar el ácido araquidónico a EET (véase Ácido epoxieicosatrienoico § Producción ). En general, estas mismas epoxigenasas CYP también metabolizan DHA a EDP (así como EPA a EEQ; aún no se ha probado la capacidad de metabolizar DHA de CYP2S1), haciéndolo a tasas que a menudo son mayores que sus tasas de metabolización de ácido araquidónico a EET; es decir, el DHA (y el EPA) parecen ser preferidos sobre el ácido araquidónico como sustratos para muchas de las epoxigenasas CYP. [4] CYP1A1 , CYP1A2 , CYP2C18 , CYP2E1 , CYP4A11 , CYP4F8 y CYP4F12 también metabolizan DHA a EDP. [5] CYP2C8, CYP2C18, CYP2E1, CYP2J2, VYP4A11, CYP4F8 y CYP4F12 atacan preferentemente el doble enlace omega-3 terminal que distingue al DHA de los ácidos grasos omega-6 y, por lo tanto, metabolizan el DHA principalmente a isómeros 19,20-EDP, mientras que CYP2C19 metaboliza el DHA a isómeros 7,8-EDP, 10,11-EDP y 19,20-EDP [5] [6] CYP2J2 metaboliza el DHA a EPA, principalmente 19,20-EPA, al doble de la velocidad a la que metaboliza el ácido araquidónico a EET. [7] Además de los CYP citados, CYP4A11 , CYP4F8 , CYP4F12 , CYP1A1 , CYP1A2 y CYP2E1 , que se clasifican como CYP monooxigenasas en lugar de CYP epoxigenasas porque metabolizan el ácido araquidónico en ácidos monohidroxieicosatetraenoicos (véase Ácido 20-hidroxieicosatetraenoico ), es decir, el ácido 19-hidroxieicosatetraenoico y/o el ácido 20-hidroxieicosatetranoico, asumen la actividad epoxigenasa al convertir DHA principalmente en isómeros 19,20-EDP (véase Ácido epoxieicosatrienoico ). [5] Las epoxigenasas CYP450 capaces de metabolizar DHA a EDP están ampliamente distribuidas en órganos y tejidos como el hígado, riñón, corazón, pulmón, páncreas, intestino, vasos sanguíneos, leucocitos sanguíneos y cerebro. [8] [9] Se sabe que estos tejidos metabolizan el ácido araquidónico a EET; se ha demostrado o se presume que también metabolizan DHA a EPD. [10] [11] [12]
Los EDP se producen comúnmente mediante la estimulación de tipos celulares específicos por los mismos mecanismos que producen EET (ver Ácido epoxieicosatrienoico ). Es decir, la estimulación celular hace que el DHA se libere de la posición sn-2 de sus reservas celulares de fosfolípidos unidos a la membrana a través de la acción de una enzima de tipo fosfolipasa A2 y el posterior ataque del DHA liberado por las epoxidasas CYP450. Es notable que el consumo de dietas ricas en ácidos grasos omega-3 aumenta drásticamente los niveles séricos y tisulares de EDP y EEQ en animales, así como en humanos. De hecho, este aumento en los niveles de EDP (y EEQ) en humanos es, con mucho, el cambio más destacado en el perfil de metabolitos de PUFA causado por los ácidos grasos omega-3 de la dieta y, se sugiere, puede ser responsable de al menos algunos de los efectos beneficiosos atribuidos a los ácidos grasos omega-3 de la dieta. [1] [13]
De manera similar a los EET (ver Ácido epoxieicosatrienoico ), los EDP se metabolizan rápidamente en las células por una epóxido hidrolasa soluble citosólica (sEH, también denominada epóxido hidrolasa 2 [EC 3.2.2.10.]) para formar sus correspondientes ácidos dihidroxieicosapentaenoicos de diol vecinales . Por lo tanto, la sEH convierte 19,20-EDP en ácido 19,10-dihidroxidocosapentaenoico (DPA), 16,17-EDP en 16,17-dihidroxi-DPA, 13,14-EDP en 13,14-dihidroxi-DPA, 10,11-EDP en 10,11-dihidroxi-DPA y 7,8-EDP en 7,8-dihidroxi-EDP; el 4,5-EDP es inestable y, por lo tanto, generalmente no se detecta en las células. [14] Los productos de dihidroxi-EDP, al igual que sus precursores epoxi, son mezclas de enantiómeros ; por ejemplo, sEH convierte 16,17-EDP en una mezcla de 16( S ),17( R )-dihidroxi-DPA y 16( R ),17( S )-dihidroxi-DPA. [2] Estos dihidroxi-DPA suelen ser mucho menos activos que sus precursores epóxidos. La vía sEH actúa rápidamente y es, con mucho, la vía predominante de inactivación de EDP; su funcionamiento hace que los EDP funcionen como mediadores de corta duración cuyas acciones se limitan a sus células parentales y cercanas, es decir, son agentes de señalización autocrinos y paracrinos , respectivamente. [14] [15] [16]
Además de la vía sEH, los EDP, de manera similar a los EET, pueden acilarse en fosfolípidos en una reacción similar a la acilación ; esta vía puede servir para limitar la acción de los EET o almacenarlos para su liberación futura. [2] Finalmente, nuevamente de manera similar a los EET, los EDP están sujetos a inactivación al ser metabolizados aún más por oxidación beta . [17]
Los EDP no se han estudiado tan bien como los EET. Este es particularmente el caso de los estudios en animales sobre su posible importancia clínica. En comparación con una selección de las muchas actividades atribuidas a los EET (ver Ácido epoxieicosatrienoico ), los estudios en animales informados hasta la fecha encuentran que ciertos EDP (16,17-EDP y 19,20-EDP han sido examinados con mayor frecuencia) son: 1) más potentes que los EET en la disminución de la hipertensión y la percepción del dolor; 2) más potentes o al menos igual en potencia que los EET en la supresión de la inflamación; y 3) actúan de manera opuesta a los EET en que los EDP inhiben la angiogénesis , la migración de células endoteliales, la proliferación de células endoteliales y el crecimiento y la metástasis de líneas celulares de cáncer de mama y próstata humanos, mientras que los EET tienen efectos estimulantes en cada uno de estos sistemas. [1] [3] [16] [17] Como se indica en la sección Metabolismo, el consumo de dietas ricas en ácidos grasos omega-3 aumenta drásticamente los niveles séricos y tisulares de EDP y EEQ en animales y humanos, y en los humanos es, con mucho, el cambio más destacado en el perfil de metabolitos de PUFA causado por los ácidos grasos omega-3 de la dieta. Por lo tanto, el metabolismo de DHA a EDP (y de EPA a EEQ) puede ser responsable de al menos algunos de los efectos beneficiosos atribuidos a los ácidos grasos omega-3 de la dieta. [1] [13] [17]