
El ácido tríflico , el nombre corto del ácido trifluorometanosulfónico , TFMS , TFSA , HOTf o TfOH , es un ácido sulfónico con la fórmula química CF3SO3H . Es uno de los ácidos más fuertes conocidos . El ácido tríflico se utiliza principalmente en investigación como catalizador para la esterificación . [ 2] [3] Es un líquido higroscópico , incoloro, ligeramente viscoso y es soluble en disolventes polares .
El ácido trifluorometanosulfónico se produce industrialmente mediante fluoración electroquímica (ECF) del ácido metanosulfónico :
El CF3SO2F resultante se hidroliza y la sal triflato resultante se vuelve a tonar. Alternativamente, el ácido trifluorometanosulfónico surge por oxidación del cloruro de trifluorometilsulfenilo : [4]
El ácido tríflico se purifica por destilación del anhídrido tríflico . [3]
El ácido trifluorometanosulfónico fue sintetizado por primera vez en 1954 por Robert Haszeldine y Kidd mediante la siguiente reacción: [5]
En el laboratorio, el ácido tríflico es útil en protonaciones porque la base conjugada del ácido tríflico no es nucleófila. También se utiliza como valorante ácido en la titulación ácido-base no acuosa porque se comporta como un ácido fuerte en muchos disolventes ( acetonitrilo , ácido acético , etc.) donde los ácidos minerales comunes (como HCl o H 2 SO 4 ) son solo moderadamente fuertes.
Con una K a =5 × 10 14 , p K a =−14,7 ± 2,0 , [1] El ácido tríflico se considera un superácido . Debe muchas de sus propiedades útiles a su gran estabilidad térmica y química. Tanto el ácido como su base conjugada CF 3 SO−
3Los triflatos , conocidos como triflatos , resisten las reacciones de oxidación/reducción , mientras que muchos ácidos fuertes son oxidantes, como el ácido perclórico o el nítrico . Además, se recomienda su uso porque el ácido tríflico no sulfona los sustratos, lo que puede ser un problema con el ácido sulfúrico , el ácido fluorosulfúrico y el ácido clorosulfónico . A continuación se muestra una sulfonación prototípica, que el ácido tríflico no experimenta:
El ácido tríflico se evapora en aire húmedo y forma un sólido monohidrato estable, CF 3 SO 3 H·H 2 O, punto de fusión 34 °C.
El ligando triflato es lábil, lo que refleja su baja basicidad. El ácido trifluorometanosulfónico reacciona exotérmicamente con carbonatos , hidróxidos y óxidos metálicos. Un ejemplo ilustrativo es la síntesis de Cu(OTf) 2 . [6]
Los ligandos de cloruro se pueden convertir en los triflatos correspondientes:
Esta conversión se lleva a cabo en HOTf puro a 100 °C, seguida de la precipitación de la sal tras la adición de éter.
El ácido tríflico reacciona con haluros de acilo para dar anhídridos triflatos mixtos, que son agentes acilantes fuertes, por ejemplo, en las reacciones de Friedel-Crafts .
El ácido tríflico cataliza la reacción de compuestos aromáticos con cloruros de sulfonilo, probablemente también a través de la intermediación de un anhídrido mixto del ácido sulfónico.
El ácido tríflico promueve otras reacciones similares a las de Friedel-Crafts, como el craqueo de alcanos y la alquilación de alquenos, que son muy importantes para la industria petrolera. Estos catalizadores derivados del ácido tríflico son muy eficaces para isomerizar hidrocarburos de cadena lineal o ligeramente ramificados que pueden aumentar el índice de octano de un combustible a base de petróleo en particular.
El ácido tríflico reacciona exotérmicamente con alcoholes para producir éteres y olefinas.
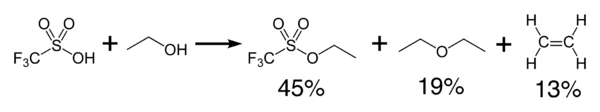
La deshidratación produce el anhídrido de ácido , anhídrido trifluorometanosulfónico , ( CF3SO2 ) 2O .
El ácido tríflico es uno de los ácidos más fuertes. El contacto con la piel provoca quemaduras graves con destrucción retardada del tejido. La inhalación provoca espasmos letales, inflamación y edema . [7]
Al igual que el ácido sulfúrico, el ácido tríflico debe agregarse lentamente a los solventes polares para evitar el descontrol térmico .