Las saponinas (del latín "sapon", jabón + "-in", uno de) son metabolitos secundarios derivados de plantas , generalmente tóxicos y de sabor amargo , que son sustancias químicas orgánicas , que tienen una calidad espumosa cuando se agitan en agua y un alto peso molecular . Están presentes en una amplia gama de especies de plantas en la corteza , hojas , tallos, raíces y flores , pero se encuentran particularmente en la saponaria (género Saponaria ), una planta con flores, el árbol de corteza de jabón ( Quillaja saponaria ), la agrostemma githago L., la gypsophila spp . y la soja ( Glycine max L.). Se utilizan en jabones, medicamentos (por ejemplo, adyuvantes de medicamentos), extintores de incendios, como suplementos dietéticos, para la síntesis de esteroides y en bebidas carbonatadas (por ejemplo, son responsables de mantener la espuma en la cerveza de raíz ). Las saponinas son solubles en agua y grasa, lo que les da sus útiles propiedades jabonosas. Algunos ejemplos de estos productos químicos son la glicirricina ( saborizante de regaliz ) y la quillaia (alt. quillaja), un extracto de corteza utilizado en bebidas. [1] [2] [3]
Estructuralmente, son glicósidos con al menos un enlace glicosídico entre una cadena de azúcar ( glicona ) y la otra molécula orgánica no azúcar ( aglicona ). [ cita requerida ]
Los glicósidos esteroides son saponinas con átomos de 27-C. [4] Son triterpenoides modificados donde su aglicón es un esteroide , estos compuestos consisten típicamente en un aglicón esteroide unido a una o más moléculas de azúcar , que pueden tener varias actividades biológicas. Estos compuestos son conocidos por sus importantes propiedades citotóxicas , neurotróficas y antibacterianas . Estos también pueden usarse para la síntesis parcial de hormonas sexuales o esteroides . [5] [1]
Los glicósidos triterpénicos son glicósidos naturales presentes en varias plantas , hierbas y pepinos de mar [6] y poseen átomos de 30-C. [4] Estos compuestos consisten en un aglicón triterpénico unido a una o más moléculas de azúcar . Los glicósidos triterpénicos exhiben una amplia gama de actividades biológicas y propiedades farmacológicas, lo que los hace valiosos en la medicina tradicional y el descubrimiento de fármacos modernos. [1]
Las saponinas son una subclase de terpenoides, la clase más grande de extractos de plantas. La naturaleza anfipática de las saponinas les da actividad como surfactantes con capacidad potencial para interactuar con componentes de la membrana celular , como el colesterol y los fosfolípidos , posiblemente haciendo que las saponinas sean útiles para el desarrollo de cosméticos y medicamentos . [7] Las saponinas también se han utilizado como adyuvantes en el desarrollo de vacunas , [8] como Quil A , un extracto de la corteza de Quillaja saponaria . [7] [9] Esto las hace de interés para su posible uso en vacunas de subunidades y vacunas dirigidas contra patógenos intracelulares. [8] En su uso como adyuvantes para la fabricación de vacunas, la toxicidad asociada con la complejación de esteroles sigue siendo una preocupación. [10]
El quillay es tóxico cuando se consume en grandes cantidades, lo que puede provocar daño hepático , dolor gástrico, diarrea u otros efectos adversos . [9] El NOAEL de saponinas es de alrededor de 300 mg/kg en roedores, por lo que una dosis de 3 mg/kg debería ser segura con un factor de seguridad (ver Índice terapéutico ) de 100. [11]
Las saponinas se utilizan por sus efectos sobre las emisiones de amoníaco en la alimentación animal. [12] En los Estados Unidos, los investigadores están explorando el uso de saponinas derivadas de plantas para controlar especies de gusanos invasores, incluido el gusano saltador. [13] [14]
El principal uso histórico de estas plantas era hervirlas para hacer jabón. La Saponaria officinalis es la más adecuada para este procedimiento, pero también funcionan otras especies relacionadas. La mayor concentración de saponina se produce durante la floración, y la mayor parte de esta se encuentra en los tallos leñosos y las raíces, pero las hojas también contienen algo de saponina.
Las saponinas han sido históricamente derivadas de plantas, pero también han sido aisladas de organismos marinos como el pepino de mar . [15] Derivan su nombre de la planta saponaria (género Saponaria , familia Caryophyllaceae ), cuya raíz se usó históricamente como jabón. [1] [16] [2] En otros representantes de esta familia, por ejemplo Agerostemma githago , Gypsophila spp. y Dianthus sp ., las saponinas también están presentes en grandes cantidades. [17] Las saponinas también se encuentran en la familia botánica Sapindaceae , incluido su género definitorio Sapindus (baya de jabón o nuez de jabón) y el castaño de Indias , y en las familias estrechamente relacionadas Aceraceae (arces) e Hippocastanaceae . También se encuentra abundantemente en Gynostemma pentaphyllum ( Cucurbitaceae ) en una forma llamada gypenosides, y ginseng o ginseng rojo ( Panax , Araliaceae ) en una forma llamada ginsenósidos . Las saponinas también se encuentran en la fruta verde de Manilkara zapota (también conocida como sapodillas), lo que resulta en propiedades altamente astringentes. Nerium oleander ( Apocynaceae ), también conocida como adelfa blanca, es una fuente de la potente toxina cardíaca oleandrina . Dentro de estas familias, esta clase de compuestos químicos se encuentra en varias partes de la planta: hojas, tallos, raíces, bulbos, flores y frutos. [18] Las formulaciones comerciales de saponinas derivadas de plantas, por ejemplo, del árbol de corteza de jabón, Quillaja saponaria , y las de otras fuentes están disponibles a través de procesos de fabricación controlados, que las hacen útiles como reactivos químicos y biomédicos. [19] Las saponinas de soja son un grupo de saponinas triterpenoides de tipo oleanano estructuralmente complejas que incluyen soyasapogenol (aglicona) y fracciones de oligosacáridos biosintetizadas en los tejidos de la soja . Las saponinas de soja se asociaron previamente a interacciones planta-microbio [20] a partir de exudados de raíces y estreses abióticos, como deficiencia nutricional. [21]
En las plantas, las saponinas pueden actuar como antialimentarios , [2] y proteger a la planta contra microbios y hongos . [ cita requerida ] Algunas saponinas vegetales (por ejemplo, de la avena y la espinaca) pueden mejorar la absorción de nutrientes y ayudar en la digestión animal . Sin embargo, las saponinas suelen tener un sabor amargo, por lo que pueden reducir la palatabilidad de las plantas (por ejemplo, en los alimentos para el ganado), o incluso imbuirlas de una toxicidad animal potencialmente mortal . Algunas saponinas son tóxicas para los organismos de sangre fría y los insectos en concentraciones particulares. Se necesita más investigación para definir las funciones de estos productos naturales en sus organismos hospedadores, que se han descrito como "poco comprendidos" hasta la fecha. [22]
La mayoría de las saponinas, que se disuelven fácilmente en el agua, son venenosas para los peces . [23] Por lo tanto, en etnobotánica , se sabe que los pueblos indígenas las utilizan para obtener fuentes de alimentos acuáticos. Desde tiempos prehistóricos, las culturas de todo el mundo han utilizado plantas que matan peces , que normalmente contienen saponinas, para pescar. [24] [25] [26]
Aunque la ley lo prohíbe, las plantas venenosas para peces todavía son ampliamente utilizadas por las tribus indígenas de Guyana . [27]
En el subcontinente indio, el pueblo Gondi utiliza extractos de plantas venenosas para pescar. [28]
En el siglo XVI, la planta rica en saponinas, Agrostemma githago, se utilizó para tratar úlceras, fístulas y hemorragias. [29]
Muchas de las tribus nativas americanas de California usaban tradicionalmente la raíz de jabón (género Chlorogalum ) y/o la raíz de varias especies de yuca , que contienen saponina, como veneno para peces. Pulverizaban las raíces, las mezclaban con agua para generar espuma y luego vertían la espuma en un arroyo. Esto mataba o incapacitaba a los peces, que podían ser recogidos fácilmente de la superficie del agua. Entre las tribus que usaban esta técnica estaban los Lassik , los Luiseño y los Mattole . [30]
La gran heterogeneidad de estructuras subyacentes a esta clase de compuestos dificulta las generalizaciones; son una subclase de terpenoides , derivados oxigenados de hidrocarburos terpénicos. Los terpenos, a su vez, están formados formalmente por unidades de isopreno de cinco carbonos (la base esteroide alternativa es un terpeno al que le faltan algunos átomos de carbono). Los derivados se forman sustituyendo otros grupos por algunos de los átomos de hidrógeno de la estructura de la base. En el caso de la mayoría de las saponinas, uno de estos sustituyentes es un azúcar, por lo que el compuesto es un glicósido de la molécula base. [1]
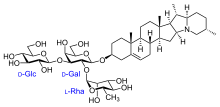
Más específicamente, la estructura de base lipófila de una saponina puede ser un triterpeno, un esteroide (como el espirostanol o el furostanol) o un alcaloide esteroidal (en el que los átomos de nitrógeno reemplazan a uno o más átomos de carbono). Alternativamente, la estructura de base puede ser una cadena de carbono acíclica en lugar de la estructura de anillo típica de los esteroides. Una o dos (raramente tres) unidades de monosacáridos hidrófilos (azúcares simples) se unen a la estructura de base a través de sus grupos hidroxilo (OH). En algunos casos, están presentes otros sustituyentes, como cadenas de carbono que llevan grupos hidroxilo o carboxilo. Estas estructuras de cadena pueden tener de 1 a 11 átomos de carbono de longitud, pero normalmente tienen de 2 a 5 carbonos de longitud; las propias cadenas de carbono pueden ser ramificadas o no ramificadas. [1]
Los azúcares más comunes son los monosacáridos, como la glucosa y la galactosa, aunque en la naturaleza existe una amplia variedad de azúcares. Otros tipos de moléculas, como los ácidos orgánicos, también pueden unirse a la base formando ésteres a través de sus grupos carboxilo (COOH). Entre ellos, destacan los ácidos de azúcar, como el ácido glucurónico y el ácido galacturónico, que son formas oxidadas de la glucosa y la galactosa. [1]