El alcanfor ( / ˈk æ m f ər / ) es un sólido ceroso, incoloro con un fuerte aroma. [5] Se clasifica como un terpenoide y una cetona cíclica . Se encuentra en la madera del laurel alcanforero ( Cinnamomum camphora ), un gran árbol de hoja perenne que se encuentra en el este de Asia; y en el árbol kapur ( Dryobalanops sp. ), un árbol maderable alto del sudeste de Asia. También se presenta en algunos otros árboles relacionados en la familia del laurel , en particular Ocotea usambarensis . Las hojas de romero ( Rosmarinus officinalis ) contienen entre 0,05 y 0,5% de alcanfor, [6] mientras que la alcanforera ( Heterotheca ) contiene alrededor del 5%. [7] Una fuente importante de alcanfor en Asia es la albahaca alcanforera (el progenitor de la albahaca azul africana ). El alcanfor también se puede producir sintéticamente a partir de aceite de trementina .
El compuesto es quiral y existe en dos posibles enantiómeros , como se muestra en los diagramas estructurales. La estructura de la izquierda es el (+)-alcanfor natural ((1 R ,4 R )-bornan-2-ona), mientras que su imagen especular que se muestra a la derecha es el (−)-alcanfor ((1 S ,4 S )-bornan-2-ona). El alcanfor tiene pocos usos, pero es de importancia histórica como un compuesto que se purifica fácilmente a partir de fuentes naturales.
La palabra alcanfor deriva en el siglo XIV del francés antiguo: camphre , a su vez del latín medieval : camfora , del árabe : كافور , romanizado : kāfūr , tal vez a través del sánscrito : कर्पूर , romanizado : karpūra , del tamil : கற்பூரம் , romanizado: karpooram aparentemente del malayo austronesio : kapur 'cal' (tiza). [8]
En malayo antiguo , el alcanfor se llamaba kapur barus , que significa "la tiza de Barus", en referencia a Barus, un antiguo puerto cerca de la moderna Sibolga en la costa occidental de Sumatra . [9] Este puerto comerciaba con alcanfor extraído de los árboles de alcanfor de Borneo ( Dryobalanops aromatica ) que abundaban en la región. [10]
El alcanfor se ha producido como un producto forestal durante siglos, condensado a partir del vapor emitido por el tostado de astillas de madera cortadas de Camphora officinarum , y más tarde haciendo pasar vapor a través de la madera pulverizada y condensando los vapores. [11] A principios del siglo XIX, la mayoría de las reservas de árboles de alcanfor se habían agotado y las grandes reservas restantes estaban en Japón y Taiwán , con una producción taiwanesa que excedía en gran medida a la japonesa. El alcanfor era uno de los principales recursos extraídos por las potencias coloniales de Taiwán, así como uno de los más lucrativos. Primero los chinos y luego los japoneses establecieron monopolios sobre el alcanfor taiwanés. En 1868, una fuerza naval británica navegó hacia el puerto de Anping y el representante británico local exigió el fin del monopolio chino del alcanfor. Después de que el representante imperial local se negara, los británicos bombardearon la ciudad y tomaron el puerto. Las "regulaciones del alcanfor" negociadas entre las dos partes posteriormente vieron un breve fin del monopolio del alcanfor. [12]
El alcanfor se produce a partir del alfa-pineno , que es abundante en los aceites de los árboles coníferos y se puede destilar a partir de la trementina producida como subproducto de la pulpa química . Con anhídrido acético como disolvente y con catálisis por un ácido fuerte, el alfa-pineno se convierte en acetato de isobornilo . La hidrólisis de este éster da isoborneol que se puede oxidar para dar alcanfor racémico . Por el contrario, el alcanfor se presenta de forma natural como D -alcanfor, el enantiómero ( R ) . [ cita requerida ]
Las reacciones del alcanfor se han estudiado en profundidad. Algunas transformaciones representativas incluyen:
El alcanfor también se puede reducir a isoborneol utilizando borohidruro de sodio .
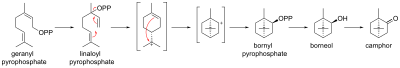
En la biosíntesis , el alcanfor se produce a partir de pirofosfato de geranilo , mediante la ciclización del pirofosfato de linaloilo a pirofosfato de bornilo , seguida de hidrólisis a borneol y oxidación a alcanfor.
Los primeros plásticos artificiales importantes fueron los plásticos de nitrocelulosa (piroxilina) con bajo contenido de nitrógeno (o "solubles") . En las primeras décadas de la industria del plástico , el alcanfor se utilizaba en inmensas cantidades [15] : 130 como plastificante que crea celuloide a partir de nitrocelulosa, en lacas de nitrocelulosa y otros plásticos y lacas.
El alcanfor se ha utilizado por su aroma, como líquido para embalsamar , como medicamento tópico , como producto químico de fabricación y en ceremonias religiosas.

El alcanfor se ha utilizado como medicina popular durante siglos, probablemente más comúnmente como descongestionante . [16] El alcanfor se usaba en la antigua Sumatra para tratar esguinces , hinchazones e inflamaciones . [17] El alcanfor también se usó durante siglos en la medicina tradicional china para diversos fines. [16] En Europa, el alcanfor se utilizó después de la era de la Peste Negra . [18]
En el siglo XX, el alcanfor se utilizó como analéptico mediante inyección, [19] y para inducir convulsiones en personas esquizofrénicas en un intento de tratar la psicosis . [20]
El alcanfor tiene un uso limitado en medicina veterinaria mediante inyección intramuscular para tratar dificultades respiratorias en caballos. [21]
El alcanfor se aplica comúnmente como un medicamento tópico en forma de crema o ungüento para la piel para aliviar la picazón causada por picaduras de insectos, irritaciones menores de la piel o dolor en las articulaciones. [22] Se absorbe en la epidermis de la piel , [22] donde estimula las terminaciones nerviosas sensibles al calor y al frío, produciendo una sensación de calor cuando se aplica vigorosamente, o una sensación de frescor cuando se aplica suavemente, lo que indica sus propiedades como contrairritante . [16] La acción sobre las terminaciones nerviosas también induce una ligera analgesia local . [23]
El alcanfor también se utiliza en forma de aerosol , generalmente por inhalación de vapor, a veces en forma de inhaladores nasales de marca, para inhibir la tos y aliviar la congestión de las vías respiratorias superiores debido al resfriado común. [24] Sin embargo, la eficacia clínica de estos remedios está en tela de juicio. [25]
Los tiradores utilizan el alcanfor para ennegrecer las miras delantera y trasera de los rifles y evitar que se reflejen. [26] Esto se hace encendiendo una pequeña cantidad de alcanfor, que arde a una temperatura relativamente baja, y utilizando el hollín que se eleva de la llama para depositar una capa sobre una superficie colocada encima de ella. Históricamente, este ennegrecimiento con hollín también se utilizaba para recubrir los gráficos de registro barográfico .
Se cree que el alcanfor es tóxico para los insectos y, por lo tanto, a veces se utiliza como repelente. [27] El alcanfor se utiliza como una alternativa a las bolas de naftalina . Los cristales de alcanfor a veces se utilizan para evitar que otros insectos pequeños dañen las colecciones de insectos . Se guarda en la ropa que se usa en ocasiones especiales y festivales, y también en las esquinas de los armarios como repelente de cucarachas. El humo del cristal de alcanfor o de las varillas de incienso de alcanfor se puede utilizar como un repelente de mosquitos ecológico. [28]
Estudios recientes han indicado que el aceite esencial de alcanfor se puede utilizar como un fumigante eficaz contra las hormigas rojas de fuego , ya que afecta el comportamiento de ataque, trepa y alimentación de las obreras mayores y menores. [29]
El alcanfor también se utiliza como sustancia antimicrobiana . En el embalsamamiento , el aceite de alcanfor era uno de los ingredientes utilizados por los antiguos egipcios para la momificación . [30]
El alcanfor sólido libera vapores que forman una capa antioxidante y, por lo tanto, se almacena en cajas de herramientas para protegerlas contra el óxido. [31]
En el antiguo mundo árabe, el alcanfor era un ingrediente común en los perfumes. [32] Los chinos se referían al mejor alcanfor como "perfume de cerebro de dragón", debido a su "aroma penetrante y portentoso" y a "siglos de incertidumbre sobre su procedencia y modo de origen". [33]
Una de las primeras recetas conocidas de helado que data de la dinastía Tang incluye alcanfor como ingrediente. [34] Se utilizaba para dar sabor al pan leudado en el antiguo Egipto. [35] En la Europa antigua y medieval, el alcanfor se utilizaba como ingrediente en dulces . Se utilizaba en una amplia variedad de platos salados y dulces en los libros de cocina medievales en lengua árabe, como al-Kitab al-Ṭabikh compilado por ibn Sayyār al-Warrāq en el siglo X. [36] También se utilizaba en platos dulces y salados en el Ni'matnama , según un libro escrito a finales del siglo XV para los sultanes de Mandu . [37] Es un componente principal de una especia conocida como "alcanfor comestible" (o kapur ), que puede utilizarse en postres tradicionales del sur de la India como Payasam y Chakkarai Pongal . [38]
El alcanfor se utiliza ampliamente en las ceremonias religiosas hindúes. El aarti se realiza después de colocarlo en un soporte y prenderle fuego, generalmente como el último paso de la puja o ritual de adoración devocional a una o más deidades. [39] El alcanfor se menciona en el Corán como la fragancia del vino que se les da a los creyentes en el cielo. [40]
Aplicado sobre la piel, el alcanfor puede causar reacciones alérgicas en algunas personas; cuando se ingiere por vía oral, la crema o ungüento de alcanfor es venenoso. [22] En dosis altas ingeridas, el alcanfor produce síntomas de irritabilidad, desorientación, letargo, espasmos musculares , vómitos, calambres abdominales, convulsiones y ataques epilépticos . [41] Las dosis letales por ingestión en adultos están en el rango de 50 a 500 mg/kg (por vía oral). Generalmente, la ingestión de dos gramos causa toxicidad grave y cuatro gramos son potencialmente letales. [42]
El alcanfor en suspensión en el aire puede ser tóxico si es inhalado por humanos. El límite de exposición permisible ( PEL ) para el alcanfor en el aire ambiente es de 2 mg/m3 con un tiempo de exposición ( TWA ) no superior a 8 horas. 200 mg/m3 se considera una concentración muy peligrosa ( IDLH ). [43]
Cuando su uso en las nacientes industrias químicas (que se analizan más adelante) aumentó considerablemente el volumen de la demanda a finales del siglo XIX, se produjo un potencial de cambios en la oferta y en el precio . En 1911, Robert Kennedy Duncan, químico industrial y educador, relató que el gobierno imperial japonés había intentado recientemente (1907-1908) monopolizar la producción de alcanfor natural como producto forestal en Asia, pero que el monopolio se vio impedido por el desarrollo de las alternativas de síntesis total , [15] que comenzaron en forma "puramente académica y totalmente no comercial" [15] con el primer informe de Gustav Komppa:
" ... pero selló el destino del monopolio japonés ... Porque tan pronto como se llevó a cabo, atrajo la atención de un nuevo ejército de investigadores: los químicos industriales. Las oficinas de patentes del mundo pronto se llenaron de supuestas síntesis comerciales de alcanfor, y de los procesos favorecidos se formaron compañías para explotarlas, surgieron fábricas, y en el increíblemente corto tiempo de dos años después de su síntesis académica, el alcanfor artificial, tan bueno como el producto natural, entró en los mercados del mundo ... Y sin embargo, el alcanfor artificial no desplaza -y no puede- al producto natural en una medida suficiente para arruinar la industria del cultivo del alcanfor. Su única función presente y probablemente futura es actuar como un freno permanente a la monopolización, actuar como un volante para regular los precios dentro de límites razonables". [15] : 133–134
Este control permanente del crecimiento de los precios se confirmó en 1942 en una monografía sobre la historia de DuPont , donde William S. Dutton dijo: "Indispensable en la fabricación de plásticos de piroxilina, el alcanfor natural importado de Formosa y que se vendía normalmente a unos 50 centavos la libra, alcanzó el alto precio de 3,75 dólares en 1918 [en medio de la interrupción del comercio mundial y la demanda de explosivos de gran potencia que creó la Primera Guerra Mundial]. Los químicos orgánicos de DuPont respondieron sintetizando alcanfor a partir de la trementina de los tocones de pino del sur de Estados Unidos, con el resultado de que el precio del alcanfor industrial vendido en lotes de carga en 1939 estaba entre 32 y 35 centavos la libra". [44] : 293
Los antecedentes de la síntesis de Gustaf Komppa fueron los siguientes. En el siglo XIX, se sabía que el ácido nítrico oxida al alcanfor en ácido alcanfórico . Haller y Blanc publicaron una semisíntesis de alcanfor a partir de ácido alcanfórico. Aunque demostraron su estructura, no pudieron probarla. La primera síntesis total completa de ácido alcanfórico fue publicada por Komppa en 1903. Sus insumos fueron oxalato de dietilo y ácido 3,3-dimetilpentanoico, que reaccionaron por condensación de Claisen para producir ácido dicetocanfórico. La metilación con yoduro de metilo y un procedimiento de reducción complicado produjeron ácido alcanfórico. William Perkin publicó otra síntesis poco tiempo después. Anteriormente, algunos compuestos orgánicos (como la urea ) se habían sintetizado en el laboratorio como prueba de concepto , pero el alcanfor era un producto natural escaso con demanda mundial. Komppa se dio cuenta de esto y comenzó la producción industrial de alcanfor en Tainionkoski , Finlandia, en 1907 (con mucha competencia, como informó Kennedy Duncan). [ cita requerida ]
Al mismo tiempo, el Dr. Karl Stephan de Chemische Fabrik auf Actien desarrolló un método de síntesis diferente . Este químico, que había patentado una ruta para sintetizar canfeno en 1902, descubrió que el borneol o isoborneol se podía oxidar fácilmente con permanganato en solución de benceno con rendimientos sin precedentes de más del 95%, y lo patentó en 1903. [45] El proceso era lo suficientemente eficiente como para competir con el alcanfor natural, y Japón se vio obligado a bajar los precios en 1907, pero la compañía alemana aún aumentó su producción, alcanzando las 623 toneladas en 1913, solo para ser interrumpida por la Primera Guerra Mundial. [46]