
La malla quirúrgica es un implante médico hecho de malla tejida de forma suelta , que se utiliza en cirugía como soporte estructural permanente o temporal para órganos y otros tejidos . La malla quirúrgica puede estar hecha de materiales inorgánicos y biológicos y se utiliza en una variedad de cirugías, aunque la reparación de hernias es la aplicación más común. También se puede utilizar para trabajos reconstructivos , como en el prolapso de órganos pélvicos [1] o para reparar defectos físicos (principalmente de las paredes de la cavidad corporal ) creados por resecciones extensas o pérdida de tejido traumático .
Las mallas permanentes permanecen en el cuerpo, mientras que las temporales se disuelven con el tiempo. En 2012, se demostró que una malla temporal se disolvía por completo después de tres años en un ensayo científico con ovejas. [2] Algunos tipos de mallas combinan mallas permanentes y temporales que incluyen tanto vicryl reabsorbible , hecho de ácido poliglicólico , como prolene , un polipropileno no reabsorbible. [3]
Los datos de los comportamientos mecánicos y biológicos de las mallas in vivo pueden no reflejar siempre las condiciones dentro del cuerpo humano debido a las pruebas en organismos no humanos . La mayoría de los informes publicados experimentan con ratones, lo que crea la posibilidad de posibles diferencias cuando se insertan en el cuerpo humano. Además, la mayoría de los informes de investigación publicados hacen referencia a mallas que actualmente no están permitidas en el mercado de dispositivos médicos debido a complicaciones posteriores a la cirugía. Además, la ausencia de protocolos regulatorios aprobados por la FDA y procedimientos operativos estándar universales conduce a una variedad de métodos de prueba diferentes de un investigador a otro. La experimentación puede encontrar diferentes resultados para algunas mallas. [ cita requerida ] [ investigación original? ]
La función principal de la malla quirúrgica es dar soporte a los órganos prolapsados, ya sea de manera temporal o permanente. Se utiliza con mayor frecuencia en la cirugía de hernia dentro del abdomen, que es necesaria cuando un órgano sobresale a través de los músculos abdominales. La malla quirúrgica también se puede utilizar para reconstrucciones de la pared pélvica o vaginal en mujeres y se implementa para agregar una guía de crecimiento para el tejido dañado. Idealmente, estos implantes deben ser lo suficientemente fuertes como para sobrevivir a las cargas mecánicas y las acciones de la zona del cuerpo de la que formen parte.
La cirugía de hernia es una de las aplicaciones actuales más comunes de la malla quirúrgica. Las hernias se producen cuando los órganos o el tejido graso sobresalen a través de aberturas o áreas debilitadas del músculo, generalmente en la pared abdominal. La malla quirúrgica se implanta para fortalecer la reparación del tejido y minimizar la tasa de recurrencia. La cirugía se puede realizar por vía laparoscópica (interna) o abierta con una variedad de materiales disponibles para prótesis. [4] El polipropileno (PP) es el tipo de malla más utilizado, aunque puede resultar incómodo para el paciente después de la implantación. Otro tipo que se utiliza menos en la cirugía de hernia es el tereftalato de polietileno (PET), que enfrenta complicaciones porque se degrada fácilmente después de algunos años de la implantación, borrando los efectos de la cirugía. El politetrafluoroetileno ( PTFE ) también se utiliza, pero se fabrica en forma de lámina y tiene dificultad para integrarse en el tejido circundante, por lo que pierde estabilidad. [5]
De manera similar a la cirugía de hernia, también se pueden utilizar mallas sintéticas para prolapsos de órganos en la región pélvica. El prolapso de órganos pélvicos ocurre en el 50% de las mujeres mayores de 50 años con antecedentes de uno o más partos vaginales a lo largo de su vida. [6] La cirugía de malla se puede realizar en varias áreas de la región pélvica, como cistocele, rectocele y cúpula vaginal o útero. El material más comúnmente utilizado, al igual que en la cirugía de hernia, es el PP, que se considera que tiene una biocompatibilidad aceptable dentro de la región. Induce una respuesta inflamatoria leve pero tiene una tendencia a adherirse a las vísceras. [6]
La pared vaginal tiene tres capas: túnica mucosa, muscular y adventicia. Cuando se produce prolapso, las fibras lisas de la muscular se ven comprometidas. También se ha observado que el prolapso en mujeres aumenta la rigidez de la pelvis, en particular en mujeres posmenopáusicas. [6] La malla quirúrgica que se utiliza en la reconstrucción pélvica debe contrarrestar esta rigidez, pero si el módulo de elasticidad es demasiado alto, no soportará lo suficiente los órganos. Por el contrario, si la malla es demasiado rígida, el tejido se erosionará y las respuestas inflamatorias causarán complicaciones posquirúrgicas. Después de la implantación, la malla de polipropileno a veces presenta microfisuras, descamación de las fibras y fibrosis. [7]
Además, la malla tiene suficiente resistencia para soportar acciones básicas y el comportamiento del tejido en condiciones fisiológicas, particularmente durante la regeneración del tejido a través de la propia malla. [6] La zona está sujeta a una variedad de cargas que provienen del contenido abdominal, la presión de los músculos abdominales/diafragmáticos y los órganos genitales, así como las acciones respiratorias. Para la mujer promedio en edad reproductiva, la pelvis debe soportar cargas de 20 N en posición supina, 25-35 N en posición de pie y 90-130 N al toser. [6] Cualquier malla que se implante en el área pélvica debe ser lo suficientemente fuerte para soportar estas cargas.
En 2018, el Reino Unido suspendió temporalmente los implantes de malla vaginal para el tratamiento de la incontinencia urinaria en espera de más investigaciones sobre los riesgos y las salvaguardas disponibles. [8]
En los Estados Unidos, la FDA reclasificó la malla quirúrgica transvaginal como "clase III" (alto riesgo) en 2016, [9] y a fines de 2018, ordenó solicitudes de aprobación previa a la marca para mallas destinadas a la reparación transvaginal del prolapso de órganos pélvicos, con una investigación más a fondo planeada en 2019. [10] Luego, el 16 de abril de 2019, la FDA ordenó a todos los fabricantes de mallas quirúrgicas transvaginales que detuvieran inmediatamente su venta y distribución. [9]

La implantación de la malla generará naturalmente una respuesta inflamatoria a la malla insertada, pero la biocompatibilidad varía desde la facilidad con la que se integra hasta la gravedad de la reacción al cuerpo extraño. Una respuesta mínima incluye la formación de fibrosis alrededor de la prótesis (muy similar a la formación de tejido cicatricial); esta respuesta se genera con la mejor forma de biocompatibilidad. Una respuesta física desencadena una reacción inflamatoria aguda, que implica la formación de células gigantes y, posteriormente, granulomas, lo que significa que el tejido está "tolerando" la malla bastante bien. Por último, una respuesta química permite una reacción inflamatoria grave durante el intento de integración del tejido con la malla, incluida la proliferación de células fibroblásticas. [6] En última instancia, el objetivo de la creación de una malla quirúrgica es formular una que tenga una reacción mínima in vivo para maximizar la comodidad del paciente, evitar infecciones y garantizar una integración limpia en el cuerpo para la reparación del tejido.
En la biocompatibilidad de la malla influyen varios factores. La porosidad de la malla es la relación entre el área de poro y el área total, y desempeña un papel en el desarrollo de una infección bacteriana o en la regeneración de tejido liso, dependiendo del tamaño de poro. Los tamaños de poro inferiores a 10 micrómetros son susceptibles a infecciones porque las bacterias pueden entrar y proliferar, mientras que los macrófagos y los neutrófilos son demasiado grandes para pasar a través de ellos y no pueden ayudar a su eliminación. Con tamaños de poro superiores a 75 micrómetros, se permite el paso de fibroblastos, vasos sanguíneos y fibras de colágeno como parte de la regeneración tisular. Aunque no existe un consenso general sobre el mejor tamaño de poro, se puede deducir que los poros más grandes son mejores para el desarrollo del tejido y la integración in vivo . [6]
Sabiendo esto, el problema actual con una variedad de mallas utilizadas en todo tipo de cirugías es que no son lo suficientemente biocompatibles. El PP demuestra ser una malla eficaz para ajustar órganos prolapsados, pero puede causar una gran incomodidad para el paciente debido a su alto módulo de elasticidad. Esto endurece la prótesis y da como resultado una respuesta inflamatoria más pronunciada, lo que complica la integración en el cuerpo con el crecimiento del tejido. Como se mencionó anteriormente, el PET se degrada demasiado fácilmente in vivo y el tejido tiene dificultades para integrarse con el PTFE. Por estas razones, los investigadores están comenzando a buscar diferentes tipos de mallas quirúrgicas que puedan ser adecuadas para el entorno biológico y brindar una mejor comodidad al mismo tiempo que sostienen los órganos prolapsados. [5]
Un tipo particular de malla que se está estudiando es el fluoruro de polivinilideno (PVDF), o malla nanofibrosa, que se ha descubierto que es más resistente a la hidrólisis y la desintegración, a diferencia del PET, y no aumenta su rigidez con el tiempo, a diferencia del PP. Se está probando tanto para la hernia como para la cirugía de la pared pélvica/vaginal y se produce mediante la colocación de fibras capa por capa, mientras que el PP se construye mediante un proceso similar al tejido. Esto le da a la malla nanofibrosa una estructura pesada pero de baja porosidad, y también agrega mayor rigidez y umbral de estrés en comparación con el PP. Esto está respaldado por la presencia de HSP70, un indicador de estrés celular y protector de la formación celular contra daños, que es beneficioso para la prótesis y la formación de tejido, que se ha monitoreado y observado en una mayor presencia en implantes de PVDF. [11] Las observaciones in vitro de la malla nanofibrosa han arrojado evidencia de migración y proliferación celular en el conjunto [ aclaración necesaria ] de la malla. Se ha observado un crecimiento celular exitoso con formas fusiformes largas y límites claros. [11]
Una ventaja importante de utilizar una malla nanofibrosa es que puede transportar muchas más células madre que la malla PP tradicional, lo que podría mejorar la terapia basada en células para el prolapso de órganos pélvicos y los métodos de regeneración. Otra ventaja importante del PVDF es la formación de capilares después de 12 semanas, lo que es esencial para la cicatrización de heridas . Cuanto más rápido se produce la neovascularización, más rápido se puede reparar y regenerar el tejido, lo que disminuye la probabilidad de exposición o extrusión de la malla. [11]
También es necesario realizar algunas mejoras en el PVDF antes de que pueda utilizarse en cirugía humana. Aunque el módulo de elasticidad es mayor que el del PP, el estiramiento resultante bajo una tensión idéntica es mucho menor, lo que podría causar complicaciones como la degeneración tisular y la pérdida de solidez mecánica. Actualmente, la malla nanofibrosa también promueve una mayor reacción a cuerpos extraños y una respuesta inflamatoria, lo que compromete la biocompatibilidad de la malla. [11] Por estas razones, el PVDF todavía se encuentra bajo consideración y experimentación para implantes corporales.
Las respuestas inflamatorias a la inserción de la malla promueven la formación de tejido alrededor de las fibras de la malla y la proliferación de fibroblastos, polimorfonucleocitos y macrófagos, que ayudan a la integración de la malla. Si no se resuelven las respuestas inflamatorias, pueden producirse reacciones a cuerpos extraños y la encapsulación final del implante, lo que anula cualquier propósito funcional que se suponía que debía cumplir el implante. Se sabe que las células madre mesenquimales (MSC) reducen las respuestas inflamatorias que, cuando se combinan con la malla quirúrgica, podrían evitar que se vuelvan incontrolables y demasiado difíciles de controlar. Las MSC combinadas con mallas quirúrgicas se pueden utilizar como productos "listos para usar" y mejoran la polarización de los macrófagos tanto en entornos in vivo como in vitro. Esto puede estimular una respuesta antiinflamatoria y puede regular la reacción inflamatoria asociada con la implantación de la malla. [12]
Además de la erosión de la malla, la migración de la malla y la fístula enterocutánea, las infecciones del sitio quirúrgico relacionadas con la malla siguen siendo un problema de salud importante. [13] Aproximadamente 60 000 reparaciones de hernia inguinal y ventral se infectan anualmente, con números similares en Europa. [13] Los CDC distinguen entre las infecciones del sitio quirúrgico superficiales, que afectan solo la piel y el tejido subcutáneo, y las infecciones del sitio quirúrgico profundas, cuando la infección puede asentarse en el implante y, por lo tanto, requieren protocolos de tratamiento más elaborados. [14]
La patogenia de las contaminaciones relacionadas con las mallas se debe principalmente a la piel o las mucosas del paciente durante la incisión primaria y las prácticas clínicas. Se ha descubierto que la inserción de dispositivos médicos aumenta la susceptibilidad a la absorción de bacterias adherentes en un factor de 10 000 a 100 000. [15] En el caso de las operaciones de hernia, entre un tercio y dos tercios de la malla implantada se contaminaría en el punto de inserción, aunque solo una pequeña cantidad de ellos causará una infección. Muchos factores afectan las posibilidades de que se produzca una infección en un material de malla, entre los que el tipo de procedimiento quirúrgico y la ubicación son los de mayor importancia. [16] Por ejemplo, las posibilidades de que se produzca una infección son del 2 % al 4 % para una reparación inguinal abierta, pero tan altas como el 10 % para la reparación de hernia incisional. [17] La laparoscopia tiene la tasa de infección más baja, que generalmente oscila por debajo del 1 % y tan solo el 0,1 %. [17] Otros factores que afectan las posibilidades de una infección son la curva de aprendizaje del cirujano, ya que un cirujano menos experimentado puede necesitar más tiempo para realizar la operación y, por lo tanto, aumentar el tiempo en que la incisión está expuesta. Además, el tipo de malla, con una amplia variedad de prótesis disponibles en la actualidad, podría distinguirse en función del material y la composición, la arquitectura del filamento, la capacidad de absorción y el peso. La demografía del paciente también influye en las posibilidades de que se produzca una infección; entre ellos, el tabaquismo, la diabetes, el sistema inmunitario comprometido y la obesidad.
Los factores predictivos de infecciones del sitio quirúrgico de aparición temprana y tardía son la inflamación, la fiebre, el dolor focal, el eritema, la hinchazón con secreción de pus, el enrojecimiento, el calor o el dolor. [18] Esto se evaluará mediante una TC o una RMN, seguida de la aspiración de líquido y el cultivo. Las especies de estafilococos, y más específicamente S. aureus y S. epidermidis, representan aproximadamente el 90 % de las infecciones que se producen, con una presencia predominante de Staphylococcus aureus resistente a la meticilina (MRSA). [19] También se encuentran comúnmente especies gramnegativas como Pseudomonas sp. y Enterobacteriaceae . También es común encontrar biopelículas de múltiples especies. Si una infección se asienta en una malla, la administración de antibióticos suele ser ineficaz, debido a la barrera entre la sangre y la malla, y será necesario retirar la malla en más del 40 % de las infecciones profundas del sitio quirúrgico. [20]
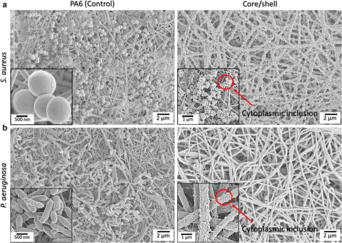
Desde una perspectiva de la ciencia de los materiales, una malla puede desempeñar un papel pasivo en la protección antibacteriana a través de su arquitectura, o un papel activo mediante la combinación de agentes terapéuticos en la composición de la malla. Por ejemplo, se ha descubierto que las mallas monofilamento tienen el doble de probabilidades de adherir bacterias que las mallas multifilamento. [22] Como sistema de administración de fármacos, una malla para hernias se puede utilizar para administrar antibióticos, [23] antisépticos, [24] antimicrobianos, [21] péptidos antimicrobianos [25] o nanopartículas. [26] Se pueden utilizar diferentes técnicas para implementar la integración de dichas sustancias, incluidas la inmersión/remojo, el recubrimiento físico, la funcionalización química de la superficie y el electrohilado.
Mallas antimicrobianas para hernias aprobadas por la FDA
Después de 36 meses, la malla de prueba se reabsorbió por completo.