El paro cardíaco , también conocido como paro cardíaco repentino ( PCS ), [11] es cuando el corazón deja de latir de manera repentina e inesperada. [12] [1] Cuando el corazón deja de latir, la sangre no puede circular adecuadamente por el cuerpo y el flujo sanguíneo al cerebro y otros órganos disminuye. Cuando el cerebro no recibe suficiente sangre, esto puede hacer que una persona pierda el conocimiento y las células cerebrales puedan comenzar a morir debido a la falta de oxígeno. [13] El coma y el estado vegetativo persistente pueden ser resultado de un paro cardíaco. El paro cardíaco también se identifica por la falta de pulsos centrales y la respiración anormal o ausente . [1]
El paro cardíaco y el colapso hemodinámico resultante suelen ocurrir debido a arritmias (ritmos cardíacos irregulares). La fibrilación ventricular y la taquicardia ventricular son las más comúnmente registradas. [14] Sin embargo, como muchos incidentes de paro cardíaco ocurren fuera del hospital o cuando una persona no tiene su actividad cardíaca monitoreada, es difícil identificar el mecanismo específico en cada caso.
La cardiopatía estructural , como la enfermedad de la arteria coronaria , es una afección subyacente común en las personas que sufren un paro cardíaco. Los factores de riesgo más comunes incluyen la edad y la enfermedad cardiovascular. [15] Otras afecciones cardíacas subyacentes incluyen la insuficiencia cardíaca y las arritmias hereditarias . Otros factores que pueden contribuir al paro cardíaco incluyen la pérdida importante de sangre , la falta de oxígeno , la alteración de los electrolitos (como un nivel muy bajo de potasio ), las lesiones eléctricas y el ejercicio físico intenso . [16]
El paro cardíaco se diagnostica por la incapacidad de encontrar el pulso en un paciente que no responde. [4] [1] El objetivo del tratamiento del paro cardíaco es lograr rápidamente el retorno de la circulación espontánea mediante una variedad de intervenciones que incluyen RCP , desfibrilación y/o marcapasos cardíaco. Se han establecido dos protocolos para la RCP: soporte vital básico (SVB) y soporte vital cardíaco avanzado (SVA). [17]
Si se logra el retorno de la circulación espontánea con estas intervenciones, se ha producido un paro cardíaco súbito. Por el contrario, si la persona no sobrevive al evento, se habla de muerte súbita cardíaca. Entre aquellos cuyos pulsos se restablecen, el equipo de atención puede iniciar medidas para proteger a la persona de una lesión cerebral y preservar la función neurológica. [18] Algunos métodos pueden incluir el manejo de las vías respiratorias y la ventilación mecánica, el mantenimiento de la presión arterial y la perfusión de los órganos terminales mediante reanimación con líquidos y apoyo vasopresor, la corrección del desequilibrio electrolítico, la monitorización del ECG y el manejo de las causas reversibles, y el control de la temperatura. El control de la temperatura dirigido puede mejorar los resultados. [19] [20] En los cuidados posteriores a la reanimación, se puede considerar un desfibrilador cardíaco implantable para reducir la probabilidad de muerte por recurrencia. [5]
Según las pautas de la Asociación Estadounidense del Corazón de 2015, en los Estados Unidos se produjeron aproximadamente 535 000 casos de paro cardíaco al año (alrededor de 13 por cada 10 000 personas). [9] De estos, 326 000 (61 %) sufren un paro cardíaco fuera del ámbito hospitalario, mientras que 209 000 (39 %) ocurren dentro de un hospital. [9]
El paro cardíaco se vuelve más común con la edad y afecta a los hombres con más frecuencia que a las mujeres. [3] Las personas de raza negra tienen el doble de probabilidades de morir de paro cardíaco que las personas blancas. Las personas asiáticas e hispanas no se ven afectadas con tanta frecuencia como las personas blancas. [3]
En aproximadamente el 50 por ciento de las personas, el paro cardíaco no se ve precedido por ningún síntoma de advertencia. [21] En el caso de las personas que presentan síntomas, estos suelen ser inespecíficos del paro cardíaco. [22] Por ejemplo, dolor de pecho nuevo o que empeora , fatiga , desmayos , mareos , dificultad para respirar , debilidad o vómitos . [22] [12]
Cuando una persona común sospecha que se ha producido un paro cardíaco (debido a signos de inconsciencia, respiración anormal o ausencia de pulso), se debe suponer que la víctima ha sufrido un paro cardíaco. Las personas que se encuentren en el lugar deben llamar a los servicios médicos de emergencia (como el 911 o el 112) e iniciar la reanimación cardiopulmonar (RCP) .
Los principales factores de riesgo de paro cardíaco incluyen la edad y la enfermedad cardiovascular subyacente . Un episodio previo de paro cardíaco repentino aumenta la probabilidad de futuros episodios. [23] Un metanálisis de 2021 que evaluó la recurrencia del paro cardíaco en sobrevivientes de un paro cardíaco extrahospitalario identificó que el 15% de los sobrevivientes experimentaron un segundo evento, con mayor frecuencia en el primer año. [24] Además, de los que experimentaron recurrencia, el 35% tuvo un tercer episodio. [24]
Otros factores de riesgo significativos incluyen el tabaquismo , la hipertensión arterial , el colesterol alto , los antecedentes de arritmia , la falta de ejercicio físico , la obesidad , la diabetes , los antecedentes familiares , la miocardiopatía , el consumo de alcohol y, posiblemente, la ingesta de cafeína. [25] [26] [27] [28] Se encontró que los fumadores actuales de cigarrillos con enfermedad de la arteria coronaria tenían un aumento de dos a tres veces en el riesgo de muerte súbita entre los 30 y los 59 años. Además, se encontró que el riesgo de los ex fumadores era más cercano al de los que nunca habían fumado. [21] [15] Un análisis estadístico de muchos de estos factores de riesgo determinó que aproximadamente el 50% de todos los paros cardíacos ocurren en el 10% de la población percibida como de mayor riesgo, debido al daño agregado de múltiples factores de riesgo, lo que demuestra que el riesgo acumulativo de múltiples comorbilidades excede la suma de cada riesgo individualmente. [29]
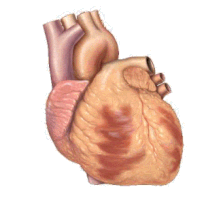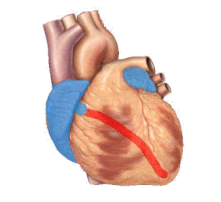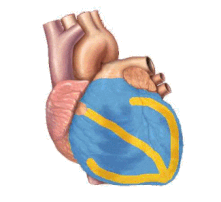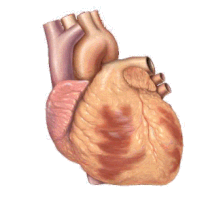
Las causas subyacentes del paro cardíaco repentino pueden ser de origen cardíaco y no cardíaco. Las causas subyacentes más comunes son diferentes, según la edad del paciente. Las causas cardíacas comunes incluyen enfermedad de la arteria coronaria , anomalías no ateroscleróticas de la arteria coronaria, daño cardíaco estructural y arritmias hereditarias. Las causas no cardíacas comunes incluyen paro respiratorio, diabetes, medicamentos y traumatismos.
El mecanismo más común subyacente al paro cardíaco repentino es una arritmia (un ritmo irregular). [30] Sin una actividad eléctrica organizada en el músculo cardíaco , hay una contracción inconsistente de los ventrículos , lo que impide que el corazón genere un gasto cardíaco adecuado (bombeo hacia adelante de sangre desde el corazón al resto del cuerpo). [31] Este colapso hemodinámico da como resultado un flujo sanguíneo deficiente al cerebro y otros órganos, que si se prolonga causa daño persistente.
Existen muchos tipos diferentes de arritmias, pero las que se registran con mayor frecuencia en el paro cardíaco repentino son la taquicardia ventricular y la fibrilación ventricular . [32] [33] Tanto la taquicardia ventricular como la fibrilación ventricular pueden impedir que el corazón genere contracciones ventriculares coordinadas, lo que impide mantener una circulación sanguínea adecuada.
Los tipos menos comunes de arritmias que ocurren en un paro cardíaco incluyen actividad eléctrica sin pulso , bradicardia y asistolia . [30] Estos ritmos se observan cuando hay un paro cardíaco prolongado, progresión de la fibrilación ventricular o esfuerzos como la desfibrilación ejecutados para resucitar a la persona. [30]
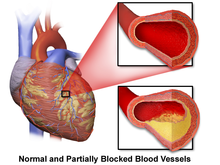
La enfermedad de las arterias coronarias (EAC), también conocida como enfermedad cardiovascular aterosclerótica, implica la deposición de colesterol y la posterior formación de placas ateroscleróticas en las arterias, impulsada por la inflamación. La EAC implica la acumulación y remodelación de los vasos coronarios junto con otros vasos sanguíneos sistémicos. [34] Cuando una placa aterosclerótica se desprende, puede bloquear el flujo de sangre y oxígeno a través de arterias pequeñas, como las arterias coronarias, lo que resulta en una lesión isquémica . En el corazón, esto da como resultado un daño en el tejido miocárdico que puede provocar cambios estructurales y funcionales que alteran los patrones normales de conducción y alteran la frecuencia y la contracción cardíacas. [29]
La CAD es la causa del 68 por ciento de las muertes cardíacas súbitas en los Estados Unidos. [35] De hecho, los exámenes post mortem han demostrado que el hallazgo más común en los casos de muerte cardíaca súbita es la estenosis crónica de alto grado de al menos un segmento de una arteria coronaria principal . [36]
Si bien la CAD es un factor contribuyente importante, se trata de un factor dependiente de la edad, siendo la CAD una causa menos común de muerte cardíaca súbita en personas menores de 40 años. [37]
Las anomalías de las arterias coronarias no relacionadas con la aterosclerosis incluyen inflamación (conocida como arteritis coronaria ), embolia , vasoespasmo , anomalías mecánicas relacionadas con enfermedades del tejido conectivo o traumatismos y anomalías congénitas de la arteria coronaria (más comúnmente origen anómalo de la arteria coronaria izquierda desde la arteria pulmonar). Estas afecciones representan el 10-15% de los paros cardíacos y la muerte cardíaca súbita. [29]

Los ejemplos de enfermedades cardíacas estructurales incluyen: miocardiopatías ( hipertróficas , dilatadas o arritmogénicas ), alteraciones del ritmo cardíaco , miocarditis e insuficiencia cardíaca congestiva . [38]

La hipertrofia ventricular izquierda es una de las principales causas de muerte cardíaca súbita en la población adulta. [39] [30] Esto es más comúnmente el resultado de una presión arterial alta de larga duración , o hipertensión, que ha llevado a un crecimiento excesivo desadaptativo del tejido muscular del ventrículo izquierdo , la principal cámara de bombeo del corazón. [40] Esto se debe a que la presión arterial elevada en el transcurso de varios años requiere que el corazón se adapte al requisito de bombear más fuerte para que circule adecuadamente la sangre por todo el cuerpo. Si el corazón hace esto durante un período prolongado de tiempo, el ventrículo izquierdo puede experimentar hipertrofia (crecer más grande) de una manera que disminuye la efectividad del corazón. [41] La hipertrofia ventricular izquierda se puede demostrar en un ecocardiograma y un electrocardiograma (ECG). [40]
Las anomalías del sistema de conducción cardíaca (en particular, el nódulo auriculoventricular y el sistema His-Purkinje ) pueden predisponer a una persona a sufrir arritmias con riesgo de progresar a un paro cardíaco repentino, aunque este riesgo sigue siendo bajo. Muchos de estos bloqueos de la conducción pueden tratarse con desfibriladores cardíacos internos en aquellas personas que se determine que tienen un riesgo alto debido a la gravedad de la fibrosis o a trastornos electrofisiológicos graves. [29]
Las enfermedades cardíacas estructurales no relacionadas con la enfermedad de la arteria coronaria representan el 10% de todas las muertes cardíacas súbitas. [31] [35] Una revisión de 1999 de las muertes cardíacas súbitas en los Estados Unidos encontró que las enfermedades cardíacas estructurales representaban más del 30% de los paros cardíacos repentinos en personas menores de 30 años. [37] [35]
Las arritmias no debidas a cardiopatía estructural representan entre el 5 y el 10% de los paros cardíacos repentinos. [42] [43] [44] Con frecuencia, estas son causadas por trastornos genéticos . [30] Las mutaciones genéticas a menudo afectan a proteínas especializadas conocidas como canales iónicos que conducen partículas cargadas eléctricamente a través de la membrana celular , y por lo tanto, este grupo de afecciones a menudo se denomina canalopatías . Los ejemplos de estos síndromes de arritmia hereditaria incluyen el síndrome de QT largo (LQTS), el síndrome de Brugada , la taquicardia ventricular polimórfica catecolaminérgica y el síndrome de QT corto . Muchos también están asociados con desencadenantes ambientales o neurogénicos, como la respuesta a sonidos fuertes que pueden iniciar arritmias letales. [29]
El síndrome de QT largo, una afección que se menciona a menudo en las muertes de personas jóvenes, se presenta en uno de cada 5000 a 7000 recién nacidos y se estima que es responsable de 3000 muertes al año en comparación con los aproximadamente 300 000 paros cardíacos que atienden los servicios de emergencia. [45] Estas afecciones son una fracción de las muertes generales relacionadas con paros cardíacos, pero representan afecciones que pueden detectarse antes del paro y pueden ser tratables. La expresión sintomática del síndrome de QT largo es bastante amplia y se presenta con mayor frecuencia con síncope en lugar de paro cardíaco. El riesgo de paro cardíaco aún está presente, y las personas con antecedentes familiares de paros cardíacos repentinos deben someterse a pruebas de detección de síndrome de QT largo y otras causas tratables de arritmia letal. Los niveles más altos de riesgo de paro cardíaco se asocian con el sexo femenino, una prolongación más significativa del intervalo QT, antecedentes de síncope inexplicable (desmayos) o muerte cardíaca súbita prematura. [29] Además, las personas con síndrome de QT largo deben evitar ciertos medicamentos que conllevan el riesgo de aumentar la gravedad de esta anomalía de la conducción, como ciertos antiarrítmicos, antidepresivos y antibióticos quinolónicos o macrólidos . [46]
Otra condición que promueve las arritmias es el síndrome de Wolff-Parkinson-White , en el que existe una vía de conducción accesoria que evita el nódulo auriculoventricular y puede causar patrones de conducción anormales que conducen a taquicardia supraventricular y paro cardíaco. [31]
Las causas no cardíacas representan entre el 15 y el 25 % de los paros cardíacos. [44] [47] Las causas no cardíacas comunes incluyen el paro respiratorio , la diabetes , ciertos medicamentos y el traumatismo cerrado (especialmente en el pecho). [3] [48] [49]
Otras causas no cardíacas incluyen hemorragia , ruptura aórtica , shock hipovolémico , embolia pulmonar , envenenamiento como el causado por las picaduras de ciertas medusas y lesiones eléctricas . [30] [52] [53] [54]
Los patrones circadianos también se reconocen como factores desencadenantes del paro cardíaco. [55] Según una revisión sistemática de 2021, a lo largo del día hay dos momentos pico principales en los que se produce un paro cardíaco. El primero es en las horas de la mañana y el segundo es en la tarde. [56] Además, las tasas de supervivencia después de un paro cardíaco fueron más bajas cuando se produjo entre la medianoche y las 6 a. m. [57]
Muchas de estas causas no cardíacas de paro cardíaco son reversibles. Una regla mnemotécnica común que se utiliza para recordar las causas reversibles de paro cardíaco se conoce como H y T. Las H son hipovolemia , hipoxia , exceso de cationes hidrógeno ( acidosis ), hipercalemia , hipocalemia , hipotermia e hipoglucemia . Las T son toxinas , taponamiento (cardíaco) , neumotórax a tensión , trombosis ( infarto de miocardio ), tromboembolia y traumatismo.
Los mecanismos eléctricos definitivos del paro cardíaco, que pueden surgir de cualquiera de las anomalías funcionales, estructurales o fisiológicas mencionadas anteriormente, se caracterizan por arritmias. [29] La fibrilación ventricular y la taquicardia ventricular sin pulso o sostenida son las arritmias registradas con mayor frecuencia que preceden al paro cardíaco. Se trata de arritmias rápidas y erráticas que alteran la vía circulatoria de tal manera que no se puede mantener un flujo sanguíneo adecuado y es inadecuado para satisfacer las necesidades del cuerpo. [29]
El mecanismo responsable de la mayoría de las muertes cardíacas súbitas es la fibrilación ventricular. La fibrilación ventricular es una taquiarritmia caracterizada por una actividad eléctrica turbulenta en el miocardio ventricular que conduce a una frecuencia cardíaca demasiado desorganizada y rápida para producir un gasto cardíaco significativo, lo que da lugar a una perfusión insuficiente del cerebro y los órganos esenciales. [58] Algunos de los mecanismos electrofisiológicos que sustentan las fibrilaciones ventriculares incluyen el automatismo ectópico, la reentrada y la actividad desencadenada. [59] Sin embargo, los cambios estructurales en el corazón enfermo como resultado de factores hereditarios (mutaciones en los genes que codifican los canales iónicos, por ejemplo) no pueden explicar la aparición repentina de un paro cardíaco. [60]
En la taquicardia ventricular, el corazón también late más rápido de lo normal, lo que puede impedir que las cámaras cardíacas se llenen adecuadamente de sangre. [61] La taquicardia ventricular se caracteriza por un complejo QRS alterado y una frecuencia cardíaca superior a 100 latidos por minuto. [62] Cuando la taquicardia ventricular se mantiene (dura al menos 30 segundos), el flujo sanguíneo inadecuado al tejido cardíaco puede provocar un paro cardíaco. [63]
Las bradiarritmias se producen tras la disociación de la conducción eléctrica espontánea y la función mecánica del corazón, lo que da lugar a una actividad eléctrica sin pulso (AESP) o a la ausencia total de actividad eléctrica del corazón, lo que da lugar a una asistolia . De forma similar a lo que ocurre con las taquiarritmias, estas afecciones también provocan una incapacidad para mantener un flujo sanguíneo adecuado, aunque en el caso de las bradiarritmias, la causa subyacente es la ausencia de actividad mecánica en lugar de latidos rápidos que provocan desorganización. [29]

El paro cardíaco es sinónimo de muerte clínica . [17] El examen físico para diagnosticar el paro cardíaco se centra en la ausencia de pulso. [30] En muchos casos, la falta de pulso central ( arterias carótidas o arterias subclavias ) es el estándar de oro . La falta de pulso en la periferia (radial/pedal) también puede ser el resultado de otras condiciones (p. ej., shock ) o ser una mala interpretación del reanimador.
Obtener una historia clínica completa puede ayudar a determinar la causa potencial y el pronóstico. [30] El médico que toma la historia clínica de la persona debe tratar de averiguar si el episodio fue observado por otra persona, cuándo ocurrió, qué estaba haciendo el paciente (en particular, si hubo algún trauma) y si hubo uso de medicamentos. [30]
Durante los esfuerzos de reanimación, se debe conectar al paciente un equipo de monitoreo continuo que incluya derivaciones de ECG para que los proveedores puedan analizar la actividad eléctrica del ciclo cardíaco y usar esta información para guiar los esfuerzos de manejo. Las lecturas de ECG ayudarán a identificar la arritmia presente y permitirán al equipo monitorear cualquier cambio que ocurra con la administración de RCP y desfibrilación. Los médicos clasifican el paro cardíaco en "desfibrilable" versus "no desfibrilable", según lo determinado por el ritmo de ECG . Esto se refiere a si una clase particular de arritmia cardíaca es tratable mediante desfibrilación . [64] Los dos ritmos "desfibrilables" son la fibrilación ventricular y la taquicardia ventricular sin pulso , mientras que los dos ritmos "no desfibrilables" son la asistolia y la actividad eléctrica sin pulso . [65] Además, en el paciente posterior a la reanimación, un ECG de 12 derivaciones puede ayudar a identificar algunas causas de paro cardíaco, como STEMI que puede requerir tratamientos específicos.
La ecografía en el punto de atención (POCUS) es una herramienta que se puede utilizar para examinar el movimiento del corazón y su fuerza de contracción junto a la cama del paciente. [66] La POCUS puede diagnosticar con precisión el paro cardíaco en entornos hospitalarios, así como visualizar las contracciones del movimiento de la pared cardíaca. [66] Con la POCUS, los médicos pueden tener vistas limitadas y bidimensionales de diferentes partes del corazón durante el paro. [67] Estas imágenes pueden ayudar a los médicos a determinar si la actividad eléctrica dentro del corazón es sin pulso o pseudo-sin pulso, así como a diagnosticar las causas potencialmente reversibles de un paro. [67] Las pautas publicadas de la Sociedad Estadounidense de Ecocardiografía , el Colegio Estadounidense de Médicos de Emergencia , el Consejo Europeo de Resucitación y la Asociación Estadounidense del Corazón , así como las pautas de Soporte Vital Cardíaco Avanzado preoperatorio de 2018 , han reconocido los posibles beneficios del uso de POCUS en el diagnóstico y manejo del paro cardíaco. [67]
La ecografía transtorácica puede ayudar a predecir los resultados de las maniobras de reanimación. En concreto, el uso de la ecografía transtorácica puede ser una herramienta útil para predecir la mortalidad en casos de paro cardíaco. Una revisión sistemática de 2020 concluyó que existe una correlación positiva significativa entre la presencia de movimiento cardíaco y la supervivencia a corto plazo con RCP. [68]
Debido a la inexactitud del diagnóstico basado únicamente en la detección del pulso central, algunos organismos como el Consejo Europeo de Resucitación han restado importancia a su importancia. En cambio, las directrices actuales instan a las personas a iniciar la RCP en cualquier persona inconsciente con respiración ausente o anormal. [64] El Consejo de Resucitación del Reino Unido se mantiene en línea con las recomendaciones del Consejo Europeo de Resucitación y las de la Asociación Estadounidense del Corazón. [17] Han sugerido que la técnica para verificar los pulsos carotideos debe ser utilizada solo por profesionales de la salud con capacitación y experiencia específicas, e incluso entonces que debe considerarse junto con otros indicadores como la respiración agónica . [64]
Se han propuesto otros métodos para detectar la circulación y, por lo tanto, diagnosticar el paro cardíaco. Las directrices que siguieron las recomendaciones del Comité de Enlace Internacional sobre Reanimación de 2000 establecían que los reanimadores debían buscar "signos de circulación", pero no específicamente el pulso. [17] Estos signos incluían tos, jadeo, color, espasmos y movimiento. [69] Debido a la evidencia de que estas directrices fueron ineficaces, la recomendación actual del Comité de Enlace Internacional sobre Reanimación es que el paro cardíaco se debe diagnosticar en todas las víctimas que están inconscientes y no respiran normalmente, un protocolo similar al que ha adoptado el Consejo Europeo de Reanimación. [17] En un entorno no agudo donde el paciente está muerto, el diagnóstico de paro cardíaco se puede realizar mediante una autopsia molecular o una prueba molecular post mortem, que utiliza un conjunto de técnicas moleculares para encontrar los canales iónicos que son defectuosos en el corazón. [70] Esto podría ayudar a dilucidar la causa de la muerte del paciente.
Otros signos o síntomas físicos pueden ayudar a determinar la causa potencial del paro cardíaco. [30] A continuación se muestra un cuadro de los hallazgos clínicos y los signos/síntomas que puede tener una persona y las posibles causas asociadas con ellos.
Ante la falta de resultados positivos tras un paro cardíaco, se han dedicado esfuerzos a encontrar estrategias eficaces para prevenir los episodios de paro cardíaco. El enfoque de la prevención primaria promueve una dieta saludable , ejercicio , consumo limitado de alcohol y dejar de fumar . [5]
El ejercicio es una medida preventiva eficaz contra el paro cardíaco en la población general, pero puede ser riesgoso para quienes padecen enfermedades preexistentes. [71] El riesgo de un evento cardíaco catastrófico transitorio aumenta en individuos con enfermedades cardíacas durante e inmediatamente después del ejercicio. [71] Los riesgos de por vida y agudos de paro cardíaco disminuyen en personas con enfermedades cardíacas que realizan ejercicio regularmente, lo que quizás sugiere que los beneficios del ejercicio superan los riesgos. [71]
Un estudio de 2021 encontró que la dieta puede ser un factor de riesgo modificable para una menor incidencia de muerte cardíaca súbita. [72] El estudio encontró que aquellos que caían dentro de la categoría de tener "dietas sureñas" que representan las de "grasas agregadas, alimentos fritos, huevos, vísceras y carnes procesadas y bebidas azucaradas" tenían una asociación positiva con un mayor riesgo de paro cardíaco, mientras que aquellos considerados siguiendo las " dietas mediterráneas " tenían una relación inversa con respecto al riesgo de paro cardíaco. [72] Según una revisión publicada en 2012, la suplementación con PUFA omega-3 no está asociada con un menor riesgo de muerte cardíaca súbita. [73]
Una revisión Cochrane publicada en 2016 encontró evidencia de calidad moderada que muestra que los medicamentos para reducir la presión arterial no reducen el riesgo de muerte cardíaca súbita. [74]
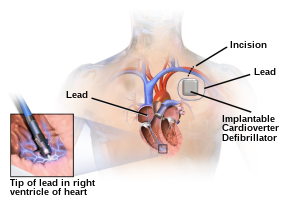
Un desfibrilador automático implantable (DAI) es un dispositivo alimentado por batería que monitorea la actividad eléctrica del corazón y, cuando se detecta una arritmia, puede administrar una descarga eléctrica para interrumpir el ritmo anormal. Los desfibriladores automáticos implantables se utilizan para prevenir la muerte súbita cardíaca (MSC) en personas que han sobrevivido a un episodio previo de paro cardíaco súbito (PCR) debido a fibrilación ventricular o taquicardia ventricular. [75]
Se han realizado numerosos estudios sobre el uso de DCI para la prevención secundaria de la MSC. Estos estudios han demostrado una mejor supervivencia con DCI en comparación con el uso de fármacos antiarrítmicos. [75] El tratamiento con DCI se asocia con una reducción del riesgo relativo del 50% de muerte causada por una arritmia y una reducción del riesgo relativo del 25% de mortalidad por todas las causas. [76]
La prevención de la MSC con terapia con CDI para poblaciones de pacientes de alto riesgo también ha demostrado mejores tasas de supervivencia en varios estudios a gran escala. Las poblaciones de pacientes de alto riesgo en estos estudios se definieron como aquellas con miocardiopatía isquémica grave (determinada por una fracción de eyección del ventrículo izquierdo [FEVI] reducida). Los criterios de FEVI utilizados en estos ensayos variaron desde menos de o igual al 30% en MADIT-II hasta menos de o igual al 40% en MUSTT. [75] [77]
En ciertas poblaciones de pacientes de alto riesgo (como pacientes con síndrome de QT largo), los DCI también se utilizan para prevenir la muerte cardíaca súbita ( prevención primaria ). [77]
En el hospital, un paro cardíaco se denomina "accidente cardíaco" o "código". Esto generalmente se refiere al código azul en los códigos de emergencia del hospital . Una caída drástica en las mediciones de los signos vitales se conoce como "codificación" o "accidente cardíaco", aunque la codificación se usa generalmente cuando resulta en un paro cardíaco, mientras que el accidente cardíaco podría no serlo. El tratamiento del paro cardíaco a veces se conoce como "llamar a un código".
Los pacientes en salas generales suelen deteriorarse durante varias horas o incluso días antes de que se produzca un paro cardíaco. [64] [78] Esto se ha atribuido a una falta de conocimientos y habilidades entre el personal de las salas, en particular, a una falta de medición de la frecuencia respiratoria , que suele ser el principal predictor de un deterioro [64] y que a menudo puede cambiar hasta 48 horas antes de un paro cardíaco. En respuesta, muchos hospitales han aumentado ahora la formación del personal de las salas. También existen varios sistemas de "alerta temprana" que tienen como objetivo cuantificar el riesgo de deterioro de la persona en función de sus signos vitales y, por tanto, proporcionar una guía al personal. Además, se está utilizando personal especializado de forma más eficaz para ampliar el trabajo que ya se realiza a nivel de sala. Estos incluyen:
El paro cardíaco repentino puede tratarse mediante intentos de reanimación . Esto suele llevarse a cabo según las pautas del soporte vital básico , soporte vital cardíaco avanzado (ACLS), soporte vital avanzado pediátrico (PALS) o programa de reanimación neonatal (NRP). [17] [79]

La reanimación cardiopulmonar (RCP) temprana es esencial para sobrevivir a un paro cardíaco con una buena función neurológica. [80] [30] Se recomienda que se inicie lo antes posible con interrupciones mínimas una vez iniciada. Los componentes de la RCP que marcan la mayor diferencia en la supervivencia son las compresiones torácicas y la desfibrilación de ritmos desfibrilables. [81] Después de la desfibrilación, las compresiones torácicas deben continuar durante dos minutos antes de volver a verificar el ritmo. [30] Esto se basa en una frecuencia de compresión de 100-120 compresiones por minuto, una profundidad de compresión de 5-6 centímetros en el tórax, retroceso torácico completo y una frecuencia de ventilación de 10 ventilaciones por minuto. [30] Las compresiones torácicas mecánicas (realizadas por una máquina) no son mejores que las compresiones torácicas realizadas a mano. [82] No está claro si unos pocos minutos de RCP antes de la desfibrilación producen resultados diferentes a la desfibrilación inmediata. [83]
Se ha demostrado que la RCP realizada correctamente por un transeúnte aumenta la supervivencia; sin embargo, se realiza en menos del 30 % de los paros cardíacos extrahospitalarios (PCEH) en 2007. [actualizar][ 84] Un metanálisis de 2019 encontró que el uso de RCP asistida por un despachador mejoró los resultados, incluida la supervivencia, en comparación con la RCP no dirigida por un transeúnte. [85] Asimismo, una revisión sistemática de 2022 sobre paros cardíacos relacionados con el ejercicio respaldó la intervención temprana de la RCP por parte de un transeúnte y el uso de DEA (para ritmos desfibrilables), ya que mejoran los resultados de supervivencia. [86]
Si la RCP de alta calidad no ha dado como resultado el retorno de la circulación espontánea y el ritmo cardíaco de la persona está en asistolia , detener la RCP y declarar la muerte de la persona es generalmente razonable después de 20 minutos. [87] Las excepciones a esto incluyen ciertos casos con hipotermia o víctimas de ahogamiento . [81] [87] Algunos de estos casos deben recibir una RCP más prolongada y sostenida hasta que estén casi normotérmicos . [81]
Si se produce un paro cardíaco después de las 20 semanas de embarazo, se debe tirar del útero o empujarlo hacia la izquierda durante la RCP. [88] Si el pulso no ha regresado a los cuatro minutos, se recomienda una cesárea de emergencia. [88]
Generalmente, durante la RCP se administran altos niveles de oxígeno. [82] Se puede utilizar una mascarilla con bolsa y válvula o un dispositivo avanzado para la vía aérea para ayudar con la respiración, en particular porque los vómitos y la regurgitación son comunes, especialmente en el OHCA. [82] [89] [90] Si esto ocurre, puede ser necesaria una modificación de la succión orofaríngea existente, como el uso de un manejo de la vía aérea asistido por succión . [91]
No se ha demostrado que la intubación traqueal mejore las tasas de supervivencia o los resultados neurológicos en caso de paro cardíaco, [84] [92] y en el entorno prehospitalario, puede empeorarlo. [93] Los tubos endotraqueales y las vías respiratorias supraglóticas parecen igualmente útiles. [92]
La respiración boca a boca como medio para proporcionar respiración a la persona ha sido eliminada gradualmente debido al riesgo de contraer enfermedades infecciosas de la persona afectada. [94]
Cuando lo realiza personal médico de emergencia, 30 compresiones seguidas de dos respiraciones parecen ser mejores que las compresiones torácicas continuas y las respiraciones administradas mientras se realizan las compresiones. [95] Para los transeúntes, la RCP que implica solo compresiones torácicas produce mejores resultados en comparación con la RCP estándar para aquellos que han sufrido un paro cardíaco debido a problemas cardíacos. [95]

La desfibrilación está indicada si existe un ritmo cardíaco electroshockeable. Los dos ritmos electroshockeables son la fibrilación ventricular y la taquicardia ventricular sin pulso . Estos ritmos electroshockeables tienen una probabilidad de supervivencia del 25-40%, en comparación con una tasa significativamente menor (menos del 5%) en los ritmos no electroshockeables. [96] Los ritmos no electroshockeables incluyen la asistolia y la actividad eléctrica sin pulso.
La fibrilación ventricular implica que los ventrículos del corazón (las cámaras inferiores responsables de bombear la sangre) se contraen rápidamente en un patrón desorganizado y, por lo tanto, limitan el flujo sanguíneo del corazón. Esto puede deberse a una actividad eléctrica descoordinada. [97] El electrocardiograma (ECG) generalmente muestra complejos QRS irregulares sin ondas P. [98] Por el contrario, el ECG para la taquicardia ventricular generalmente mostrará un complejo QRS ancho con más de 100 latidos por minuto. [99] Si se mantiene, la taquicardia ventricular también puede provocar inestabilidad y compromiso hemodinámico, lo que resulta en falta de pulso y mala perfusión a los órganos vitales.
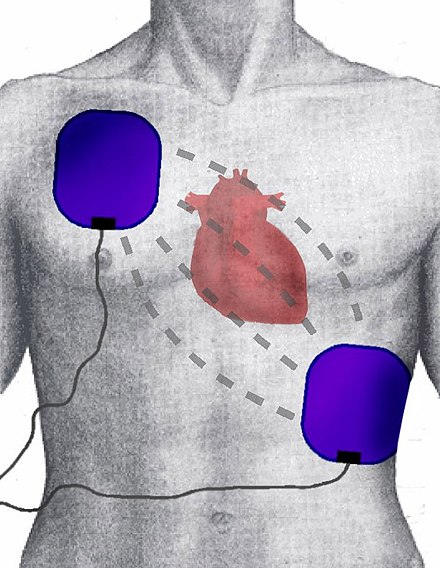
Un desfibrilador suministra una corriente eléctrica a través de un par de electrodos colocados en el pecho de la persona. Se cree que esto despolariza el tejido miocárdico y, por lo tanto, detiene la arritmia. [100] Los desfibriladores pueden suministrar energía como formas de onda monofásicas o bifásicas, aunque los desfibriladores bifásicos son los más comunes. [101] [102]
En el caso de la fibrilación ventricular, las técnicas de desfibrilación pueden utilizar ondas monofásicas o bifásicas. Estudios previos sugieren que es más probable que la descarga bifásica produzca una desfibrilación exitosa después de una sola descarga, sin embargo, la tasa de supervivencia es comparable entre los métodos. [102]
En los paros extrahospitalarios, la desfibrilación se realiza mediante un desfibrilador externo automático (DEA), un aparato portátil que puede ser utilizado por cualquier usuario. El DEA proporciona instrucciones de voz que guían el proceso, comprueba automáticamente el estado de la persona y aplica las descargas eléctricas adecuadas. Algunos desfibriladores incluso proporcionan información sobre la calidad de las compresiones de la RCP , animando al reanimador lego a presionar el pecho de la persona con la suficiente fuerza para que circule la sangre. [103]
Además, se está utilizando cada vez más la desfibrilación de acceso público, lo que implica colocar desfibriladores externos automáticos en lugares públicos y capacitar al personal de esas áreas sobre cómo utilizarlos. Esto permite que la desfibrilación se realice antes de la llegada de los servicios de emergencia, lo que se ha demostrado que aumenta las posibilidades de supervivencia. Las personas que sufren paros cardíacos en lugares remotos tienen peores resultados después de un paro cardíaco. [104]
La desfibrilación se aplica a ciertas arritmias, como la fibrilación ventricular y la taquicardia ventricular sin pulso. La desfibrilación no se puede aplicar a la asistolia, y en este caso se debe iniciar primero la RCP. Además, la desfibrilación es diferente a la cardioversión sincronizada . En la cardioversión sincronizada, se utiliza un enfoque similar en el que se aplica corriente eléctrica para corregir una arritmia, sin embargo, esto se utiliza en casos en los que hay pulso pero el paciente está hemodinámicamente inestable, como en la taquicardia supraventricular .
Los desfibriladores también pueden utilizarse como parte del tratamiento posterior a un paro cardíaco. Estos desfibriladores incluyen desfibriladores portátiles (como LifeVest), desfibriladores cardíacos subcutáneos y desfibriladores cardíacos implantables . [105]
Los medicamentos recomendados en el protocolo ACLS incluyen epinefrina, amiodarona y lidocaína. [9] El momento y la administración de estos medicamentos dependen de la arritmia subyacente del paro.
La epinefrina actúa sobre el receptor alfa-1, que a su vez aumenta el flujo sanguíneo que irriga el corazón. [106] La epinefrina en adultos mejora la supervivencia [107] pero no parece mejorar la supervivencia neurológicamente normal. [108] En la fibrilación ventricular y la taquicardia ventricular sin pulso, se administra 1 mg de epinefrina cada 3-5 minutos, después de una ronda inicial de RCP y desfibrilación. [82] No se recomiendan dosis superiores a 1 mg de epinefrina para uso rutinario en paro cardíaco. Si la persona tiene un ritmo no desfibrilable, como asistolia, después de una ronda inicial de RCP, se debe administrar 1 mg de epinefrina cada 3-5 minutos, con el objetivo de obtener un ritmo desfibrilable. [109]
La amiodarona y la lidocaína son medicamentos antiarrítmicos. La amiodarona es un antiarrítmico de clase III . La amiodarona se puede utilizar en casos de fibrilación ventricular , taquicardia ventricular sin pulso y taquicardia de complejos anchos . [110] La lidocaína es un antiarrítmico de clase Ib , que también se utiliza para tratar arritmias agudas. [111] Los medicamentos antiarrítmicos se pueden utilizar después de un intento de desfibrilación fallido. Sin embargo, ni la lidocaína ni la amiodarona, en aquellos que continúan con taquicardia ventricular o fibrilación ventricular a pesar de la desfibrilación, mejoran la supervivencia hasta el alta hospitalaria, a pesar de que ambas mejoran igualmente la supervivencia hasta el ingreso hospitalario. [112] Después de una ronda adicional de RCP y desfibrilación, también se puede administrar amiodarona. La primera dosis se administra como un bolo de 300 mg. La segunda dosis se administra en forma de bolo de 600 mg. [82]
El bicarbonato , administrado como bicarbonato de sodio, actúa para estabilizar la acidosis y la hipercalemia , que pueden contribuir al paro cardíaco y exacerbarlo. Si hay un desequilibrio ácido-base o electrolítico evidente, se puede utilizar bicarbonato. Sin embargo, si hay pocas sospechas de que estos desequilibrios estén ocurriendo y contribuyendo al paro cardíaco, no se recomienda el uso sistemático de bicarbonato, ya que no proporciona un beneficio adicional. [113]
El calcio , administrado como cloruro de calcio, funciona como inotrópico y vasopresor . El calcio se utiliza en circunstancias específicas, como alteraciones electrolíticas (hipercalemia) y toxicidad por bloqueadores de los canales de calcio . En general, el calcio no se utiliza de forma rutinaria durante el paro cardíaco, ya que no proporciona un beneficio adicional (en comparación con la falta de uso) e incluso puede causar daños (malos resultados neurológicos). [114]
En general, la vasopresina no mejora ni empeora los resultados en comparación con la epinefrina. [82] La combinación de epinefrina, vasopresina y metilprednisolona parece mejorar los resultados. [115]
No se ha demostrado que el uso de atropina, lidocaína y amiodarona mejore la supervivencia tras un paro cardíaco. [116] [117] [81]
La atropina se utiliza para la bradicardia sintomática . Se administra en dosis de 1 mg (iv) y se pueden administrar dosis adicionales de 1 mg (iv) cada 3 a 5 minutos para un total de 3 mg. Sin embargo, las pautas de 2010 de la Asociación Estadounidense del Corazón eliminaron la recomendación del uso de atropina en la actividad eléctrica sin pulso y la asistolia por falta de evidencia que respalde su uso. [118] [81]
Los pacientes en hemodiálisis tienen un mayor riesgo de sufrir paros cardíacos. Hay múltiples factores que contribuyen a ello, entre ellos, el aumento de los factores de riesgo cardiovascular, los trastornos electrolíticos (calcio y potasio, causados por la acumulación y la eliminación agresiva) y los trastornos del equilibrio ácido-base. [119] Los niveles de calcio se consideran un factor clave que contribuye a los paros cardíacos en esta población. [120]
La sobredosis de antidepresivos tricíclicos (ATC) puede provocar un paro cardíaco con hallazgos electrocardiográficos típicos, como QRS ancho y QTc prolongado. El tratamiento para esta afección incluye carbón activado y bicarbonato de sodio. [121]
El magnesio se puede administrar en dosis de 2 g (iv o bolo oral) para controlar las torsades de points . Sin embargo, sin una indicación específica, el magnesio no se suele administrar en caso de paro cardíaco. [122] En personas con una embolia pulmonar confirmada como causa del paro, los trombolíticos pueden ser beneficiosos. [123] [88] La evidencia del uso de naloxona en pacientes con paro cardíaco debido a opioides no es clara, pero aún puede usarse. [88] En personas con paro cardíaco debido a un anestésico local, se puede utilizar una emulsión lipídica . [88]
Las directrices internacionales actuales sugieren enfriar a los adultos después de un paro cardíaco utilizando el manejo de temperatura dirigido (TTM) con el objetivo de mejorar los resultados neurológicos. [124] El proceso implica enfriamiento durante un período de 24 horas, con una temperatura objetivo de 32-36 °C (90-97 °F), seguido de un recalentamiento gradual durante las siguientes 12 a 24 horas. [125] [126] Hay varios métodos utilizados para reducir la temperatura corporal, como la aplicación de bolsas de hielo o almohadillas circulantes de agua fría directamente al cuerpo o la infusión de solución salina fría.
La eficacia del TTM después de un paro cardíaco extrahospitalario es un área de estudio en curso. Varias revisiones recientes han encontrado que los pacientes tratados con TTM tienen resultados neurológicos más favorables. [20] [19] Sin embargo, se ha demostrado que el TTM prehospitalario después de un paro cardíaco extrahospitalario aumenta el riesgo de resultados adversos. [124] Las tasas de reparo cardíaco pueden ser más altas en personas que fueron tratadas con TTM prehospitalario. [124] Además, el TTM puede tener efectos neurológicos adversos en personas que sobreviven después de un paro cardíaco . [127] Las ondas de Osborn en el ECG son frecuentes durante el TTM, particularmente en pacientes tratados con 33 °C. [128] Las ondas de Osborn no están asociadas con un mayor riesgo de arritmia ventricular y pueden considerarse un fenómeno fisiológico benigno, asociado con una menor mortalidad en análisis univariables. [128]
Algunas personas optan por evitar medidas agresivas al final de la vida. Una orden de no reanimación (DNR, por sus siglas en inglés) en forma de directivas anticipadas de atención médica deja en claro que, en caso de paro cardíaco, la persona no desea recibir reanimación cardiopulmonar . [129] Se pueden hacer otras directivas para estipular el deseo de intubación en caso de insuficiencia respiratoria o, si lo único que se desea son medidas de confort, estipulando que los proveedores de atención médica deben "permitir la muerte natural". [130]
Varias organizaciones promueven la idea de una cadena de supervivencia . La cadena está formada por los siguientes "eslabones":
Si uno o más eslabones de la cadena faltan o se retrasan, las posibilidades de supervivencia disminuyen significativamente.
Estos protocolos suelen iniciarse con un código azul , que suele indicar la aparición inminente o aguda de un paro cardíaco o una insuficiencia respiratoria . [132]
Se ha intentado la reanimación con dispositivos de oxigenación por membrana extracorpórea con mejores resultados en el paro cardíaco intrahospitalario (29 % de supervivencia) que en el PCEH (4 % de supervivencia) en poblaciones seleccionadas para beneficiarse más. [133]
El cateterismo cardíaco en aquellos que han sobrevivido a un paro cardíaco extrahospitalario parece mejorar los resultados, aunque faltan evidencias de alta calidad. [134] Se recomienda realizarlo lo antes posible en aquellos que han tenido un paro cardíaco con elevación del segmento ST debido a problemas cardíacos subyacentes. [82]
El golpe precordial puede considerarse en aquellos con taquicardia ventricular inestable (incluida la TV sin pulso) presenciada y monitoreada si no hay un desfibrilador listo para su uso inmediato, pero no debe retrasar la RCP y la administración de la descarga ni usarse en aquellos con PCEH no presenciado. [135]
La tasa general de supervivencia entre quienes tienen un paro cardíaco extrahospitalario es del 10%. [136] [137] Entre quienes tienen un paro cardíaco extrahospitalario, el 70% ocurre en el hogar y su tasa de supervivencia es del 6%. [138] [139] Para quienes tienen un paro cardíaco intrahospitalario (IHCA), la tasa de supervivencia un año desde al menos la ocurrencia del paro cardíaco se estima en 13%. [140] Para IHCA, la supervivencia hasta el alta es de alrededor del 22%. [141] [81] Aquellos que sobreviven hasta el retorno de la circulación espontánea y el ingreso hospitalario con frecuencia presentan síndrome posparo cardíaco , que generalmente se presenta con lesión neurológica que puede variar desde problemas de memoria leves hasta coma . [81] Se estima que la supervivencia a un año es mayor en personas con diagnósticos de ingreso cardíaco (39%) en comparación con aquellos con diagnósticos de ingreso no cardíaco (11%). [140]
Una revisión de 1997 encontró tasas de supervivencia hasta el alta del 14%, aunque diferentes estudios variaron de 0 a 28%. [142] En aquellos mayores de 70 años que sufren un paro cardíaco mientras están hospitalizados, la supervivencia hasta el alta hospitalaria es inferior al 20%. [143] No está claro cómo se las arreglan estos individuos después de dejar el hospital. [143]
Se ha determinado que la tasa global de personas que pudieron recuperarse de un paro cardíaco extrahospitalario después de recibir RCP es de aproximadamente el 30%, y la tasa de supervivencia hasta el alta hospitalaria se ha estimado en el 9%. [144] La supervivencia hasta el alta hospitalaria es más probable entre las personas cuyo paro cardíaco fue presenciado por un transeúnte o por servicios médicos de emergencia, que recibieron RCP por parte de un transeúnte y que viven en Europa y América del Norte. [144] Se han observado tasas de supervivencia hasta el alta hospitalaria relativamente más bajas en los países asiáticos. [144]
El pronóstico se evalúa típicamente 72 horas o más después del paro cardíaco. [145] Las tasas de supervivencia son mejores en aquellos que tuvieron a alguien testigo de su colapso, recibieron RCP por parte de un transeúnte y/o tenían fibrilación ventricular o taquicardia ventricular cuando fueron evaluados. [146] La supervivencia entre aquellos con fibrilación ventricular o taquicardia ventricular es del 15 al 23%. [146] Las mujeres tienen más probabilidades de sobrevivir a un paro cardíaco y salir del hospital que los hombres. [147] La lesión cerebral hipóxica e isquémica es un resultado preocupante para las personas que sufren un paro cardíaco. [148] La mayoría de las mejoras en la cognición ocurren durante los primeros tres meses posteriores al paro cardíaco, y algunas personas informan una mejora hasta un año después del paro cardíaco. [148] Entre el 50 y el 70 % de los sobrevivientes de un paro cardíaco informan fatiga como síntoma. [148]
El riesgo de sufrir un paro cardíaco varía según la región geográfica, la edad y el sexo. El riesgo a lo largo de la vida es tres veces mayor en los hombres (12,3%) que en las mujeres (4,2%) según el análisis del Framingham Heart Study . [149] Esta diferencia de género desaparece después de los 85 años de edad. [150] Alrededor de la mitad de estos individuos son menores de 65 años de edad. [151]
Según los certificados de defunción, la muerte súbita cardíaca representa aproximadamente el 20% de todas las muertes en los Estados Unidos. [152] [153] En los Estados Unidos, ocurren aproximadamente 326.000 casos de muerte súbita cardíaca extrahospitalaria y 209.000 casos de muerte súbita cardíaca intrahospitalaria entre adultos anualmente, lo que equivale a una incidencia de aproximadamente 110,8 por cada 100.000 adultos por año. [9] [81] [152]
En los Estados Unidos, el paro cardíaco durante el embarazo ocurre en aproximadamente uno de cada doce mil partos o 1,8 por cada 10 000 nacidos vivos. [88] Las tasas son más bajas en Canadá. [88]
Las regiones no occidentales del mundo tienen diferentes incidencias. La incidencia de muerte súbita cardíaca en China es de 41,8 por 100.000 y en el sur de la India es de 39,7 por 100.000. [152]
En muchas publicaciones, el significado explícito o explícito de “muerte súbita cardíaca” es muerte súbita por causas cardíacas. [154] Algunos médicos llaman al paro cardíaco “muerte súbita cardíaca” incluso si la persona sobrevive. Por ello, se pueden oír menciones de “episodios previos de muerte súbita cardíaca” en una persona viva. [155]
En 2021, la Asociación Estadounidense del Corazón aclaró que el término "ataque cardíaco" se suele utilizar erróneamente para describir un paro cardíaco. Si bien un ataque cardíaco se refiere a la muerte del tejido muscular del corazón como resultado de la pérdida del suministro de sangre, el paro cardíaco se produce cuando el sistema eléctrico del corazón funciona mal. Además, la Asociación Estadounidense del Corazón explica que "si no se toman medidas correctivas rápidamente, esta afección progresa a muerte súbita. El paro cardíaco debe utilizarse para significar un evento como el descrito anteriormente, que se revierte, generalmente mediante RCP y/o desfibrilación o cardioversión , o marcapasos cardíaco . La muerte súbita cardíaca no debe utilizarse para describir eventos que no son fatales". [156]
Un " código lento " es un término del argot que designa la práctica de administrar de manera engañosa una RCP subóptima a una persona en paro cardíaco, cuando se considera que la RCP no tiene ningún beneficio médico. [157] Un "código de exhibición" es la práctica de fingir la respuesta por completo para el bien de la familia de la persona. [158]
Estas prácticas son éticamente controvertidas [159] y están prohibidas en algunas jurisdicciones. Las directrices del Consejo Europeo de Resucitación publicaron una declaración en 2021 en la que se indica que no se recomienda a los médicos participar en "códigos lentos". [157] Según el Colegio Estadounidense de Médicos, los intentos de reanimación poco entusiastas son engañosos y no deberían ser realizados por médicos o enfermeras. [160]
En los niños, la causa más frecuente de paro cardíaco es el shock o la insuficiencia respiratoria que no ha sido tratada. [30] Las arritmias cardíacas son otra posible causa. Las arritmias como la asistolia o la bradicardia son más probables en los niños, en contraste con la fibrilación ventricular o la taquicardia que se observan en los adultos. [30]
Otras causas de paro cardíaco repentino e inexplicable en niños incluyen miocardiopatía hipertrófica y anomalías de la arteria coronaria. [161] En la miocardiopatía hipertrófica infantil, se ha demostrado que los eventos cardíacos adversos previos, la taquicardia ventricular no sostenida, el síncope y la hipertrofia ventricular izquierda predicen la muerte cardíaca súbita. [162] Otras causas pueden incluir drogas, como la cocaína y la metanfetamina , o sobredosis de medicamentos, como los antidepresivos. [30]
Para el tratamiento del paro cardíaco pediátrico, se debe iniciar la reanimación cardiopulmonar si se sospecha. Las pautas proporcionan algoritmos para el tratamiento del paro cardíaco pediátrico. Los medicamentos recomendados durante la reanimación pediátrica incluyen epinefrina, lidocaína y amiodarona. [163] [81] [82] Sin embargo, no se recomienda el uso de bicarbonato de sodio o calcio. [82] [164] El uso de calcio en niños se ha asociado con una función neurológica deficiente, así como con una disminución de la supervivencia. [30] La dosis correcta de medicamentos en niños depende del peso y, para minimizar el tiempo dedicado a calcular las dosis de medicamentos, se recomienda el uso de una cinta de Broselow . [30]
Las tasas de supervivencia en niños con paro cardíaco son del 3 al 16% en América del Norte. [163]
{{cite journal}}: CS1 maint: DOI inactivo a partir de noviembre de 2024 ( enlace )