La purificación del agua es el proceso de eliminación de sustancias químicas indeseables, contaminantes biológicos, sólidos suspendidos y gases del agua . El objetivo es producir agua que sea apta para fines específicos. La mayor parte del agua se purifica y desinfecta para el consumo humano ( agua potable ), pero la purificación del agua también se puede llevar a cabo para una variedad de otros fines, incluidas aplicaciones médicas, farmacológicas, químicas e industriales. La historia de la purificación del agua incluye una amplia variedad de métodos. Los métodos utilizados incluyen procesos físicos como la filtración , la sedimentación y la destilación ; procesos biológicos como filtros de arena lentos o carbón biológicamente activo ; procesos químicos como la floculación y la cloración ; y el uso de radiación electromagnética como la luz ultravioleta .
La purificación del agua puede reducir la concentración de partículas, incluidas partículas suspendidas , parásitos , bacterias, algas , virus y hongos, así como reducir la concentración de una variedad de partículas y materia disuelta.
Los estándares de calidad del agua potable suelen ser establecidos por los gobiernos o por normas internacionales. Estos estándares suelen incluir concentraciones mínimas y máximas de contaminantes, según el uso previsto del agua.
Una inspección visual no puede determinar si el agua es de la calidad adecuada. Procedimientos sencillos como hervir el agua o utilizar un filtro de carbón activado para el hogar no son suficientes para tratar todos los posibles contaminantes que puedan estar presentes en el agua de origen desconocido. Incluso el agua de manantial natural , considerada segura a todos los efectos prácticos en el siglo XIX, ahora debe analizarse antes de determinar qué tipo de tratamiento, si es necesario, es necesario. Los análisis químicos y microbiológicos , aunque costosos, son la única forma de obtener la información necesaria para decidir el método de purificación adecuado.

Los objetivos del tratamiento son eliminar los componentes no deseados del agua y hacerla apta para beber o apta para un propósito específico en aplicaciones industriales o médicas. Existen técnicas muy variadas para eliminar contaminantes como sólidos finos, microorganismos y algunos materiales inorgánicos y orgánicos disueltos, o contaminantes farmacéuticos persistentes ambientales . La elección del método dependerá de la calidad del agua que se esté tratando, el costo del proceso de tratamiento y los estándares de calidad esperados del agua procesada.
Los procesos que se indican a continuación son los que se utilizan habitualmente en las plantas de purificación de agua. Es posible que algunos o la mayoría no se utilicen, según la escala de la planta y la calidad del agua cruda (de origen).
El agua pura tiene un pH cercano a 7 (ni alcalina ni ácida ). El agua de mar puede tener valores de pH que van desde 7,5 a 8,4 (moderadamente alcalina). El agua dulce puede tener valores de pH muy variables según la geología de la cuenca de drenaje o acuífero y la influencia de los aportes de contaminantes ( lluvia ácida ). Si el agua es ácida (inferior a 7), se puede añadir cal , carbonato de sodio o hidróxido de sodio para aumentar el pH durante los procesos de purificación del agua. La adición de cal aumenta la concentración de iones de calcio, aumentando así la dureza del agua. En el caso de aguas muy ácidas, los desgasificadores de tiro forzado pueden ser una forma eficaz de aumentar el pH, eliminando del agua el dióxido de carbono disuelto. [2] Hacer que el agua sea alcalina ayuda a que los procesos de coagulación y floculación funcionen de forma eficaz y también ayuda a minimizar el riesgo de que el plomo se disuelva de las tuberías de plomo y de la soldadura de plomo en los accesorios de las tuberías. Una alcalinidad suficiente también reduce la corrosividad del agua para las tuberías de hierro. En algunas circunstancias, se puede añadir ácido ( ácido carbónico , ácido clorhídrico o ácido sulfúrico ) a las aguas alcalinas para reducir el pH. El agua alcalina (por encima de un pH de 7,0) no significa necesariamente que el plomo o el cobre del sistema de plomería no se disuelvan en el agua. La capacidad del agua para precipitar carbonato de calcio para proteger las superficies metálicas y reducir la probabilidad de que se disuelvan metales tóxicos en el agua es una función del pH, el contenido mineral, la temperatura, la alcalinidad y la concentración de calcio. [3]

Uno de los primeros pasos en la mayoría de los procesos convencionales de purificación de agua es la adición de productos químicos para ayudar a eliminar las partículas suspendidas en el agua. Las partículas pueden ser inorgánicas, como arcilla y limo , u orgánicas, como algas , bacterias, virus , protozoos y materia orgánica natural . Las partículas inorgánicas y orgánicas contribuyen a la turbidez y el color del agua.
La adición de coagulantes inorgánicos como el sulfato de aluminio (o alumbre ) o sales de hierro (III) como el cloruro de hierro (III) provoca varias interacciones químicas y físicas simultáneas sobre y entre las partículas. En cuestión de segundos, las cargas negativas de las partículas son neutralizadas por coagulantes inorgánicos. También en cuestión de segundos, comienzan a formarse precipitados de hidróxido metálico de los iones de hierro y aluminio. Estos precipitados se combinan en partículas más grandes mediante procesos naturales como el movimiento browniano y mediante una mezcla inducida que a veces se denomina floculación . Los hidróxidos metálicos amorfos se conocen como "floc". Los hidróxidos de aluminio y hierro (III) amorfos grandes adsorben y enredan partículas en suspensión y facilitan la eliminación de partículas mediante procesos posteriores de sedimentación y filtración . [4] : 8.2–8.3
Los hidróxidos de aluminio se forman en un rango de pH bastante estrecho, típicamente de 5,5 a aproximadamente 7,7. Los hidróxidos de hierro (III) pueden formarse en un rango de pH más amplio, incluidos niveles de pH más bajos que los que son efectivos para el alumbre, típicamente de 5,0 a 8,5. [5] : 679
En la literatura, existe mucho debate y confusión sobre el uso de los términos coagulación y floculación: ¿dónde termina la coagulación y dónde comienza la floculación? En las plantas de purificación de agua, generalmente hay un proceso de unidad de mezcla rápida y de alta energía (tiempo de detención en segundos) mediante el cual se agregan los químicos coagulantes, seguido de cuencas de floculación (los tiempos de detención varían de 15 a 45 minutos) donde los insumos de baja energía hacen girar paletas grandes u otros dispositivos de mezcla suaves para mejorar la formación de flóculos. De hecho, los procesos de coagulación y floculación continúan una vez que se agregan los coagulantes de sales metálicas. [6] : 74–5
Los polímeros orgánicos se desarrollaron en la década de 1960 como complemento de los coagulantes y, en algunos casos, como sustitutos de los coagulantes de sales metálicas inorgánicas. Los polímeros orgánicos sintéticos son compuestos de alto peso molecular que tienen cargas negativas, positivas o neutras. Cuando se añaden polímeros orgánicos al agua con partículas, los compuestos de alto peso molecular se adsorben en las superficies de las partículas y, a través de la formación de puentes entre partículas, se fusionan con otras partículas para formar flóculos. PolyDADMAC es un polímero orgánico catiónico (con carga positiva) popular que se utiliza en plantas de purificación de agua. [5] : 667–8
Las aguas que salen de la cuenca de floculación pueden ingresar a la cuenca de sedimentación , también llamada clarificadora o cuenca de sedimentación. Es un tanque grande con bajas velocidades de agua, lo que permite que los flóculos se sedimenten en el fondo. La cuenca de sedimentación se ubica mejor cerca de la cuenca de floculación para que el tránsito entre los dos procesos no permita la sedimentación o la ruptura de los flóculos. Las cuencas de sedimentación pueden ser rectangulares, donde el agua fluye de un extremo a otro, o circulares donde el flujo es desde el centro hacia afuera. La salida de la cuenca de sedimentación generalmente se realiza sobre un vertedero, por lo que solo sale una fina capa superior de agua, la más alejada del lodo.
En 1904, Allen Hazen demostró que la eficiencia de un proceso de sedimentación era una función de la velocidad de sedimentación de las partículas, el flujo a través del tanque y el área de superficie del tanque. Los tanques de sedimentación generalmente se diseñan dentro de un rango de tasas de desbordamiento de 0,5 a 1,0 galones por minuto por pie cuadrado (o 1250 a 2500 litros por metro cuadrado por hora). En general, la eficiencia de la cuenca de sedimentación no es una función del tiempo de detención o la profundidad de la cuenca. Sin embargo, la profundidad de la cuenca debe ser suficiente para que las corrientes de agua no perturben el lodo y se fomenten las interacciones de las partículas sedimentadas. A medida que las concentraciones de partículas en el agua sedimentada aumentan cerca de la superficie del lodo en el fondo del tanque, las velocidades de sedimentación pueden aumentar debido a las colisiones y la aglomeración de partículas. Los tiempos de detención típicos para la sedimentación varían de 1,5 a 4 horas y las profundidades de la cuenca varían de 10 a 15 pies (3 a 4,5 metros). [4] : 9,39–9,40 [5] : 790–1 [6] : 140–2, 171
Se pueden añadir clarificadores de láminas , placas planas inclinadas o tubos a los tanques de sedimentación tradicionales para mejorar el rendimiento de eliminación de partículas. Las placas y tubos inclinados aumentan drásticamente la superficie disponible para eliminar las partículas, de acuerdo con la teoría original de Hazen. La cantidad de superficie del suelo ocupada por un tanque de sedimentación con placas o tubos inclinados puede ser mucho menor que la de un tanque de sedimentación convencional.
A medida que las partículas se depositan en el fondo de un estanque de sedimentación, se forma una capa de lodo en el fondo del tanque que debe eliminarse y tratarse. La cantidad de lodo generado es significativa, a menudo entre el 3 y el 5 por ciento del volumen total de agua a tratar. El costo de tratamiento y eliminación del lodo puede afectar el costo operativo de una planta de tratamiento de agua. El estanque de sedimentación puede estar equipado con dispositivos de limpieza mecánica que limpien continuamente su fondo, o el estanque puede retirarse periódicamente del servicio y limpiarse manualmente.
Una subcategoría de la sedimentación es la eliminación de partículas mediante el atrapamiento en una capa de flóculos suspendidos a medida que el agua es forzada a ascender. La principal ventaja de los clarificadores de manta de flóculos es que ocupan un espacio menor que la sedimentación convencional. Las desventajas son que la eficiencia de eliminación de partículas puede ser muy variable dependiendo de los cambios en la calidad del agua de entrada y el caudal de agua de entrada. [5] : 835–6
Cuando las partículas que se deben eliminar no se sedimentan fácilmente de la solución, a menudo se utiliza la flotación por aire disuelto (DAF). Después de los procesos de coagulación y floculación, el agua fluye hacia los tanques de DAF donde los difusores de aire en el fondo del tanque crean burbujas finas que se adhieren a los flóculos, lo que da como resultado una masa flotante de flóculos concentrados. La capa de flóculos flotantes se retira de la superficie y el agua clarificada se retira del fondo del tanque de DAF. Los suministros de agua que son particularmente vulnerables a las floraciones de algas unicelulares y los suministros con baja turbidez y alto color a menudo utilizan DAF. [4] : 9.46
Después de separar la mayor parte de los flóculos, el agua se filtra como paso final para eliminar las partículas suspendidas restantes y los flóculos no sedimentados.

El tipo de filtro más común es el filtro de arena rápido . El agua se mueve verticalmente a través de la arena, que a menudo tiene una capa de carbón activado o carbón antracita encima de la arena. La capa superior elimina los compuestos orgánicos, que contribuyen al sabor y el olor. El espacio entre las partículas de arena es mayor que el de las partículas suspendidas más pequeñas, por lo que la filtración simple no es suficiente. La mayoría de las partículas pasan a través de las capas superficiales, pero quedan atrapadas en los espacios porosos o se adhieren a las partículas de arena. La filtración eficaz se extiende a la profundidad del filtro. Esta propiedad del filtro es clave para su funcionamiento: si la capa superior de arena bloqueara todas las partículas, el filtro se obstruiría rápidamente. [7]
Para limpiar el filtro, se hace pasar agua rápidamente hacia arriba a través del filtro, en dirección opuesta a la normal (lo que se denomina retrolavado o lavado a contracorriente ) para eliminar las partículas incrustadas o no deseadas. Antes de este paso, se puede soplar aire comprimido a través de la parte inferior del filtro para romper el medio filtrante compactado y ayudar al proceso de retrolavado; esto se conoce como limpieza con aire . Esta agua contaminada se puede eliminar junto con el lodo del depósito de sedimentación o se puede reciclar mezclándola con el agua cruda que ingresa a la planta, aunque esto a menudo se considera una mala práctica ya que reintroduce una concentración elevada de bacterias en el agua cruda.
Algunas plantas de tratamiento de agua emplean filtros a presión. Estos funcionan según el mismo principio que los filtros de gravedad rápidos, pero se diferencian en que el medio filtrante está encerrado en un recipiente de acero y el agua pasa a través de él bajo presión.
Ventajas:


Los filtros de arena lentos se pueden utilizar donde hay suficiente terreno y espacio, ya que el agua fluye muy lentamente a través de los filtros. Estos filtros dependen de procesos de tratamiento biológico para su acción en lugar de filtración física. Se construyen cuidadosamente utilizando capas graduadas de arena, con la arena más gruesa, junto con algo de grava, en la parte inferior y la arena más fina en la parte superior. Los desagües en la base transportan el agua tratada para su desinfección. La filtración depende del desarrollo de una fina capa biológica, llamada capa zoogleal o Schmutzdecke , en la superficie del filtro. Un filtro de arena lento eficaz puede permanecer en servicio durante muchas semanas o incluso meses, si el pretratamiento está bien diseñado, y produce agua con un nivel de nutrientes disponibles muy bajo, que los métodos físicos de tratamiento rara vez logran. Los niveles muy bajos de nutrientes permiten enviar agua de forma segura a través de sistemas de distribución con niveles muy bajos de desinfectante, lo que reduce la irritación del consumidor por los niveles ofensivos de cloro y subproductos del cloro. Los filtros de arena lentos no se lavan a contracorriente; se mantienen raspando la capa superior de arena cuando el flujo finalmente se obstruye por el crecimiento biológico. [8]
En la filtración de ribera , los sedimentos naturales de la ribera de un río se utilizan para proporcionar la primera etapa de filtración de contaminantes. Si bien por lo general no están lo suficientemente limpios como para usarse directamente para agua potable, el agua obtenida de los pozos de extracción asociados es mucho menos problemática que el agua del río tomada directamente del río.
Los filtros de membrana se utilizan ampliamente para filtrar tanto agua potable como aguas residuales . En el caso del agua potable, los filtros de membrana pueden eliminar prácticamente todas las partículas de más de 0,2 μm, incluidas Giardia y Cryptosporidium . Los filtros de membrana son una forma eficaz de tratamiento terciario cuando se desea reutilizar el agua para la industria, para fines domésticos limitados o antes de verterla en un río que utilizan las ciudades situadas más abajo. Se utilizan ampliamente en la industria, en particular para la preparación de bebidas (incluida el agua embotellada ). Sin embargo, ninguna filtración puede eliminar sustancias que están realmente disueltas en el agua, como fosfatos , nitratos e iones de metales pesados .
Las membranas de ultrafiltración utilizan membranas de polímero con poros microscópicos formados químicamente que se pueden utilizar para filtrar sustancias disueltas, evitando el uso de coagulantes. El tipo de medio de membrana determina cuánta presión se necesita para hacer pasar el agua y qué tamaños de microorganismos se pueden filtrar. [ cita requerida ]
Intercambio iónico : [9] Los sistemas de intercambio iónico utilizan columnas rellenas de resina de intercambio iónico o zeolita para reemplazar los iones no deseados. El caso más común es el de ablandamiento de agua que consiste en la eliminación de iones Ca 2+ y Mg 2+ reemplazándolos con iones Na + o K + benignos (amigables con el jabón) . Las resinas de intercambio iónico también se utilizan para eliminar iones tóxicos como nitrito , plomo, mercurio , arsénico y muchos otros.
Suavizado precipitativo : [4] : 13,12–13,58 El agua rica en dureza ( iones de calcio y magnesio ) se trata con cal ( óxido de calcio ) y/o carbonato de sodio ( carbonato de sodio ) para precipitar el carbonato de calcio de la solución utilizando el efecto del ión común .
Electrodesionización : [9] El agua pasa entre un electrodo positivo y un electrodo negativo. Las membranas de intercambio iónico permiten que solo los iones positivos migren del agua tratada hacia el electrodo negativo y solo los iones negativos hacia el electrodo positivo. Se produce agua desionizada de alta pureza de forma continua, de forma similar al tratamiento de intercambio iónico. La eliminación completa de iones del agua es posible si se cumplen las condiciones adecuadas. El agua normalmente se trata previamente con una unidad de ósmosis inversa para eliminar contaminantes orgánicos no iónicos y con membranas de transferencia de gas para eliminar el dióxido de carbono . Es posible una recuperación de agua del 99% si la corriente de concentrado se alimenta a la entrada de RO.

La desinfección se lleva a cabo filtrando los microorganismos nocivos y añadiendo productos químicos desinfectantes. El agua se desinfecta para matar cualquier patógeno que pase a través de los filtros y para proporcionar una dosis residual de desinfectante para matar o inactivar microorganismos potencialmente dañinos en los sistemas de almacenamiento y distribución. Los posibles patógenos incluyen virus , bacterias, incluidas Salmonella , Cólera , Campylobacter y Shigella , y protozoos , incluidos Giardia lamblia y otros criptosporidios . Después de la introducción de cualquier agente desinfectante químico, el agua suele almacenarse en un depósito temporal, a menudo llamado tanque de contacto o pozo transparente , para permitir que se complete la acción desinfectante.
El método de desinfección más común implica alguna forma de cloro o sus compuestos, como la cloramina o el dióxido de cloro . El cloro es un oxidante fuerte que mata rápidamente muchos microorganismos dañinos. Debido a que el cloro es un gas tóxico, existe el peligro de una liberación asociada con su uso. Este problema se evita mediante el uso de hipoclorito de sodio , que es una solución relativamente económica utilizada en la lejía doméstica que libera cloro libre cuando se disuelve en agua. Las soluciones de cloro se pueden generar en el sitio mediante la electrolisis de soluciones de sal común. Una forma sólida, el hipoclorito de calcio , libera cloro al contacto con el agua. Sin embargo, la manipulación del sólido requiere un contacto humano más rutinario a través de la apertura de bolsas y el vertido que el uso de cilindros de gas o lejía, que se automatizan más fácilmente. La generación de hipoclorito de sodio líquido es económica y también más segura que el uso de cloro gaseoso o sólido. Los niveles de cloro de hasta 4 miligramos por litro (4 partes por millón) se consideran seguros en el agua potable. [10]
Todas las formas de cloro se utilizan ampliamente, a pesar de sus respectivos inconvenientes. Uno de los inconvenientes es que el cloro de cualquier fuente reacciona con los compuestos orgánicos naturales del agua y forma subproductos químicos potencialmente dañinos. Estos subproductos, trihalometanos (THM) y ácidos haloacéticos (HAA), son cancerígenos en grandes cantidades y están regulados por la Agencia de Protección Ambiental de los Estados Unidos (EPA) y la Inspección de Agua Potable del Reino Unido. La formación de THM y ácidos haloacéticos se puede minimizar mediante la eliminación eficaz de la mayor cantidad posible de compuestos orgánicos del agua antes de agregar el cloro. Aunque el cloro es eficaz para matar bacterias, tiene una eficacia limitada contra los protozoos patógenos que forman quistes en el agua, como Giardia lamblia y Cryptosporidium .
El dióxido de cloro es un desinfectante de acción más rápida que el cloro elemental. Se utiliza con relativa poca frecuencia porque en algunas circunstancias puede crear cantidades excesivas de clorito , que es un subproducto regulado a niveles bajos permitidos en los Estados Unidos. El dióxido de cloro se puede suministrar como una solución acuosa y agregarse al agua para evitar problemas de manipulación del gas; las acumulaciones de gas de dióxido de cloro pueden detonar espontáneamente.
El uso de cloramina como desinfectante es cada vez más común. Aunque la cloramina no es un oxidante tan fuerte, proporciona un residuo más duradero que el cloro libre debido a su menor potencial redox en comparación con este último. Además, no forma fácilmente trihalometanos ni ácidos haloacéticos ( subproductos de la desinfección ).
Es posible convertir el cloro en cloramina añadiendo amoníaco al agua después de añadir cloro. El cloro y el amoníaco reaccionan para formar cloramina. Los sistemas de distribución de agua desinfectados con cloraminas pueden experimentar nitrificación , ya que el amoníaco es un nutriente para el crecimiento bacteriano y los nitratos se generan como subproducto.
El ozono es una molécula inestable que cede fácilmente un átomo de oxígeno, lo que proporciona un potente agente oxidante que es tóxico para la mayoría de los organismos transmitidos por el agua. Es un desinfectante muy potente y de amplio espectro que se utiliza ampliamente en Europa y en algunos municipios de los Estados Unidos y Canadá. La desinfección con ozono, u ozonización, es un método eficaz para inactivar protozoos dañinos que forman quistes. También funciona bien contra casi todos los demás patógenos. El ozono se produce al pasar oxígeno a través de luz ultravioleta o una descarga eléctrica "fría". Para utilizar el ozono como desinfectante, debe crearse en el lugar y agregarse al agua por contacto con burbujas. Algunas de las ventajas del ozono incluyen la producción de menos subproductos peligrosos y la ausencia de problemas de sabor y olor (en comparación con la cloración ). No queda ozono residual en el agua. [11] En ausencia de un desinfectante residual en el agua, se puede agregar cloro o cloramina a lo largo de un sistema de distribución para eliminar cualquier patógeno potencial en las tuberías de distribución.
El ozono se ha utilizado en plantas de agua potable desde 1906, cuando se construyó la primera planta de ozonización industrial en Niza , Francia. La Administración de Alimentos y Medicamentos de los Estados Unidos ha aceptado que el ozono es seguro; y se aplica como un agente antimicrobiológico para el tratamiento, almacenamiento y procesamiento de alimentos. Sin embargo, aunque se forman menos subproductos por ozonización, se ha descubierto que el ozono reacciona con los iones de bromuro en el agua para producir concentraciones del presunto carcinógeno bromato . El bromuro se puede encontrar en suministros de agua dulce en concentraciones suficientes para producir (después de la ozonización) más de 10 partes por mil millones (ppb) de bromato, el nivel máximo de contaminante establecido por la USEPA. [12] La desinfección con ozono también consume mucha energía.

La luz ultravioleta (UV) es muy eficaz para inactivar quistes en aguas con baja turbidez. La eficacia desinfectante de la luz ultravioleta disminuye a medida que aumenta la turbidez, como resultado de la absorción , dispersión y sombreado causados por los sólidos suspendidos. La principal desventaja del uso de la radiación ultravioleta es que, al igual que el tratamiento con ozono, no deja desinfectante residual en el agua; por lo tanto, a veces es necesario agregar un desinfectante residual después del proceso de desinfección primaria. Esto se hace a menudo mediante la adición de cloraminas, analizadas anteriormente como desinfectante primario. Cuando se utilizan de esta manera, las cloraminas proporcionan un desinfectante residual eficaz con muy pocos de los efectos negativos de la cloración.
Más de 2 millones de personas en 28 países en desarrollo utilizan la desinfección solar para el tratamiento diario del agua potable. [13]
Al igual que la radiación ultravioleta, la radiación ionizante (rayos X, rayos gamma y haces de electrones) se ha utilizado para esterilizar el agua. [ cita requerida ]
El bromo y el yodo también se pueden utilizar como desinfectantes. Sin embargo, el cloro en el agua es más de tres veces más eficaz como desinfectante contra Escherichia coli que una concentración equivalente de bromo , y más de seis veces más eficaz que una concentración equivalente de yodo . [14] El yodo se utiliza habitualmente para la purificación de agua portátil , y el bromo es común como desinfectante de piscinas .
Existen dispositivos y métodos portátiles de purificación de agua para su desinfección y tratamiento en situaciones de emergencia o en lugares remotos. La desinfección es el objetivo principal, ya que las consideraciones estéticas, como el sabor, el olor, la apariencia y la contaminación química residual, no afectan la seguridad a corto plazo del agua potable.
A continuación se enumeran otros métodos populares para purificar el agua, especialmente para el suministro privado local. En algunos países, algunos de estos métodos se utilizan para el suministro municipal a gran escala. Particularmente importantes son la destilación ( desalinización del agua de mar ) y la ósmosis inversa.
Llevar el agua a su punto de ebullición (alrededor de 100 °C o 212 F al nivel del mar), es la forma más antigua y efectiva, ya que elimina la mayoría de los microbios que causan enfermedades intestinales , [19] pero no puede eliminar toxinas químicas o impurezas. [20] Para la salud humana, no se requiere la esterilización completa del agua, ya que los microbios resistentes al calor no afectan los intestinos. [19] El consejo tradicional de hervir el agua durante diez minutos es principalmente para mayor seguridad, ya que los microbios comienzan a expirar a temperaturas superiores a 60 °C (140 °F). Aunque el punto de ebullición disminuye con el aumento de la altitud, no es suficiente para afectar la desinfección. [19] [21] En áreas donde el agua es "dura" (es decir, que contiene sales de calcio disueltas significativas), la ebullición descompone los iones de bicarbonato , lo que resulta en una precipitación parcial como carbonato de calcio . Esta es la "pelusa" que se acumula en los elementos de la tetera, etc., en áreas de agua dura. Con excepción del calcio, la ebullición no elimina los solutos con un punto de ebullición más alto que el agua y, de hecho, aumenta su concentración (debido a que parte del agua se pierde en forma de vapor). La ebullición no deja un desinfectante residual en el agua. Por lo tanto, el agua que se hierve y luego se almacena durante un período prolongado puede adquirir nuevos patógenos.
El carbón activado granular es una forma de carbón activado con una gran superficie. Absorbe muchos compuestos, incluidos muchos compuestos tóxicos. El agua que pasa a través del carbón activado se usa comúnmente en regiones municipales con contaminación orgánica, sabor u olores. Muchos filtros de agua domésticos y peceras usan filtros de carbón activado para purificar el agua. Los filtros domésticos para agua potable a veces contienen plata como nanopartículas de plata metálica . Si el agua se mantiene en el bloque de carbón durante períodos más largos, los microorganismos pueden crecer en el interior, lo que provoca incrustaciones y contaminación. Las nanopartículas de plata son un excelente material antibacteriano y pueden descomponer compuestos orgánicos halogenados tóxicos, como pesticidas, en productos orgánicos no tóxicos. [22] El agua filtrada debe usarse poco después de filtrarse, ya que la baja cantidad de microbios restantes puede proliferar con el tiempo. En general, estos filtros domésticos eliminan más del 90% del cloro en un vaso de agua tratada. Estos filtros deben reemplazarse periódicamente, de lo contrario, el contenido bacteriano del agua puede aumentar debido al crecimiento de bacterias dentro de la unidad de filtrado. [11]
La destilación consiste en hervir agua para producir vapor de agua . El vapor entra en contacto con una superficie fría donde se condensa en forma de líquido. Como los solutos normalmente no se vaporizan, permanecen en la solución hirviendo. Ni siquiera la destilación purifica completamente el agua, debido a los contaminantes con puntos de ebullición similares y a las gotitas de líquido no vaporizado que se transportan con el vapor. Sin embargo, se puede obtener agua pura al 99,9 % mediante destilación.
La destilación por membrana de contacto directo (DCMD) hace pasar agua de mar calentada por la superficie de una membrana de polímero hidrófobo . El agua evaporada pasa del lado caliente a través de los poros de la membrana y forma una corriente de agua pura fría en el otro lado. La diferencia de presión de vapor entre el lado caliente y el lado frío ayuda a empujar las moléculas de agua a través de ella.
La ósmosis inversa implica la aplicación de presión mecánica para forzar el paso del agua a través de una membrana semipermeable . Los contaminantes quedan al otro lado de la membrana. La ósmosis inversa es, en teoría, el método más completo de purificación de agua a gran escala disponible, aunque es difícil crear membranas semipermeables perfectas. A menos que las membranas se mantengan bien, las algas y otras formas de vida pueden colonizarlas. [23]
El dióxido de carbono u otro gas de bajo peso molecular se puede mezclar con agua contaminada a alta presión y baja temperatura para formar cristales de hidratos de gas de forma exotérmica. Los hidratos se pueden separar mediante centrifugación o sedimentación. El agua se puede liberar de los cristales de hidratos mediante calentamiento. [24]
La oxidación química in situ (ISCO) es un proceso de oxidación avanzado. Se utiliza para la remediación de suelos y/o aguas subterráneas con el fin de reducir las concentraciones de contaminantes específicos. La ISCO se logra inyectando o introduciendo de otro modo oxidantes en el medio contaminado (suelo o agua subterránea) para destruir los contaminantes. Se puede utilizar para remediar una variedad de compuestos orgánicos, incluidos algunos que son resistentes a la degradación natural.
La biorremediación utiliza microorganismos para eliminar los desechos de un área contaminada. Desde 1991, la biorremediación ha sido una táctica sugerida para eliminar impurezas como alcanos, percloratos y metales. [25] La biorremediación ha tenido éxito porque los percloratos son altamente solubles, lo que los hace difíciles de eliminar. [26] Entre los ejemplos de aplicaciones de la cepa CKB de Dechloromonas agitata se incluyen estudios de campo realizados en Maryland y el suroeste de los EE. UU. [26] [27] [28]
Peróxido de hidrógeno ( H
2Oh
2) es un desinfectante común que puede purificar el agua. Normalmente se produce en plantas químicas y se transporta al agua contaminada. Un enfoque alternativo emplea un catalizador de oro y paladio para sintetizar H
2Oh
2a partir de átomos de hidrógeno y oxígeno ambientales en el lugar de uso. Se informó que este último era más rápido y 10 7 veces más potente para matar Escherichia coli que el H comercial.
2Oh
2, y más de 10 8 veces más eficaz que el cloro. La reacción catalítica también produce especies reactivas de oxígeno (ROS) que se unen y degradan otros compuestos. [29]

En abril de 2007, el suministro de agua de Spencer, Massachusetts , en los Estados Unidos de América, se contaminó con un exceso de hidróxido de sodio (lejía) cuando su equipo de tratamiento funcionó mal. [30]
Muchos municipios han dejado de utilizar cloro libre para utilizar cloramina como agente desinfectante. Sin embargo, la cloramina parece ser un agente corrosivo en algunos sistemas de agua. La cloramina puede disolver la película "protectora" que hay en el interior de las líneas de servicio antiguas, lo que provoca la filtración de plomo en los grifos residenciales. Esto puede provocar una exposición nociva, incluidos niveles elevados de plomo en sangre . El plomo es una neurotoxina conocida . [31]
La destilación elimina todos los minerales del agua, y los métodos de membrana de ósmosis inversa y nanofiltración eliminan la mayoría o todos los minerales. Esto da como resultado agua desmineralizada que no se considera agua potable ideal . La Organización Mundial de la Salud ha investigado los efectos sobre la salud del agua desmineralizada desde 1980. [32] Los experimentos en humanos encontraron que el agua desmineralizada aumentó la diuresis y la eliminación de electrolitos , con una disminución de la concentración de potasio en el suero sanguíneo . El magnesio , el calcio y otros minerales en el agua pueden ayudar a proteger contra la deficiencia nutricional. El agua desmineralizada también puede aumentar el riesgo de metales tóxicos porque lixivia más fácilmente materiales de las tuberías como el plomo y el cadmio, lo que se previene con minerales disueltos como el calcio y el magnesio. El agua con bajo contenido mineral se ha relacionado con casos específicos de envenenamiento por plomo en bebés, cuando el plomo de las tuberías se filtró a tasas especialmente altas en el agua. Las recomendaciones para el magnesio se han establecido en un mínimo de 10 mg/L con 20-30 mg/L óptimo; Para el calcio, un mínimo de 20 mg/L y un óptimo de 40–80 mg/L, y una dureza total del agua (añadiendo magnesio y calcio) de 2 a 4 mmol /L. Con una dureza del agua superior a 5 mmol/L, se ha observado una mayor incidencia de cálculos biliares, cálculos renales, cálculos urinarios, artrosis y artropatías. [33] Además, los procesos de desalinización pueden aumentar el riesgo de contaminación bacteriana. [33]
Los fabricantes de destiladores de agua domésticos afirman lo contrario: que los minerales del agua son la causa de muchas enfermedades y que la mayoría de los minerales beneficiosos provienen de los alimentos, no del agua. [34] [35]

Los primeros experimentos sobre filtración de agua se realizaron en el siglo XVII. Sir Francis Bacon intentó desalinizar el agua del mar haciendo pasar el flujo a través de un filtro de arena . Aunque su experimento no tuvo éxito, marcó el comienzo de un nuevo interés en el campo. Los padres de la microscopía , Antonie van Leeuwenhoek y Robert Hooke , utilizaron el microscopio recién inventado para observar por primera vez pequeñas partículas de material que se encontraban suspendidas en el agua, sentando las bases para la futura comprensión de los patógenos transmitidos por el agua. [36]
El primer uso documentado de filtros de arena para purificar el suministro de agua data de 1804, cuando el propietario de una blanqueadora en Paisley, Escocia , John Gibb, instaló un filtro experimental, vendiendo su excedente no deseado al público. [37] Este método fue refinado en las dos décadas siguientes por ingenieros que trabajaban para compañías de agua privadas, y culminó en el primer suministro público de agua tratada del mundo, instalado por el ingeniero James Simpson para la Chelsea Waterworks Company en Londres en 1829. [38] Esta instalación proporcionó agua filtrada para todos los residentes de la zona, y el diseño de la red fue ampliamente copiado en todo el Reino Unido en las décadas siguientes.
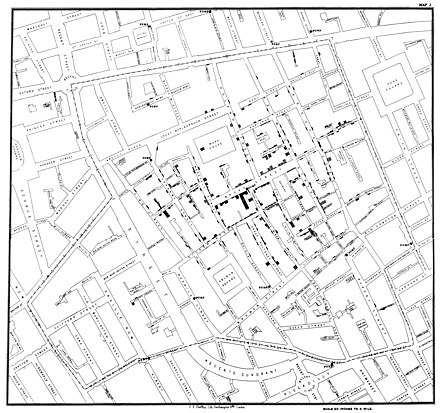
La práctica del tratamiento del agua pronto se convirtió en algo común y corriente, y las virtudes del sistema se hicieron evidentes después de las investigaciones del médico John Snow durante el brote de cólera de Broad Street en 1854. Snow era escéptico ante la teoría del miasma , entonces dominante , que afirmaba que las enfermedades eran causadas por "aires malos" nocivos. Aunque la teoría de los gérmenes de la enfermedad aún no se había desarrollado, las observaciones de Snow lo llevaron a descartar la teoría predominante. Su ensayo de 1855 Sobre el modo de comunicación del cólera demostró de manera concluyente el papel del suministro de agua en la propagación de la epidemia de cólera en Soho , [39] [40] con el uso de un mapa de distribución de puntos y una prueba estadística para ilustrar la conexión entre la calidad de la fuente de agua y los casos de cólera. Sus datos convencieron al consejo local de desactivar la bomba de agua, lo que rápidamente puso fin al brote.
La Ley del Agua Metropolitana introdujo la regulación de las compañías de suministro de agua en Londres, incluyendo estándares mínimos de calidad del agua por primera vez. La Ley "estableció disposiciones para asegurar el suministro a la Metrópolis de agua pura y saludable", y requirió que toda el agua fuera "efectivamente filtrada" a partir del 31 de diciembre de 1855. [41] Esto fue seguido por una legislación para la inspección obligatoria de la calidad del agua, incluyendo análisis químicos exhaustivos, en 1858. Esta legislación sentó un precedente mundial para intervenciones estatales de salud pública similares en toda Europa. La Comisión Metropolitana de Alcantarillados se formó al mismo tiempo, la filtración de agua se adoptó en todo el país y se establecieron nuevas tomas de agua en el Támesis por encima de la esclusa de Teddington . Los filtros de presión automáticos, donde el agua es forzada bajo presión a través del sistema de filtración, fueron innovados en 1899 en Inglaterra. [37]
John Snow fue el primero en utilizar con éxito cloro para desinfectar el suministro de agua del Soho que había contribuido a propagar el brote de cólera. William Soper también utilizó cal clorada para tratar las aguas residuales producidas por pacientes con fiebre tifoidea en 1879.
En un artículo publicado en 1894, Moritz Traube propuso formalmente la adición de cloruro de cal ( hipoclorito de calcio ) al agua para dejarla "libre de gérmenes". Otros dos investigadores confirmaron los hallazgos de Traube y publicaron sus artículos en 1895. [42] Los primeros intentos de implementar la cloración del agua en una planta de tratamiento de agua se realizaron en 1893 en Hamburgo , Alemania y en 1897 la ciudad de Maidstone , Inglaterra, fue la primera en tener todo su suministro de agua tratado con cloro. [43]
La cloración permanente del agua comenzó en 1905, cuando un filtro lento de arena defectuoso y un suministro de agua contaminada provocaron una grave epidemia de fiebre tifoidea en Lincoln, Inglaterra . [44] Alexander Cruickshank Houston utilizó la cloración del agua para detener la epidemia. Su instalación alimentó el agua que se estaba tratando con una solución concentrada de cloruro de cal. La cloración del suministro de agua ayudó a detener la epidemia y, como precaución, la cloración continuó hasta 1911, cuando se instituyó un nuevo suministro de agua. [45]

El primer uso continuo de cloro en los Estados Unidos para la desinfección tuvo lugar en 1908 en el embalse de Boonton (en el río Rockaway ), que servía como suministro para la ciudad de Jersey, Nueva Jersey . [46] La cloración se lograba mediante adiciones controladas de soluciones diluidas de cloruro de cal ( hipoclorito de calcio ) en dosis de 0,2 a 0,35 ppm. El proceso de tratamiento fue concebido por John L. Leal y la planta de cloración fue diseñada por George Warren Fuller. [47] Durante los siguientes años, la desinfección con cloro utilizando cloruro de cal se instaló rápidamente en los sistemas de agua potable de todo el mundo. [48]
La técnica de purificación del agua potable mediante el uso de gas cloro licuado comprimido fue desarrollada por un oficial británico del Servicio Médico de la India , Vincent B. Nesfield, en 1903. Según su propio relato:
Se me ocurrió que el gas de cloro podría resultar satisfactorio... si se pudieran encontrar medios adecuados para utilizarlo... La siguiente cuestión importante era cómo hacer que el gas fuera portátil. Esto se podía lograr de dos maneras: licuándolo y almacenándolo en recipientes de hierro revestidos de plomo, que tuvieran un chorro con un canal capilar muy fino y provistos de un grifo o una tapa de rosca. Se abre el grifo y se coloca el cilindro en la cantidad de agua necesaria. El cloro burbujea y en diez o quince minutos el agua es absolutamente segura. Este método sería útil a gran escala, como para los carros de agua de servicio. [49]
El mayor del ejército estadounidense Carl Rogers Darnall , profesor de química en la Escuela de Medicina del Ejército , dio la primera demostración práctica de esto en 1910. Poco después, el mayor William JL Lyster del Departamento Médico del Ejército utilizó una solución de hipoclorito de calcio en una bolsa de lino para tratar el agua. Durante muchas décadas, el método de Lyster siguió siendo el estándar para las fuerzas terrestres estadounidenses en el campo y en los campamentos, implementado en la forma de la conocida bolsa Lyster (también escrita bolsa Lister). La bolsa estaba hecha de lona y podía contener 36 galones de agua. Era porosa y se sostenía con cuerdas, purificando el agua con la ayuda de una solución de hipoclorito de calcio. Cada bolsa tenía un grifo adjunto, que se usaba para hacer correr el agua para las pruebas, así como para dispensarla para su uso. Esto se convirtió en la base de los sistemas actuales de purificación de agua municipal . [50]
Según un informe de la Organización Mundial de la Salud (OMS) de 2007, 1.100 millones de personas carecen de acceso a un suministro mejorado de agua potable ; el 88% de los 4.000 millones de casos anuales de enfermedades diarreicas se atribuyen al agua insalubre y a un saneamiento e higiene inadecuados, mientras que 1,8 millones de personas mueren cada año por enfermedades diarreicas . La OMS estima que el 94% de estos casos de enfermedades diarreicas se pueden prevenir mediante modificaciones del medio ambiente, incluido el acceso a agua potable. [51] Técnicas sencillas para tratar el agua en el hogar, como la cloración, los filtros y la desinfección solar, y para almacenarla en contenedores seguros podrían salvar una enorme cantidad de vidas cada año. [52] Reducir las muertes por enfermedades transmitidas por el agua es un objetivo importante de salud pública en los países en desarrollo.
El mercado mundial de purificación de agua tiene un valor de 22 mil millones de dólares. [53] Los filtros y purificadores de agua domésticos son comunes en la India. [54]
