Las topoisomerasas de tipo II son topoisomerasas que cortan ambas hebras de la hélice de ADN simultáneamente para gestionar los ovillos y superenrollamientos de ADN . Utilizan la hidrólisis de ATP , a diferencia de la topoisomerasa de tipo I. En este proceso, estas enzimas cambian el número de enlace del ADN circular en ±2. Las topoisomerasas son enzimas ubicuas, que se encuentran en todos los organismos vivos. [1]
En los animales, la topoisomerasa II es un objetivo de la quimioterapia. En los procariotas, la girasa es un objetivo antibacteriano. [2] De hecho, estas enzimas son de interés por una amplia gama de efectos.
Las topoisomerasas de tipo II aumentan o disminuyen el número de enlace de un bucle de ADN en 2 unidades y promueven el desenredo de los cromosomas. Por ejemplo, la ADN girasa , una topoisomerasa de tipo II observada en E. coli y la mayoría de los demás procariotas , introduce superenrollamientos negativos y disminuye el número de enlace en 2. La girasa también puede eliminar nudos del cromosoma bacteriano . Junto con la girasa, la mayoría de los procariotas también contienen una segunda topoisomerasa de tipo IIA, denominada topoisomerasa IV. La girasa y la topoisomerasa IV se diferencian por sus dominios C-terminales, que se cree que dictan la especificidad del sustrato y la funcionalidad de estas dos enzimas. La huella indica que la girasa, que forma una huella de 140 pares de bases y envuelve el ADN, introduce superenrollamientos negativos , mientras que la topoisomerasa IV, que forma una huella de 28 pares de bases, no envuelve el ADN.
La topoisomerasa eucariota tipo II no puede introducir superenrollamientos; sólo puede relajarlos.
Las funciones de las topoisomerasas de tipo IIB son menos conocidas. A diferencia de las topoisomerasas de tipo IIA, las topoisomerasas de tipo IIB no pueden simplificar la topología del ADN (ver a continuación), pero comparten varias características estructurales con las topoisomerasas de tipo IIA.
Las topoisomerasas de tipo IIA son esenciales en la separación de las hebras hijas enredadas durante la replicación. Se cree que esta función la realiza la topoisomerasa II en eucariotas y la topoisomerasa IV en procariotas. Si no se separan estas hebras, se produce la muerte celular. Las topoisomerasas de tipo IIA tienen la capacidad especial de relajar el ADN a un estado inferior al del equilibrio termodinámico, una característica que no tienen las topoisomerasas de tipo IA, IB y IIB. Esta capacidad, conocida como simplificación topológica, fue identificada por primera vez por Rybenkov et al. [3] La hidrólisis del ATP impulsa esta simplificación, pero aún falta un mecanismo molecular claro para esta simplificación. Se han propuesto varios modelos para explicar este fenómeno, incluidos dos modelos que se basan en la capacidad de las topoisomerasas de tipo IIA para reconocer dúplex de ADN doblados. [4] La bioquímica, la microscopía electrónica y las estructuras recientes de la topoisomerasa II unida al ADN revelan que las topoisomerasas de tipo IIA se unen a los vértices del ADN, lo que respalda este modelo.
Hay dos subclases de topoisomerasas tipo II, tipo IIA y IIB.
Algunos organismos, incluidos los humanos, tienen dos isoformas de la topoisomerasa II: alfa y beta . En los cánceres , la topoisomerasa IIα se expresa en gran medida en las células en proliferación. En ciertos cánceres, como los tumores de la vaina de los nervios periféricos, la alta expresión de su proteína codificada también se asocia a una baja supervivencia del paciente.
Las dos clases de topoisomerasas poseen un mecanismo de paso de cadena y una estructura de dominio similares (ver más abajo), sin embargo también tienen varias diferencias importantes. Las topoisomerasas de tipo IIA forman roturas de doble cadena con salientes de cuatro pares de bases, mientras que las topoisomerasas de tipo IIB forman roturas de doble cadena con salientes de dos bases. [6] Además, las topoisomerasas de tipo IIA pueden simplificar la topología del ADN, [3] mientras que las topoisomerasas de tipo IIB no lo hacen. [7]
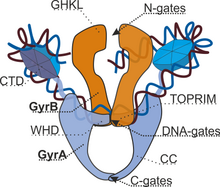
Las topoisomerasas de tipo IIA constan de varios motivos clave:
Las topoisomerasas eucariotas de tipo II son homodímeras (A 2 ), mientras que las topoisomerasas procariotas de tipo II son heterotetrámeras (A 2 B 2 ). Los procariotas tienen el dominio ATPasa y el pliegue Toprim en un polipéptido ( Pfam PF00204), mientras que el núcleo de escisión del ADN y el CTD se encuentran en un segundo polipéptido ( Pfam PF00521). Para la girasa, el primer polipéptido se llama GyrB y el segundo polipéptido se llama GyrA. Para la topo IV, el primer polipéptido se llama ParE y el segundo polipéptido se llama ParC. Ambas firmas Pfam se encuentran en la topoisomerasa eucariota de cadena sencilla.
Las estructuras del dominio ATPasa N-terminal de la girasa [8] y la topoisomerasa II de la levadura [9] se han resuelto en complejo con AMPPNP (un análogo de ATP), lo que demuestra que dos dominios ATPasa se dimerizan para formar una conformación cerrada. En el caso de la girasa, la estructura tiene un agujero sustancial en el medio, que se supone que aloja el segmento T.
El dominio ATPasa se conecta al pliegue Toprim mediante un elemento helicoidal conocido como dominio transductor. Se cree que este dominio comunica el estado del nucleótido del dominio ATPasa al resto de la proteína. Las modificaciones de este dominio afectan la actividad de la topoisomerasa, y el trabajo estructural realizado por el grupo Verdine muestra que el estado de ATP afecta la orientación del dominio transductor. [10]
El núcleo central de la proteína contiene un pliegue Toprim y un núcleo de unión al ADN que contiene un dominio de hélice alada (WHD), a menudo denominado dominio CAP, ya que se identificó por primera vez que se parecía al WHD de la proteína activadora de catabolito. La tirosina catalítica se encuentra en este WHD. El pliegue Toprim es un pliegue de Rossmann que contiene tres residuos ácidos invariantes que coordinan los iones de magnesio involucrados en la escisión del ADN y la religación del ADN. [11] La estructura del pliegue Toprim y el núcleo de unión al ADN de la topoisomerasa II de levadura fue resuelta por primera vez por Berger y Wang, [12] y el primer núcleo de unión al ADN de la girasa fue resuelto por Morais Cabral et al. [13] La estructura resuelta por Berger reveló importantes conocimientos sobre la función de la enzima. El núcleo de unión al ADN consta del WHD, que conduce a un dominio de torre. Una región de hélice superenrollada conduce a un dominio C-terminal que forma la interfaz principal del dímero para este estado cristalino (a menudo denominado C-gate). Mientras que la estructura original de la topoisomerasa II muestra una situación en la que los WHD están separados por una gran distancia, la estructura de la girasa muestra una conformación cerrada, en la que los WHD se cierran.
El núcleo de la topoisomerasa II se resolvió posteriormente en nuevas conformaciones, incluida una de Fass et al. [14] y otra de Dong et al. [15] . La estructura de Fass muestra que el dominio Toprim es flexible y que esta flexibilidad puede permitir que el dominio Toprim se coordine con el WHD para formar un complejo de escisión competente. Esto fue finalmente corroborado por la estructura de Dong et al. que se resolvió en presencia de ADN. Esta última estructura mostró que el dominio Toprim y el WHD formaban un complejo de escisión muy similar al de las topoisomerasas de tipo IA e indicó cómo se podía desacoplar la unión y la escisión del ADN, y la estructura mostró que el ADN se doblaba ~150 grados a través de una isoleucina invariante (en la topoisomerasa II es I833 y en la girasa es I172). Este mecanismo de doblado se parece mucho al del factor de integración del huésped (IHF) y HU, dos proteínas arquitecturales en bacterias. Además, mientras que las estructuras anteriores del núcleo de unión del ADN tenían la puerta C cerrada, esta estructura capturó la puerta abierta, un paso clave en el mecanismo de dos puertas (ver a continuación).
Más recientemente, se han resuelto varias estructuras de la estructura unida al ADN en un intento de comprender tanto el mecanismo químico de la escisión del ADN como la base estructural de la inhibición de la topoisomerasa por venenos antibacterianos. La primera arquitectura completa de la ADN girasa de E. coli se ha resuelto mediante criomicroscopía electrónica con una resolución cercana a la atómica. [16] El complejo de nucleoproteína se capturó con un dúplex largo de ADN y gepotidacina , un nuevo inhibidor de la topoisomerasa bacteriana.
La región C-terminal de las topoisomerasas procariotas ha sido resuelta para múltiples especies. La primera estructura de un dominio C-terminal de girasa fue resuelta por Corbett et al. [17] y el dominio C-terminal de la topoisomerasa IV fue resuelto por Corbett et al. [7] Las estructuras formaron un nuevo barril beta, que dobla el ADN envolviendo el ácido nucleico alrededor de sí mismo. La curvatura del ADN por girasa ha sido propuesta como un mecanismo clave en la capacidad de la girasa para introducir superenrollamientos negativos en el ADN. Esto es consistente con los datos de huellas que muestran que la girasa tiene una huella de 140 pares de bases. Tanto los CTD de girasa como de topoisomerasa IV doblan el ADN, pero solo la girasa introduce superenrollamientos negativos.
A diferencia de la función del dominio C-terminal de las topoisomerasas procariotas, la función de la región C-terminal de la topoisomerasa II eucariota aún no está clara. Los estudios han sugerido que esta región está regulada por fosforilación y que esto modula la actividad de la topoisomerasa, sin embargo, es necesario realizar más investigaciones para investigar esto.
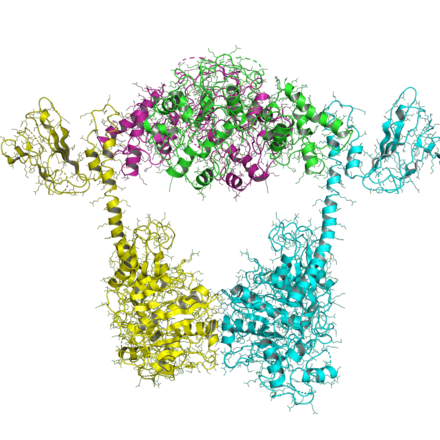
La organización de las topoisomerasas de tipo IIB es similar a la de las de tipo IIA, excepto que todas las de tipo IIB tienen dos genes y forman heterotetrámeros. Un gen, denominado topo VI-B (ya que se parece a gyrB), contiene el dominio ATPasa, un dominio transductor ( Pfam PF09239) y un dominio H2TH similar al pliegue de Ig C-terminal ( Pfam PF18000). El segundo gen, denominado topo VI-A ( Pfam PF04406), contiene el WHD y el dominio Toprim.
El dominio ATPasa de topo VI B se resolvió en múltiples estados de nucleótidos. [18] Se parece mucho al del dominio GHKL de topo II y MutL y muestra que el estado del nucleótido (ADP versus ATP) afecta la orientación del dominio transductor (y 1MX0).
La estructura del topo VI-A fue resuelta por Bergerat et al. [19] mostrando que el pliegue HTH y Toprim tenía una conformación novedosa en comparación con la del topo IIA.
Recientemente se ha resuelto una estructura del complejo topo VI A/B, que muestra una conformación abierta y cerrada, dos estados que se predicen en el mecanismo de dos compuertas (véase más abajo). Estas estructuras, de las cuales una es una estructura cristalina de rayos X y la otra es una reconstrucción de dispersión de rayos X de ángulo pequeño (SAXS), muestran que el dominio de la ATPasa puede ser abierto o cerrado. [20]
La topoisomerasa tipo IIA opera a través de un mecanismo de "dos puertas" (aunque esta es una notación histórica), un mecanismo respaldado por la bioquímica [21] así como por el trabajo estructural. [22]
Una hebra de ADN, llamada puerta o segmento G, está unida por una puerta central de unión al ADN (puerta ADN). Una segunda hebra de ADN, llamada transporte o segmento T, es capturada por la dimerización del dominio ATPasa N-terminal (la puerta ATPasa) cuando se unen dos moléculas de ATP. La hidrólisis del ATP y la liberación de un fosfato inorgánico conducen a la escisión del segmento G, ya que las tirosinas catalíticas forman un enlace covalente de fosfotirosina con el extremo 5' del ADN. Esto crea un saliente de cuatro bases y una rotura de doble cadena en el segmento G. A medida que la puerta de unión al ADN se separa, el segmento T se transfiere a través del segmento G. El segmento G se sella, lo que lleva a que la puerta C-terminal (o puerta C) se abra, lo que permite la liberación del segmento T. La liberación del producto ADP provoca un reinicio del sistema y permite capturar un segundo segmento T.
Las topoisomerasas de tipo IIB funcionan de manera similar, excepto que la proteína forma un saliente de dos bases en el segmento G y la puerta C-terminal falta por completo.
En el mecanismo de paso de cadena, la escisión del ADN es clave para permitir que el segmento T pase a través del segmento G. El mecanismo de escisión del ADN por las topoisomerasas de tipo IIA ha sido recientemente el foco de muchos estudios de biología estructural y bioquímica.
La concatenación es el proceso por el cual dos cadenas circulares de ADN se unen entre sí como eslabones de una cadena. Esto ocurre después de la replicación del ADN, donde dos cadenas simples se concatenan y aún pueden replicarse pero no pueden separarse en las dos células hijas. Como las topoisomerasas de tipo II rompen una doble cadena, pueden fijar este estado (las topoisomerasas de tipo I podrían hacer esto solo si ya hubiera una muesca en la cadena simple), y el número correcto de cromosomas puede permanecer en las células hijas. El ADN lineal en eucariotas es tan largo que puede considerarse sin extremos; las topoisomerasas de tipo II son necesarias por la misma razón.
Las moléculas pequeñas que atacan a la topoisomerasa tipo II se dividen en dos clases: inhibidores y venenos. Debido a su frecuente presencia en células eucariotas en proliferación, los inhibidores de la topoisomerasa tipo II han sido ampliamente estudiados y utilizados como medicamentos contra el cáncer. [23]
El fármaco antitumoral experimental m-AMSA (4'-(9'-acridinilamino)metanosulfon-m-anisidide) también inhibe la topoisomerasa tipo 2. [24]
Los venenos de topoisomerasa se han utilizado ampliamente como terapias anticáncer y antibacterianas. Si bien los compuestos antibacterianos como la ciprofloxacina actúan sobre la girasa bacteriana, no inhiben las topoisomerasas eucariotas de tipo IIA. Además, las bacterias resistentes a los fármacos suelen tener una mutación puntual en la girasa (serina79alanina en E. coli ) que hace que las quinolonas sean ineficaces. [ cita requerida ] Estudios estructurales recientes han llevado al descubrimiento de un compuesto que ya no depende de este residuo y, por lo tanto, tiene eficacia contra las bacterias resistentes a los fármacos. [ cita requerida ]
La girasa T4 del bacteriófago (fago) (topoismerasa tipo II) es una proteína multisubunidad que consiste en los productos de los genes 39, 52 y probablemente 60. [25] [26] Cataliza la relajación del ADN superhelicoidal negativo o positivo y se emplea en la replicación del ADN del fago durante la infección del huésped bacteriano E. coli . [27] La proteína del gen 52 del fago comparte homología con la subunidad gyrA de la girasa de E. coli [28] y la proteína del gen 39 del fago comparte homología con la subunidad gyr B. [29] Dado que la girasa del ADN del huésped E. coli puede compensar parcialmente la pérdida de los productos del gen T4 del fago, los mutantes defectuosos en los genes 39, 52 o 60 no eliminan por completo la replicación del ADN del fago, sino que retrasan su inicio. [27] La tasa de elongación del ADN no es más lenta que la del tipo salvaje en tales infecciones mutantes. [30] Los mutantes defectuosos en los genes 39, 52 o 60 muestran una recombinación genética aumentada , así como una mutación por sustitución de bases y deleción aumentada , lo que sugiere que la síntesis de ADN compensada por el huésped es menos precisa que la dirigida por el fago de tipo salvaje. [31] Un mutante defectuoso en el gen 39 muestra una mayor sensibilidad a la inactivación por irradiación ultravioleta durante la etapa de infección del fago después del inicio de la replicación del ADN cuando están presentes múltiples copias del cromosoma del fago . [32] Los mutantes defectuosos en los genes 39, 52 y 60 tienen una capacidad reducida para llevar a cabo la reactivación por multiplicidad, una forma de reparación recombinatoria que puede tratar diferentes tipos de daño del ADN. [33] La girasa especificada por el genoma de E. coli no infectada también parece participar en la reparación recombinatoria al proporcionar un punto de inicio para el intercambio de cadena recíproca impulsado por la proteína RecA. [34]
{{cite book}}: Mantenimiento de CS1: falta la ubicación del editor ( enlace )