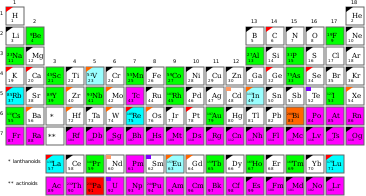
Un elemento monoisotópico es un elemento que tiene un solo isótopo estable (nucleido). Existen 26 elementos de este tipo, como se indica a continuación.
La estabilidad se define experimentalmente para los elementos químicos, ya que hay una serie de nucleidos estables con números atómicos superiores a ~ 40 que son teóricamente inestables, pero aparentemente tienen vidas medias tan largas que no se ha observado ni directa ni indirectamente (a partir de la medición de productos) su desintegración.
Los elementos monoisotópicos se caracterizan, excepto en un caso, por un número impar de protones ( Z impar ) y un número par de neutrones. Debido a la ganancia de energía por apareamiento nuclear, el número impar de protones imparte inestabilidad a los isótopos de un Z impar , lo que en los elementos más pesados requiere un conjunto de neutrones completamente emparejado para compensar esta tendencia hacia la estabilidad. (Los cinco nucleidos estables con Z impar y número impar de neutrones son hidrógeno-2, litio-6, boro-10, nitrógeno-14 y tantalio-180m1).
La única excepción monoisotópica a la regla Z impar es el berilio; su único isótopo estable y primordial, el berilio-9, tiene 4 protones y 5 neutrones. Este elemento no puede tener un isótopo estable con igual número de neutrones y protones ( berilio-8 , con 4 de cada uno) debido a su inestabilidad hacia la desintegración alfa , que se ve favorecida debido a la unión extremadamente estrecha de los núcleos de helio-4 . No puede tener un isótopo estable con 4 protones y 6 neutrones debido al gran desajuste en la relación protón/neutrón para un elemento tan ligero. (Sin embargo, el berilio-10 tiene una vida media de 1,36 millones de años, que es demasiado corta para ser primordial , pero aún así indica una estabilidad inusual para un isótopo ligero con tal desequilibrio).
El conjunto de elementos monoisotópicos se superpone pero no es el mismo que el conjunto de 21 elementos mononucleídicos , que se caracterizan por tener esencialmente un solo isótopo (nucleido) encontrado en la naturaleza. [1] La razón de esto es la aparición de ciertos nucleidos primordiales radiactivos de larga duración en la naturaleza, que pueden formar mezclas con los monoisotópicos y, por lo tanto, evitar que sean naturalmente mononucleídicos. Esto sucede en los casos de siete de los elementos monoisotópicos. Estos isótopos son monoisotópicos, pero debido a la presencia del nucleido primordial radiactivo de larga duración, no son mononucleídicos. Estos elementos son vanadio , rubidio , indio , lantano , europio , lutecio y renio . Para el indio y el renio, el radionucleido de larga duración es en realidad el isótopo más abundante en la naturaleza, y el isótopo estable es menos abundante.
En otros dos casos ( bismuto [2] y protactinio ) se encuentran elementos mononucleídicos que no son monoisotópicos porque el nucleido natural es radiactivo y, por lo tanto, el elemento no tiene ningún isótopo estable. Para que un elemento sea monoisotópico, debe tener un nucleido estable.
Los elementos no mononucleídicos están marcados con un asterisco y se indica el radioisótopo primordial de larga duración . En dos casos (indio y renio), el isótopo natural más abundante es el ligeramente radiactivo y, en el caso del europio, casi la mitad.