La síntesis de indol de Gassman es una serie de reacciones químicas utilizadas para sintetizar indoles sustituidos mediante la adición de una anilina y una cetona que lleva un sustituyente tioéter.

Esta es una reacción química que se lleva a cabo en un solo paso y ninguno de los intermediarios está aislado. R 1 puede ser hidrógeno o alquilo , mientras que R 2 funciona mejor con arilo , pero también puede ser alquilo. Las anilinas ricas en electrones, como la 4-metoxianilina, tienden a fallar en esta reacción.
El grupo tiometilo en la posición 3 a menudo se elimina usando níquel Raney para dar el 3-H-indol.
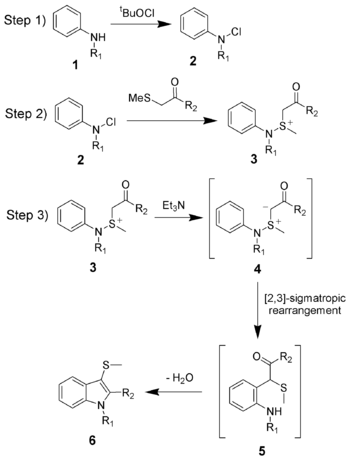
El mecanismo de reacción de la síntesis de indol de Gassman se divide en tres pasos.
El primer paso es la oxidación de la anilina 1 usando hipoclorito de terc -butilo (tBuOCl) para dar la cloramina 2 .
El segundo paso es la adición del ceto-tioéter para obtener el ion sulfonio 3 , y normalmente se realiza a bajas temperaturas (−78 °C).
El tercer y último paso es la adición de una base , que en este caso es trietilamina . Al calentarse a temperatura ambiente, la base desprotonará el ion sulfonio creando el iluro de sulfonio 4 , que experimenta rápidamente una transposición sigmatrópica [2,3] para dar la cetona 5. La cetona 5 experimentará una condensación fácil para dar el 3-tiometilindol deseado 6 .