La síntesis de indol de Bartoli ( también llamada reacción de Bartoli ) es la reacción química de nitroarenos y nitrosarenos ortosustituidos con reactivos vinílicos de Grignard para formar indoles sustituidos . [2] [3] [4] [5]
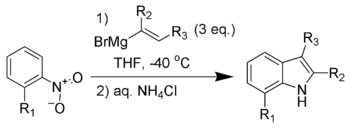
La reacción a menudo no tiene éxito sin una sustitución orto con respecto al grupo nitro, y los sustituyentes orto más voluminosos generalmente dan como resultado mayores rendimientos de la reacción. La masa estérica del grupo orto contribuye al reordenamiento [3,3]-sigmatrópico necesario para la formación del producto. Se necesitan tres equivalentes del reactivo vinílico de Grignard para que la reacción logre una conversión completa cuando se realiza con nitroarenos, y sólo dos equivalentes cuando se realiza con nitrosoarenos.
Este método se ha convertido en una de las rutas más cortas y flexibles hacia los indoles 7 sustituidos. [6] [7] La síntesis de indol de Leimgruber-Batcho proporciona flexibilidad y regioespecificidad similares a los derivados del indol. Una ventaja de la síntesis de indol de Bartoli es la capacidad de producir indoles sustituidos tanto en el anillo carbocíclico como en el anillo pirrol , lo cual es difícil de hacer con la síntesis de indol de Leimgruber-Batcho.
El mecanismo de reacción [8] de la síntesis del indol de Bartoli se ilustra a continuación utilizando o-nitrotolueno ( 1 ) y propenil Grignard ( 2 ) para formar 3,7-dimetilindol ( 13 ).

El mecanismo comienza con la adición del reactivo de Grignard ( 2 ) al nitroareno ( 1 ) para formar el intermedio 3 . El intermedio 3 se descompone espontáneamente para formar un nitrosoareno ( 4 ) y una sal de magnesio ( 5 ). (Al finalizar la reacción, la sal de magnesio liberará un compuesto carbonílico ( 6 ).) La reacción del nitrosoareno ( 4 ) con un segundo equivalente del reactivo de Grignard ( 2 ) forma el intermedio 7 . La masa estérica del grupo orto provoca un reordenamiento [3,3]-sigmatrópico que forma el intermedio 8 . La ciclación y la tautomerización dan el intermedio 10 , que reaccionará con un tercer equivalente del reactivo de Grignard ( 2 ) para dar una sal de indol de dimagnesio ( 12 ). El análisis de la reacción elimina el agua y proporciona el indol final deseado ( 13 ).
Por lo tanto, son necesarios tres equivalentes del reactivo de Grignard, ya que un equivalente se convierte en el compuesto carbonílico 6 , un equivalente desprotona 10 formando un alqueno ( 11 ) y un equivalente se incorpora al anillo de indol.
El intermedio nitroso ( 4 ) ha sido aislado de la reacción. Además, la reacción del intermedio nitroso ( 4 ) con dos equivalentes del reactivo de Grignard produce el indol esperado.
El alcance de la reacción incluye piridinas sustituidas que pueden usarse para producir 4-azaindoles (izquierda) y 6-azaindoles (derecha). [9]
Adrian Dobbs mejoró enormemente el alcance de la síntesis del indol de Bartoli mediante el uso de un ortobromo como grupo director, que posteriormente se elimina mediante AIBN e hidruro de tributilestaño . [10]
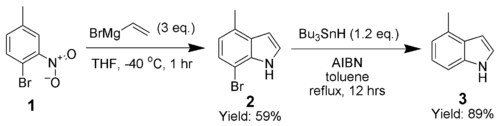
La síntesis de 4-metilindol ( 3 ) resalta la capacidad de esta técnica para producir indoles altamente sustituidos.