La resistencia genética humana a la malaria se refiere a cambios heredados en el ADN de los seres humanos que aumentan la resistencia a la malaria y dan como resultado una mayor supervivencia de los individuos con esos cambios genéticos. La existencia de estos genotipos se debe probablemente a la presión evolutiva ejercida por los parásitos del género Plasmodium que causan la malaria. Dado que la malaria infecta a los glóbulos rojos , estos cambios genéticos son alteraciones más comunes de las moléculas esenciales para la función de los glóbulos rojos (y, por lo tanto, la supervivencia del parásito), como la hemoglobina u otras proteínas celulares o enzimas de los glóbulos rojos. Estas alteraciones generalmente protegen a los glóbulos rojos de la invasión por parásitos Plasmodium o de la replicación de parásitos dentro del glóbulo rojo.
Estos cambios hereditarios en la hemoglobina u otras proteínas características, que son características críticas y bastante invariables de la bioquímica de los mamíferos, suelen causar algún tipo de enfermedad hereditaria. Por lo tanto, se los suele denominar con los nombres de los trastornos sanguíneos asociados a ellos, como la anemia de células falciformes , la talasemia , la deficiencia de glucosa-6-fosfato deshidrogenasa y otros. Estos trastornos sanguíneos causan un aumento de la morbilidad y la mortalidad en áreas del mundo donde la malaria es menos prevalente.
Los parásitos microscópicos , como los virus, los protozoos que causan la malaria y otros, no pueden replicarse por sí solos y dependen de un huésped para continuar sus ciclos de vida. Se replican invadiendo las células del huésped y usurpando la maquinaria celular para replicarse a sí mismos. Finalmente, la replicación descontrolada hace que las células exploten, matando a las células y liberando los organismos infecciosos en el torrente sanguíneo, donde pueden infectar a otras células. A medida que las células mueren y los productos tóxicos de la replicación del organismo invasor se acumulan, aparecen los síntomas de la enfermedad. Debido a que este proceso involucra proteínas específicas producidas por el organismo infeccioso, así como por la célula huésped, incluso un cambio muy pequeño en una proteína crítica puede dificultar o imposibilitar la infección. Dichos cambios pueden surgir por un proceso de mutación en el gen que codifica la proteína. Si el cambio se produce en el gameto, es decir, el espermatozoide o el óvulo que se unen para formar un cigoto que crece hasta convertirse en un ser humano, la mutación protectora se heredará. Dado que las enfermedades letales matan a muchas personas que carecen de mutaciones protectoras, con el tiempo, muchas personas en regiones donde las enfermedades letales son endémicas llegan a heredar mutaciones protectoras. [ cita requerida ]
Cuando el parásito P. falciparum infecta una célula huésped, altera las características de la membrana de los glóbulos rojos, volviéndola "más pegajosa" a otras células. Los grupos de glóbulos rojos parasitados pueden superar el tamaño de la circulación capilar, adherirse al endotelio y bloquear la circulación. Cuando estos bloqueos se forman en los vasos sanguíneos que rodean el cerebro, causan hipoxia cerebral , lo que da lugar a síntomas neurológicos conocidos como malaria cerebral . Esta afección se caracteriza por confusión, desorientación y, a menudo, coma terminal . Representa el 80% de las muertes por malaria. Por lo tanto, las mutaciones que protegen contra la infección y la letalidad de la malaria suponen una ventaja significativa. [ cita requerida ]
La malaria ha ejercido la presión selectiva más fuerte conocida sobre el genoma humano desde el origen de la agricultura en los últimos 10.000 años. [1] [2] El Plasmodium falciparum probablemente no pudo afianzarse entre las poblaciones africanas hasta que surgieron comunidades sedentarias más grandes en asociación con la evolución de la agricultura doméstica en África (la revolución agrícola ). Varias variantes heredadas en los glóbulos rojos se han vuelto comunes en partes del mundo donde la malaria es frecuente como resultado de la selección ejercida por este parásito . [3] Esta selección fue históricamente importante como el primer ejemplo documentado de enfermedad como agente de selección natural en humanos . También fue el primer ejemplo de inmunidad innata controlada genéticamente que opera temprano en el curso de las infecciones, precediendo a la inmunidad adaptativa que ejerce efectos después de varios días. En la malaria, como en otras enfermedades, la inmunidad innata conduce a la inmunidad adaptativa y la estimula . [ cita requerida ]
Las mutaciones pueden tener efectos perjudiciales y beneficiosos, y cualquier mutación individual puede tener ambos. La infectividad de la malaria depende de proteínas específicas presentes en las paredes celulares y en otras partes de los glóbulos rojos. Las mutaciones protectoras alteran estas proteínas de manera que las hacen inaccesibles para los organismos de la malaria. Sin embargo, estos cambios también alteran el funcionamiento y la forma de los glóbulos rojos, lo que puede tener efectos visibles, ya sea de manera manifiesta o mediante un examen microscópico de los glóbulos rojos. Estos cambios pueden perjudicar la función de los glóbulos rojos de diversas maneras que tienen un efecto perjudicial sobre la salud o la longevidad del individuo. Sin embargo, si el efecto neto de la protección contra la malaria supera los otros efectos perjudiciales, la mutación protectora tenderá a conservarse y propagarse de generación en generación. [ cita requerida ]
Estas alteraciones que protegen contra las infecciones palúdicas pero dañan los glóbulos rojos se consideran generalmente trastornos sanguíneos, ya que tienden a tener efectos evidentes y perjudiciales. Su función protectora solo se ha descubierto y reconocido en tiempos recientes. Algunos de estos trastornos se conocen con nombres extravagantes y crípticos como anemia de células falciformes, talasemia, deficiencia de glucosa-6-fosfato deshidrogenasa, ovalocitosis, eliptocitosis y pérdida del antígeno de Gerbich y del antígeno de Duffy. Estos nombres se refieren a varias proteínas, enzimas y la forma o función de los glóbulos rojos. [ cita requerida ]
El potente efecto de la resistencia innata controlada genéticamente se refleja en la probabilidad de supervivencia de los niños pequeños en zonas donde la malaria es endémica. Es necesario estudiar la inmunidad innata en el grupo de edad susceptible (menores de cuatro años) porque, en los niños mayores y los adultos, los efectos de la inmunidad innata se ven eclipsados por los de la inmunidad adaptativa. También es necesario estudiar poblaciones en las que no se produce un uso aleatorio de medicamentos antipalúdicos . En la Tabla 1 se resumen algunas de las primeras contribuciones sobre la resistencia innata a las infecciones de los vertebrados, incluidos los humanos.
Es destacable que dos de los estudios pioneros se centraran en la malaria. Los estudios clásicos sobre el receptor Toll en la mosca de la fruta Drosophila [6] se extendieron rápidamente a los receptores tipo Toll en los mamíferos [7] y luego a otros receptores de reconocimiento de patrones , que desempeñan papeles importantes en la inmunidad innata. Sin embargo, las primeras contribuciones sobre la malaria siguen siendo ejemplos clásicos de resistencia innata, que han resistido la prueba del tiempo. [ cita requerida ]
Los mecanismos por los cuales los eritrocitos que contienen hemoglobinas anormales, o que son deficientes en G6PD, están parcialmente protegidos contra las infecciones por P. falciparum no se comprenden completamente, aunque no han faltado sugerencias. Durante la etapa de replicación en sangre periférica, los parásitos de la malaria tienen una alta tasa de consumo de oxígeno [8] e ingieren grandes cantidades de hemoglobina. [9] Es probable que la HbS en las vesículas endocíticas se desoxigene, se polimerice y se digiera mal. En los glóbulos rojos que contienen hemoglobinas anormales, o que son deficientes en G6PD, se producen radicales de oxígeno y los parásitos de la malaria inducen estrés oxidativo adicional. [10] Esto puede resultar en cambios en las membranas de los glóbulos rojos, incluida la translocación de fosfatidilserina a su superficie [ jerga ] , seguida del reconocimiento e ingestión de macrófagos. [11] Los autores sugieren que es probable que este mecanismo ocurra antes en los glóbulos rojos anormales que en los normales, restringiendo así la multiplicación en los primeros. Además, la unión de las células falciformes parasitadas a las células endoteliales disminuye significativamente debido a una expresión alterada de la proteína de membrana eritrocítica 1 (PfMP-1) de P. falciparum . [12] Esta proteína es el principal ligando de citoadherencia del parásito y su factor de virulencia en la superficie celular. Durante las últimas etapas de la replicación del parásito, los glóbulos rojos se adhieren al endotelio venoso y la inhibición de esta unión podría suprimir la replicación. [ cita requerida ]
La hemoglobina falciforme induce la expresión de la hemooxigenasa-1 en las células hematopoyéticas . El monóxido de carbono , un subproducto del catabolismo del hemo por la hemooxigenasa -1 (HO-1), previene la acumulación de hemo libre circulante después de la infección por Plasmodium , suprimiendo así la patogénesis de la malaria cerebral experimental. [13] Se han descrito otros mecanismos, como la mayor tolerancia a la enfermedad mediada por la HO-1 y la reducción del crecimiento parasitario debido a la translocación del micro-ARN del huésped al parásito. [14]
La primera línea de defensa contra la malaria se ejerce principalmente mediante hemoglobinas anormales y deficiencia de glucosa-6-fosfato deshidrogenasa. Los tres tipos principales de resistencia genética hereditaria – anemia falciforme , talasemias y deficiencia de G6PD – estaban presentes en el mundo mediterráneo en la época del Imperio Romano . [ cita requerida ]
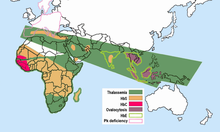
La malaria no se da en los climas más fríos y secos de las tierras altas de las regiones tropicales y subtropicales del mundo. Se han estudiado decenas de miles de individuos y no se han encontrado altas frecuencias de hemoglobinas anormales en ninguna población que estuviera libre de malaria. Las frecuencias de hemoglobinas anormales en diferentes poblaciones varían mucho, pero algunas son indudablemente polimórficas, con frecuencias más altas de lo esperado por mutación recurrente. Ya no hay duda de que la selección palúdica jugó un papel importante en la distribución de todos estos polimorfismos. Todos ellos se encuentran en áreas palúdicas, [ cita requerida ]
Las talasemias tienen una alta incidencia en una amplia banda que se extiende desde la cuenca mediterránea y partes de África, a lo largo del Medio Oriente, el subcontinente indio, el sudeste asiático, Melanesia y hasta las islas del Pacífico.
La enfermedad de células falciformes era un trastorno genético que se relacionaba con una mutación de una proteína específica. Pauling introdujo su concepto fundamental de la anemia de células falciformes como una enfermedad molecular de transmisión genética. [20]

La base molecular de la anemia de células falciformes se dilucidó finalmente en 1959, cuando Ingram perfeccionó las técnicas de la huella dactilar tripsínica de péptidos. A mediados de la década de 1950, una de las formas más nuevas y fiables de separar péptidos y aminoácidos era mediante la enzima tripsina, que divide las cadenas polipeptídicas degradando específicamente los enlaces químicos formados por los grupos carboxilo de dos aminoácidos, lisina y arginina. Pequeñas diferencias en la hemoglobina A y S darán lugar a pequeños cambios en uno o más de estos péptidos. [21] Para intentar detectar estas pequeñas diferencias, Ingram combinó la electroforesis en papel y los métodos de cromatografía en papel. Mediante esta combinación, creó un método bidimensional que le permitió "tomar la huella dactilar" comparativamente de los fragmentos de hemoglobina S y A que obtuvo del digesto con tripsina. Las huellas dactilares revelaron aproximadamente 30 manchas de péptidos; había una mancha de péptidos claramente visible en el digesto de hemoglobina S que no era obvia en la huella dactilar de hemoglobina A. El defecto del gen HbS es una mutación de un solo nucleótido (A a T) del gen de la β-globina que reemplaza el aminoácido ácido glutámico por el aminoácido menos polar valina en la sexta posición de la cadena β. [22]
La HbS tiene una carga negativa menor a pH fisiológico que la hemoglobina adulta normal. Las consecuencias de la simple sustitución de un aminoácido cargado por un aminoácido neutro e hidrofóbico son de amplio alcance. Estudios recientes en África occidental sugieren que el mayor impacto de la HbS parece ser la protección contra la muerte o la enfermedad grave (es decir, anemia profunda o malaria cerebral), mientras que tiene un efecto menor sobre la infección per se. Los niños heterocigotos para el gen de la anemia falciforme tienen sólo una décima parte del riesgo de muerte por falciparum que los homocigotos para el gen de la hemoglobina normal. La unión de los eritrocitos falciformes parasitados a las células endoteliales y a los monocitos sanguíneos se reduce significativamente debido a una expresión alterada de la proteína 1 de la membrana eritrocitaria de Plasmodium falciparum (PfEMP-1), el principal ligando de citoadherencia del parásito y factor de virulencia en la superficie de los eritrocitos. [23]
La protección también se deriva de la inestabilidad de la hemoglobina falciforme, que agrupa la proteína predominante integral de la membrana de los glóbulos rojos (llamada banda 3) y desencadena una eliminación acelerada por parte de las células fagocíticas. Los anticuerpos naturales reconocen estos grupos en los eritrocitos senescentes. La protección por HbAS implica la mejora no solo de la inmunidad innata sino también de la adquirida al parásito. [24] La hemoglobina falciforme desnaturalizada prematuramente da lugar a una regulación positiva de los anticuerpos naturales que controlan la adhesión de los eritrocitos tanto en la malaria como en la enfermedad de células falciformes. [25] Dirigirse a los estímulos que conducen a la activación endotelial constituirá una estrategia terapéutica prometedora para inhibir la adhesión de los glóbulos rojos falciformes y la vasooclusión. [26]
Esto ha llevado a la hipótesis de que mientras los homocigotos para el gen de la anemia falciforme padecen la enfermedad, los heterocigotos podrían estar protegidos contra la malaria. [27] La malaria sigue siendo un factor selectivo para el rasgo de la anemia falciforme. [28]
Desde hace tiempo se sabe que un tipo de anemia, denominada talasemia , tiene una alta frecuencia en algunas poblaciones mediterráneas, incluidas las griegas y las del sur de Italia. El nombre se deriva de las palabras griegas para mar ( thalassa ), que significa mar Mediterráneo , y sangre ( haima ). Vernon Ingram merece el crédito por explicar la base genética de las diferentes formas de talasemia como un desequilibrio en la síntesis de las dos cadenas polipeptídicas de la hemoglobina. [29]
En la variante mediterránea común, las mutaciones disminuyen la producción de la cadena β (β-talasemia). En la α-talasemia, que es relativamente frecuente en África y en otros países, la producción de la cadena α de la hemoglobina está alterada y hay una sobreproducción relativa de la cadena β. Los individuos homocigotos para la β-talasemia tienen anemia grave y es poco probable que sobrevivan y se reproduzcan, por lo que la selección contra el gen es fuerte. Los homocigotos para la α-talasemia también sufren anemia y hay cierto grado de selección contra el gen. [ cita requerida ]
Las estribaciones inferiores del Himalaya y los valles del Terai interior o Doon de Nepal y la India son altamente palúdicas debido a un clima cálido y pantanos mantenidos durante la estación seca por el agua subterránea que se filtra desde las colinas más altas. Los gobernantes de Nepal mantuvieron intencionalmente los bosques palúdicos como una medida defensiva. Los humanos que intentaron vivir en esta zona sufrieron una mortalidad mucho mayor que en elevaciones más altas o más bajas en la llanura del Ganges más seca . Sin embargo, el pueblo Tharu había vivido en esta zona el tiempo suficiente para desarrollar resistencia a través de múltiples genes. Los estudios médicos entre la población Tharu y no Tharu del Terai arrojaron la evidencia de que la prevalencia de casos de malaria residual es casi siete veces menor entre los Tharus. Se ha establecido que la base de la resistencia es la homocigosidad del gen de la α-talasemia dentro de la población local. [30] La endogamia a lo largo de las líneas de casta y etnia parece haber impedido que estos genes se extendieran más en las poblaciones vecinas. [31]
Hay evidencia de que las personas con α-talasemia, HbC y HbE tienen cierto grado de protección contra el parásito. [17] [32] La hemoglobina C (HbC) es una hemoglobina anormal con sustitución de un residuo de lisina por un residuo de ácido glutámico de la cadena de β-globina, exactamente en la misma posición β-6 que la mutación HbS. La designación "C" para HbC proviene del nombre de la ciudad donde fue descubierta: Christchurch, Nueva Zelanda. Las personas que tienen esta enfermedad, particularmente los niños, pueden tener episodios de dolor abdominal y articular, agrandamiento del bazo e ictericia leve, pero no tienen crisis graves, como ocurre en la enfermedad de células falciformes. La hemoglobina C es común en las áreas palúdicas de África Occidental, especialmente en Burkina Faso. En un amplio estudio de casos y controles realizado en Burkina Faso sobre 4.348 sujetos mossi, la HbC se asoció con una reducción del 29% del riesgo de malaria clínica en heterocigotos HbAC y del 93% en homocigotos HbCC. La HbC representa una adaptación genética "lenta pero gratuita" a la malaria a través de un polimorfismo transitorio, en comparación con la adaptación policéntrica "rápida pero costosa" a través del polimorfismo equilibrado de la HbS. [33] [34] La HbC modifica la cantidad y distribución del antígeno variante proteína de membrana de eritrocitos P. falciparum 1 (PfEMP1) en la superficie del glóbulo rojo infectado y la presentación modificada de las proteínas de superficie de la malaria reduce la adhesividad del parásito (evitando así su eliminación por el bazo) y puede reducir el riesgo de enfermedad grave. [35] [36]
La hemoglobina E se debe a una mutación puntual única en el gen de la cadena beta con una sustitución de glutamato por lisina en la posición 26. Es una de las hemoglobinopatías más prevalentes, con 30 millones de personas afectadas. La hemoglobina E es muy común en partes del sudeste asiático. Los eritrocitos HbE tienen una anomalía de membrana no identificada que hace que la mayoría de la población de glóbulos rojos sea relativamente resistente a la invasión por P. falciparum . [37]
Otras mutaciones genéticas además de las anomalías de la hemoglobina que confieren resistencia a la infección por Plasmodia implican alteraciones de las proteínas antigénicas de la superficie celular , proteínas estructurales de la membrana celular o enzimas involucradas en la glucólisis . [ cita requerida ]
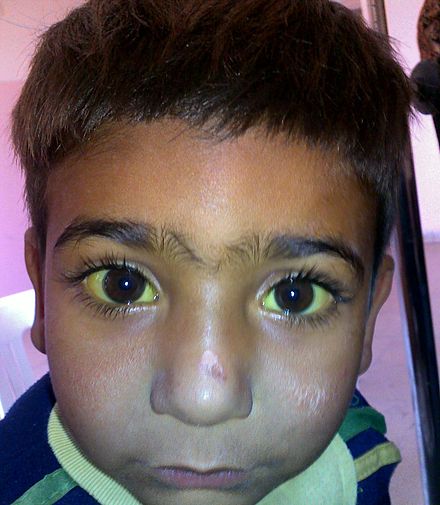
La glucosa-6-fosfato deshidrogenasa (G6PD) es una enzima importante en los glóbulos rojos, que metaboliza la glucosa a través de la vía de las pentosas fosfato , una alternativa anabólica a la oxidación catabólica (glucólisis), manteniendo al mismo tiempo un entorno reductor. [38] La G6PD está presente en todas las células humanas, pero es particularmente importante para los glóbulos rojos. Dado que los glóbulos rojos maduros carecen de núcleo y ARN citoplasmático , no pueden sintetizar nuevas moléculas enzimáticas para reemplazar a las genéticamente anormales o envejecidas. Todas las proteínas, incluidas las enzimas, tienen que durar toda la vida del glóbulo rojo, que normalmente es de 120 días. [ cita requerida ]
En 1956, Alving y sus colegas demostraron que en algunos afroamericanos el fármaco antipalúdico primaquina induce anemia hemolítica y que esos individuos tienen una deficiencia hereditaria de G6PD en los eritrocitos. [39] La deficiencia de G6PD está ligada al sexo y es común en poblaciones mediterráneas, africanas y otras. En los países mediterráneos, estos individuos pueden desarrollar una diátesis hemolítica ( favismo ) después de consumir habas . Las personas con deficiencia de G6PD también son sensibles a varios fármacos además de la primaquina. [ cita requerida ]
La deficiencia de G6PD es la segunda deficiencia enzimática más común en humanos (después de la deficiencia de ALDH2 ), y se estima que afecta a unos 400 millones de personas. [40] Hay muchas mutaciones en este locus, dos de las cuales alcanzan frecuencias del 20% o más en las poblaciones africanas y mediterráneas; estas se denominan mutaciones A y Med. [41] Las variedades mutantes de G6PD pueden ser más inestables que la enzima natural, por lo que su actividad disminuye más rápidamente a medida que los glóbulos rojos envejecen.
Esta cuestión se ha estudiado en poblaciones aisladas donde no se utilizaron medicamentos antipalúdicos en Tanzania, África Oriental [42] y en la República de Gambia , África Occidental, siguiendo a niños durante el período en que son más susceptibles a la malaria falciparum . [43] En ambos casos, los recuentos de parásitos fueron significativamente menores en personas deficientes en G6PD que en aquellas con enzimas de glóbulos rojos normales. La asociación también se ha estudiado en individuos, lo que es posible porque la deficiencia enzimática está ligada al sexo y los heterocigotos femeninos son mosaicos debido a la lionización , donde la inactivación aleatoria de un cromosoma X en ciertas células crea una población de glóbulos rojos deficientes en G6PD que coexisten con glóbulos rojos normales. Los parásitos de la malaria se observaron significativamente más a menudo en glóbulos rojos normales que en células deficientes en enzimas. [44] Tishkoff y Verelli han publicado un análisis genético evolutivo de la selección palúdica de genes de deficiencia de G6PD. [41] La deficiencia enzimática es común en muchos países que son, o fueron anteriormente, palúdicos, pero no en otros lugares. [ cita requerida ]
La deficiencia de piruvato quinasa (PK), también llamada deficiencia de piruvato quinasa eritrocitaria, es un trastorno metabólico hereditario de la enzima piruvato quinasa. En esta afección, la falta de piruvato quinasa ralentiza el proceso de glucólisis. Este efecto es especialmente devastador en las células que carecen de mitocondrias porque estas células deben utilizar la glucólisis anaeróbica como su única fuente de energía porque el ciclo del TCA no está disponible. Un ejemplo son los glóbulos rojos, que en un estado de deficiencia de piruvato quinasa rápidamente se vuelven deficientes en ATP y pueden sufrir hemólisis. Por lo tanto, la deficiencia de piruvato quinasa puede causar anemia hemolítica. [ cita requerida ]
Existe una correlación significativa entre la gravedad de la deficiencia de PK y el grado de protección contra la malaria. [45]
Eliptocitosis, un trastorno sanguíneo en el que una cantidad anormalmente grande de eritrocitos del paciente son elípticos. Existe una gran variabilidad genética entre los afectados. Existen tres formas principales de eliptocitosis hereditaria: eliptocitosis hereditaria común, eliptocitosis esferocítica y ovalocitosis del sudeste asiático . [ cita requerida ]

La ovalocitosis es un subtipo de eliptocitosis y es una afección hereditaria en la que los eritrocitos tienen una forma ovalada en lugar de redonda. En la mayoría de las poblaciones, la ovalocitosis es rara, pero la ovalocitosis del sudeste asiático (SAO) se presenta en hasta un 15 % de los pueblos indígenas de Malasia y Papúa Nueva Guinea . Se han descrito varias anomalías de los eritrocitos SAO, entre ellas, una mayor rigidez de los glóbulos rojos y una expresión reducida de algunos antígenos de los glóbulos rojos. [47] La SAO es causada por una mutación en el gen que codifica la proteína de la banda 3 de los eritrocitos . Hay una deleción de los codones 400-408 en el gen, lo que conduce a una deleción de 9 aminoácidos en el límite entre los dominios citoplasmático y transmembrana de la proteína de la banda 3. [48] La banda 3 sirve como el principal sitio de unión para el esqueleto de la membrana, una red de proteínas submembrana compuesta de anquirina , espectrina , actina y banda 4.1 . La banda 3 del ovalocito se une más fuertemente que la banda 3 normal a la anquirina, que conecta el esqueleto de la membrana al transportador de aniones de la banda 3. Estos defectos cualitativos crean una membrana de glóbulos rojos que es menos tolerante al esfuerzo cortante y más susceptible a la deformación permanente. [ cita requerida ]
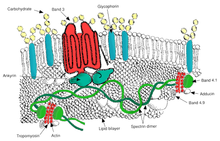
La SAO se asocia con la protección contra la malaria cerebral en niños porque reduce el secuestro de eritrocitos parasitados por P. falciparum en la microvasculatura cerebral. [49] La adhesión de los glóbulos rojos infectados por P. falciparum al CD36 se ve potenciada por el rasgo SAO protector contra la malaria cerebral. Una mayor eficiencia del secuestro a través del CD36 en individuos SAO podría determinar una distribución orgánica diferente de los glóbulos rojos infectados secuestrados. Estos proporcionan una posible explicación de la ventaja selectiva conferida por la SAO contra la malaria cerebral. [50]
Plasmodium vivax tiene una amplia distribución en países tropicales, pero está ausente o es raro en una gran región de África occidental y central, como se confirmó recientemente mediante la tipificación de especies por PCR. [51] Esta brecha en la distribución se ha atribuido a la falta de expresión del receptor de antígeno Duffy para quimiocinas (DARC) en los glóbulos rojos de muchos africanos subsaharianos. Los individuos Duffy negativos son homocigotos para un alelo DARC, que porta una mutación de un solo nucleótido (DARC 46 T → C), que perjudica la actividad del promotor al interrumpir un sitio de unión para el factor de transcripción de linaje eritroide hGATA1. [ jerga ] [52] En estudios in vitro e in vivo ampliamente citados , Miller et al. informaron que el grupo sanguíneo Duffy es el receptor para P. vivax y que la ausencia del grupo sanguíneo Duffy en los glóbulos rojos es el factor de resistencia a P. vivax en personas de ascendencia africana. [5] Este se ha convertido en un ejemplo bien conocido de resistencia innata a un agente infeccioso debido a la ausencia de un receptor para el agente en las células objetivo. [ cita requerida ]
Sin embargo, se han acumulado observaciones que muestran que el informe original de Miller necesita una calificación. En estudios humanos de transmisión de P. vivax , hay evidencia de la transmisión de P. vivax entre poblaciones Duffy-negativas en Kenia occidental, [53] la región amazónica brasileña , [54] y Madagascar . [55] La gente malgache en Madagascar tiene una mezcla de personas Duffy-positivas y Duffy-negativas de diversos orígenes étnicos. [56] Se encontró que el 72% de la población de la isla era Duffy-negativa. Se encontró positividad de P. vivax en el 8,8% de 476 personas asintomáticas Duffy-negativas, y malaria clínica por P. vivax se encontró en 17 de esas personas. La genotipificación indicó que múltiples cepas de P. vivax estaban invadiendo los glóbulos rojos de las personas Duffy-negativas. Los autores sugieren que entre las poblaciones malgaches hay suficientes personas Duffy-positivas para mantener la transmisión de mosquitos y la infección hepática. Más recientemente, se encontraron individuos Duffy negativos infectados con dos cepas diferentes de P. vivax en Angola y Guinea Ecuatorial ; además, se encontraron infecciones por P. vivax tanto en humanos como en mosquitos, lo que significa que está ocurriendo una transmisión activa. La frecuencia de dicha transmisión aún se desconoce. [57] Debido a estos varios informes de diferentes partes del mundo, está claro que algunas variantes de P. vivax se están transmitiendo a humanos que no expresan DARC en sus glóbulos rojos. El mismo fenómeno se ha observado en monos del Nuevo Mundo. [Nota 1] Sin embargo, DARC todavía parece ser un receptor importante para la transmisión humana de P. vivax .
La distribución de la negatividad de Duffy en África no se correlaciona precisamente con la de la transmisión de P. vivax . [51] Las frecuencias de negatividad de Duffy son tan altas en África Oriental (por encima del 80%), donde se transmite el parásito, como en África Occidental, donde no se transmite. La potencia de P. vivax como agente de selección natural es desconocida y puede variar de un lugar a otro. La negatividad de DARC sigue siendo un buen ejemplo de resistencia innata a una infección, pero produce una resistencia relativa y no absoluta a la transmisión de P. vivax . [ cita requerida ]

El sistema de antígenos de Gerbich es una proteína de membrana integral del eritrocito y desempeña un papel funcionalmente importante en el mantenimiento de la forma del eritrocito. También actúa como receptor de la proteína de unión a los eritrocitos de P. falciparum . Hay cuatro alelos del gen que codifica el antígeno, Ge-1 a Ge-4. Se conocen tres tipos de negatividad del antígeno Ge: Ge-1,-2,-3, Ge-2,-3 y Ge-2,+3. Las personas con el fenotipo relativamente raro Ge-1,-2,-3, son menos susceptibles (~60% de la tasa de control) a la invasión por P. falciparum . Tales individuos tienen un subtipo de una condición llamada eliptocitosis hereditaria , caracterizada por eritrocitos de forma ovalada o elíptica. [ cita requerida ]
También se sabe que mutaciones raras de las proteínas glicoforina A y B median la resistencia a P. falciparum .
Los polimorfismos del antígeno leucocitario humano (HLA), comunes en los africanos occidentales pero poco comunes en otros grupos raciales, se asocian con la protección contra la malaria grave. Este grupo de genes codifica proteínas presentadoras de antígenos de la superficie celular y tiene muchas otras funciones. En África occidental, son responsables de una reducción tan grande en la incidencia de la enfermedad como la variante de la hemoglobina falciforme. Los estudios sugieren que el polimorfismo inusual de los genes del complejo mayor de histocompatibilidad ha evolucionado principalmente a través de la selección natural por patógenos infecciosos. [ cita requerida ]
Los polimorfismos en los loci HLA, que codifican proteínas que participan en la presentación de antígenos, influyen en el curso de la malaria. En África occidental, un antígeno HLA de clase I (HLA Bw53) y un haplotipo HLA de clase II (DRB1*13OZ-DQB1*0501) se asocian de forma independiente con la protección contra la malaria grave. [60] Sin embargo, las correlaciones HLA varían, dependiendo de la constitución genética del parásito polimórfico de la malaria, que difiere en diferentes ubicaciones geográficas. [61] [62]
Algunos estudios sugieren que niveles elevados de hemoglobina fetal (HbF) confieren cierta protección contra la malaria falciparum en adultos con persistencia hereditaria de hemoglobina fetal . [63]
El biólogo evolutivo JBS Haldane fue el primero en proponer una hipótesis sobre la relación entre la malaria y esta enfermedad genética. Expuso por primera vez su hipótesis en el Octavo Congreso Internacional de Genética celebrado en 1948 en Estocolmo sobre el tema "La tasa de mutación de los genes humanos". [64] Formalizó su hipótesis en un artículo técnico publicado en 1949 en el que hizo una declaración profética: "Los corpúsculos de los heterocigotos anémicos son más pequeños de lo normal y más resistentes a las soluciones hipotónicas. Es al menos concebible que también sean más resistentes a los ataques de los esporozoos que causan la malaria". [65] Esta hipótesis se conoció como "la hipótesis de la malaria de Haldane" o, en pocas palabras, la "hipótesis de la malaria". [66]

Un estudio detallado de una cohorte de 1022 niños kenianos que vivían cerca del lago Victoria , publicado en 2002, confirmó esta predicción. [67] Muchos niños SS todavía morían antes de cumplir un año de edad. Entre los 2 y los 16 meses, se encontró que la mortalidad en los niños AS era significativamente menor que en los niños AA. Esta investigación bien controlada muestra la acción continua de la selección natural a través de la enfermedad en una población humana. [ cita requerida ]
El análisis de la asociación de todo el genoma (GWA) y el mapeo de asociación de alta resolución son métodos poderosos para establecer la herencia de la resistencia a infecciones y otras enfermedades. Se han llevado a cabo dos análisis preliminares independientes de la asociación de GWA con malaria falciparum grave en africanos, uno por parte del Consorcio Malariagen en una población gambiana y el otro por Rolf Horstmann (Instituto Bernhard Nocht de Medicina Tropical, Hamburgo) y sus colegas en una población ghanesa. En ambos casos, la única señal de asociación que alcanzó significación de todo el genoma fue con el locus HBB que codifica la cadena β de la hemoglobina, que es anormal en HbS. [68] Esto no implica que HbS sea el único gen que confiere resistencia innata a la malaria falciparum; podría haber muchos genes de este tipo que ejerzan efectos más modestos que son difíciles de detectar por GWA debido a los bajos niveles de desequilibrio de ligamiento en las poblaciones africanas. Sin embargo, la misma asociación de GWA en dos poblaciones es una evidencia poderosa de que el gen único que confiere la resistencia innata más fuerte a la malaria por falciparum es el que codifica la HbS. [ cita requerida ]
En 1954, Anthony Allison estimó la aptitud de diferentes genotipos en una región africana donde hay una intensa selección palúdica. [69] En la población Baamba que vive en la región forestal Semliki en Uganda occidental, la frecuencia de heterocigotos drepanocíticos (AS) es del 40%, lo que significa que la frecuencia del gen de la anemia falciforme es de 0,255 y el 6,5% de los niños nacidos son homocigotos SS. [Nota 2] Es una suposición razonable que hasta que se dispuso de un tratamiento moderno, tres cuartas partes de los homocigotos SS no se reproducían. Para equilibrar esta pérdida de genes drepanocíticos, sería necesaria una tasa de mutación de 1:10,2 por gen por generación. Esto es aproximadamente 1000 veces mayor que las tasas de mutación medidas en Drosophila y otros organismos y mucho más alta que la registrada para el locus drepanocítico en africanos. [70] Para equilibrar el polimorfismo, Anthony Allison estimó que la aptitud del heterocigoto AS tendría que ser 1,26 veces mayor que la del homocigoto normal. Análisis posteriores de cifras de supervivencia han dado resultados similares, con algunas diferencias de un sitio a otro. En los gambianos, se estimó que los heterocigotos AS tienen un 90% de protección contra la anemia grave asociada a P. falciparum y la malaria cerebral, [60] mientras que en la población Luo de Kenia se estimó que los heterocigotos AS tienen un 60% de protección contra la anemia palúdica grave. [67] Estas diferencias reflejan la intensidad de la transmisión de la malaria por P. falciparum de una localidad a otra y de una estación a otra, por lo que los cálculos de aptitud también variarán. En muchas poblaciones africanas la frecuencia de AS es de alrededor del 20%, y una superioridad de aptitud sobre aquellos con hemoglobina normal del orden del 10% es suficiente para producir un polimorfismo estable. [ cita requerida ]