La recombinasa Cre es una enzima tirosina recombinasa derivada del bacteriófago P1 . La enzima utiliza un mecanismo similar a la topoisomerasa I para llevar a cabo eventos de recombinación específica del sitio . La enzima (38 kDa) es un miembro de la familia de integrasas de recombinasas específicas del sitio y se sabe que cataliza el evento de recombinación específica del sitio entre dos sitios de reconocimiento de ADN ( sitios LoxP ). Este sitio de reconocimiento loxP de 34 pares de bases (pb) consta de dos secuencias palindrómicas de 13 pb que flanquean una región espaciadora de 8 pb. Los productos de la recombinación mediada por Cre en los sitios loxP dependen de la ubicación y la orientación relativa de los sitios loxP. Dos especies de ADN separadas que contienen sitios loxP pueden sufrir fusión como resultado de la recombinación mediada por Cre. Las secuencias de ADN que se encuentran entre dos sitios loxP se dice que están " floxadas ". En este caso, los productos de la recombinación mediada por Cre dependen de la orientación de los sitios loxP. El ADN que se encuentra entre dos sitios loxP orientados en la misma dirección se cortará como un bucle circular de ADN, mientras que el ADN intermedio entre dos sitios loxP que están orientados de manera opuesta se invertirá. [1] La enzima no requiere cofactores adicionales (como ATP ) o proteínas accesorias para su función. [2]
La enzima desempeña funciones importantes en el ciclo de vida del bacteriófago P1, como la ciclización del genoma lineal y la resolución de los cromosomas diméricos que se forman después de la replicación del ADN . [3]
La recombinasa Cre es una herramienta ampliamente utilizada en el campo de la biología molecular . El sistema de recombinación único y específico de la enzima se aprovecha para manipular genes y cromosomas en una amplia gama de investigaciones, como estudios de knock out o knock in de genes . La capacidad de la enzima para operar de manera eficiente en una amplia gama de entornos celulares (incluidos mamíferos, plantas, bacterias y levaduras) permite que el sistema de recombinación Cre-Lox se utilice en una gran cantidad de organismos, lo que lo convierte en una herramienta particularmente útil en la investigación científica. [4]
Estudios realizados en 1981 por Sternberg y Hamilton demostraron que el bacteriófago " P1 " tenía un sistema de recombinación específico de sitio único. Se generaron fragmentos EcoRI del genoma del bacteriófago P1 y se clonaron en vectores lambda . Se encontró que un fragmento EcoRI de 6,5 kb (Fragmento 7) permitía eventos de recombinación eficientes. [5] Se sabía que el mecanismo de estos eventos de recombinación era único ya que ocurrían en ausencia de las proteínas bacterianas RecA y RecBCD . Los componentes de este sistema de recombinación se dilucidaron utilizando estudios de mutagénesis por deleción. Estos estudios mostraron que un producto del gen P1 y un sitio de recombinación eran necesarios para que ocurrieran eventos de recombinación eficientes. El producto del gen P1 se denominó Cre ( ciclación recombinación ) y el sitio de recombinación se denominó loxP ( locus de cruce ( x ) sobre, P 1). [5] La proteína Cre se purificó en 1983 y se encontró que era una proteína de 35.000 Da. [2] No se requieren cofactores de alta energía como ATP o proteínas accesorias para la actividad de recombinasa de la proteína purificada. [2] Los primeros estudios también demostraron que Cre se une a secuencias de ADN no específicas mientras que tiene una afinidad 20 veces mayor por las secuencias loxP y los resultados de los primeros estudios de huellas de ADN también sugirieron que las moléculas de Cre se unen a sitios loxP como dímeros . [2]
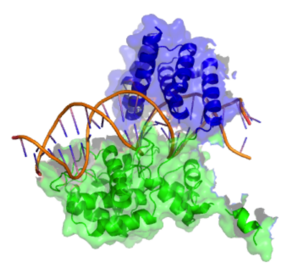

La recombinasa Cre consta de 343 aminoácidos que forman dos dominios distintos. El dominio amino terminal abarca los residuos 20-129 y este dominio contiene 5 segmentos helicoidales alfa unidos por una serie de bucles cortos. Las hélices A y E están involucradas en la formación del tetrámero de la recombinasa, y se sabe que la región C terminal de la hélice E forma contactos con el dominio C terminal de las subunidades adyacentes. Las hélices B y D forman contactos directos con el surco mayor del ADN loxP. Se cree que estas dos hélices hacen tres contactos directos con las bases de ADN en el sitio loxP. El dominio carboxiterminal de la enzima consta de los aminoácidos 132-341 y alberga el sitio activo de la enzima. La estructura general de este dominio comparte una gran similitud estructural con el dominio catalítico de otras enzimas de la misma familia, como la integrasa λ y la integrasa HP1. Este dominio tiene una estructura predominantemente helicoidal con 9 hélices distintas (F−N). La hélice terminal (N) sobresale del cuerpo principal del dominio carboxilo y se cree que esta hélice desempeña un papel en la mediación de interacciones con otras subunidades. Las estructuras cristalinas demuestran que esta hélice N terminal entierra su superficie hidrofóbica en un bolsillo aceptor de una subunidad Cre adyacente. [6]
El efecto de la estructura de dos dominios es formar una abrazadera en forma de C que sujeta el ADN desde lados opuestos. [3]

El sitio activo de la enzima Cre consiste en los residuos conservados de la tríada catalítica Arg 173, His 289, Arg 292, así como los residuos nucleofílicos conservados Tyr 324 y Trp 315. A diferencia de algunas enzimas recombinasas como la recombinasa Flp, Cre no forma un sitio activo compartido entre subunidades separadas y todos los residuos que contribuyen al sitio activo se encuentran en una sola subunidad. En consecuencia, cuando dos moléculas de Cre se unen en un solo sitio loxP, hay dos sitios activos presentes. La recombinación mediada por Cre requiere la formación de una sinapsis en la que dos complejos Cre-LoxP se asocian para formar lo que se conoce como el tetrámero de sinapsis en el que están presentes 4 sitios activos distintos. [6] Tyr 324 actúa como un nucleófilo para formar un enlace covalente 3'-fosfotirosina al sustrato de ADN. El fosfato escindible (fosfato que se dirige al ataque nucleofílico en el sitio de escisión) está coordinado por las cadenas laterales de los 3 residuos de aminoácidos de la tríada catalítica ( Arg 173, His 289 y Trp 315). El nitrógeno indólico del triptófano 315 también forma un enlace de hidrógeno con este fosfato escindible. (Nb A Histidina ocupa este sitio en otros miembros de la familia de la tirosina recombinasa y realiza la misma función). Esta reacción escinde el ADN y libera un grupo hidroxilo 5'. Este proceso ocurre en el sitio activo de dos de las cuatro subunidades de la recombinasa presentes en el tetrámero de la sinapsis. Si los grupos hidroxilo 5' atacan el enlace 3'-fosfotirosina, un par de las cadenas de ADN se intercambiarán para formar un intermediario de unión de Holliday . [3]
La recombinasa Cre desempeña papeles importantes en el ciclo de vida del bacteriófago P1 . Tras la infección de una célula, el sistema Cre-loxP se utiliza para provocar la circularización del ADN P1. Además de esto, Cre también se utiliza para resolver el ADN P1 lisogénico dimérico que se forma durante la división celular del fago. [7]
La activación inducible de Cre se logra utilizando la variante CreER (receptor de estrógeno), que solo se activa después de la administración de tamoxifeno . [8] Esto se hace a través de la fusión de un dominio de unión de ligando mutado del receptor de estrógeno a la recombinasa Cre, lo que da como resultado que Cre se active específicamente por tamoxifeno. En ausencia de tamoxifeno, CreER dará como resultado el transporte de la recombinasa mutada al citoplasma. La proteína permanecerá en esta ubicación en su estado inactivado hasta que se administre tamoxifeno. Una vez que se introduce el tamoxifeno, se metaboliza en 4-hidroxitamoxifeno, que luego se une al RE y da como resultado la translocación de CreER al núcleo, donde luego puede escindir los sitios lox. [9] Es importante destacar que, a veces, los reporteros fluorescentes pueden activarse en ausencia de tamoxifeno, debido a la fuga de unas pocas moléculas de recombinasa Cre al núcleo que, en combinación con reporteros muy sensibles, da como resultado un etiquetado celular no deseado. [10] CreER(T2) se desarrolló para minimizar la recombinación independiente del tamoxifeno y maximizar la sensibilidad al tamoxifeno.
En los últimos años, la recombinasa Cre se ha mejorado con la conversión a codones mamíferos preferidos , la eliminación de sitios de empalme crípticos informados , un codón de terminación alterado y un contenido de CpG reducido para reducir el riesgo de silenciamiento epigenético en mamíferos . [11] También se han identificado varios mutantes con mayor precisión. [12]