En química , la absorción es un fenómeno físico o químico o un proceso en el que átomos , moléculas o iones entran en alguna fase masiva: material líquido o sólido . Este es un proceso diferente a la adsorción , ya que las moléculas que se absorben son absorbidas por el volumen, no por la superficie (como en el caso de la adsorción).
Una definición más común es que "La absorción es un fenómeno químico o físico en el que las moléculas, átomos e iones de la sustancia que se absorbe entran en la fase general (gas, líquido o sólido) del material en el que se absorbe".
Un término más general es sorción , que cubre absorción, adsorción e intercambio iónico . La absorción es una condición en la que algo absorbe otra sustancia. [1]
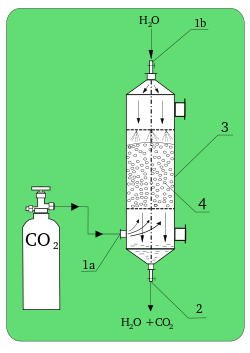
En muchos procesos importantes en tecnología, la absorción química se utiliza en lugar del proceso físico, por ejemplo, la absorción de dióxido de carbono por hidróxido de sodio; estos procesos ácido-base no siguen la ley de partición de Nernst (ver: solubilidad ).
Para ver algunos ejemplos de este efecto, consulte extracción líquido-líquido . Es posible extraer un soluto de una fase líquida a otra sin reacción química. Ejemplos de tales solutos son los gases nobles y el tetróxido de osmio . [1]
El proceso de absorción significa que una sustancia captura y transforma energía. El absorbente distribuye el material que capta por todo el conjunto y el adsorbente sólo lo distribuye por la superficie.
El proceso por el cual un gas o líquido penetra en el cuerpo del adsorbente se conoce comúnmente como absorción.
Si la absorción es un proceso físico no acompañado de ningún otro proceso físico o químico, suele seguir la ley de distribución de Nernst :
El valor de la constante K N depende de la temperatura y se llama coeficiente de partición . Esta ecuación es válida si las concentraciones no son demasiado grandes y si la especie "x" no cambia de forma en ninguna de las dos fases "1" o "2". Si dicha molécula sufre asociación o disociación , entonces esta ecuación aún describe el equilibrio entre "x" en ambas fases, pero solo para la misma forma; las concentraciones de todas las formas restantes deben calcularse teniendo en cuenta todos los demás equilibrios. [1]
En el caso de la absorción de gas, se puede calcular su concentración utilizando, por ejemplo, la ley de los gases ideales , c = p/RT . De manera alternativa, se pueden usar presiones parciales en lugar de concentraciones.
La absorción es un proceso que puede ser químico (reactivo) o físico (no reactivo).
La absorción química o absorción reactiva es una reacción química entre las sustancias absorbidas y absorbentes. A veces se combina con la absorción física. Este tipo de absorción depende de la estequiometría de la reacción y de la concentración de sus reactivos. Pueden realizarse en diferentes unidades, con un amplio espectro de tipos de flujo de fases e interacciones. En la mayoría de los casos, la AR se lleva a cabo en columnas de placas o empaquetadas. [2]
Los sólidos hidrófilos , que incluyen muchos sólidos de origen biológico, pueden absorber agua fácilmente. Las interacciones polares entre el agua y las moléculas del sólido favorecen la partición del agua en el sólido, lo que puede permitir una absorción significativa de vapor de agua incluso con una humedad relativamente baja.
Una fibra (u otro material hidrófilo) que ha estado expuesta a la atmósfera normalmente contendrá algo de agua incluso si se siente seca. El agua puede eliminarse calentándola en un horno, lo que produce una disminución mensurable de peso, que se recuperará gradualmente si la fibra regresa a una atmósfera "normal". Este efecto es crucial en la industria textil, donde la proporción del peso de un material compuesta por agua se llama recuperación de humedad . [3]