
Los polisulfuros son una clase de compuestos químicos derivados de cadenas aniónicas de átomos de azufre . [1] Hay dos clases principales de polisulfuros: inorgánicos y orgánicos. Los polisulfuros inorgánicos tienen la fórmula general S.2-
norte. Estos aniones son las bases conjugadas de los polisulfanos H 2 S n . Los polisulfuros orgánicos generalmente tienen las fórmulas R1SnR2 , donde R = alquilo o arilo . [2]

Los polisulfuros de metales alcalinos surgen del tratamiento de una solución de sulfuro , por ejemplo, sulfuro de sodio , con azufre elemental :
En algunos casos, estos aniones se han obtenido como sales orgánicas, que son solubles en disolventes orgánicos. [4]
La energía liberada en la reacción del sodio y el azufre elemental es la base de la tecnología de las baterías. La batería de sodio-azufre y la batería de litio-azufre requieren altas temperaturas para mantener las membranas conductoras de polisulfuro líquido y Na + que no reaccionan con el sodio, el azufre y el sulfuro de sodio.
Los polisulfuros son ligandos en la química de coordinación . Ejemplos de complejos de polisulfido de metales de transición incluyen (C 5 H 5 ) 2 TiS 5 , [Ni(S 4 ) 2 ] 2− y [Pt(S 5 ) 3 ] 2− . [5] Los elementos del grupo principal también forman polisulfuros. [6]

En el comercio, el término "polisulfuro" suele referirse a una clase de polímeros con cadenas alternas de varios átomos de azufre e hidrocarburos. Tienen la fórmula R 1 S n R 2 . En esta fórmula, n indica el número de átomos de azufre (o "rango"). Los polímeros de polisulfuro se pueden sintetizar mediante reacciones de polimerización por condensación entre dihaluros orgánicos y sales de metales alcalinos de aniones de polisulfuro:
Los dihaluros utilizados en esta polimerización por condensación son dicloroalcanos (como 1,2 -dicloroetano , bis-(2-cloroetil)formal ( ClCH2CH2OCH2OCH2CH2Cl ) y 1,3 -dicloropropano) . Los polímeros se llaman tiokoles . En algunos casos, los polímeros de polisulfuro se pueden formar mediante reacciones de polimerización con apertura de anillo .
Los polímeros de polisulfuro también se preparan mediante la adición de polisulfanos a alquenos. Una ecuación idealizada es:
En realidad, las muestras homogéneas de H 2 S n son difíciles de preparar. [2]
Los polímeros de polisulfuro son insolubles en agua, aceites y muchos otros disolventes orgánicos. Debido a su resistencia a los disolventes, estos materiales se utilizan como selladores para rellenar las juntas en pavimentos, cristales de ventanas de automóviles y estructuras de aviones.
Los polímeros que contienen uno o dos átomos de azufre separados por secuencias de hidrocarburos generalmente no se clasifican como polisulfuros, por ejemplo, poli ( p -fenileno)sulfuro ( C6H4S ) n .
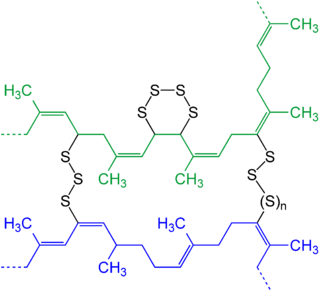
Muchos elastómeros comerciales contienen polisulfuros como enlaces cruzados . Estos enlaces cruzados interconectan cadenas de polímeros vecinas, confiriendo así rigidez. El grado de rigidez está relacionado con el número de enlaces cruzados. Por lo tanto, los elastómeros tienen una capacidad característica de "recuperar" su forma original después de ser estirados o comprimidos. Debido a esta memoria de su forma curada original , los elastómeros se denominan comúnmente cauchos . El proceso de reticular las cadenas poliméricas de estos polímeros con azufre se llama vulcanización . Las cadenas de azufre se unen a los átomos de carbono "alílicos", que son adyacentes a los enlaces C=C. La vulcanización es un paso en el procesamiento de varias clases de cauchos, incluido el policloropreno ( neopreno ) , el estireno-butadieno y el poliisopreno , que es químicamente similar al caucho natural. El descubrimiento de Charles Goodyear de la vulcanización, que implicaba calentar poliisopreno con azufre, fue revolucionario porque convirtió un material pegajoso y casi inútil en un elastómero que podía transformarse en productos útiles.
Además de agua y amoníaco , las nubes en las atmósferas de los planetas gigantes gaseosos contienen sulfuros de amonio. Las nubes de color marrón rojizo se atribuyen a polisulfuros, que surgen de la exposición de los sulfuros de amonio a la luz. [7]
Los polisulfuros, al igual que los sulfuros, pueden inducir fisuración por corrosión bajo tensión en acero al carbono y acero inoxidable .