
La teoría de la descompresión es el estudio y modelado de la transferencia del componente de gas inerte de los gases respiratorios desde el gas en los pulmones a los tejidos y viceversa durante la exposición a variaciones en la presión ambiental. En el caso del buceo submarino y el trabajo con aire comprimido, esto implica principalmente presiones ambientales mayores que la presión superficial local, [1] pero los astronautas, montañistas de gran altitud y viajeros en aeronaves que no están presurizadas a la presión del nivel del mar, [2] [3] generalmente están expuestos a presiones ambientales menores que la presión atmosférica estándar al nivel del mar. En todos los casos, los síntomas causados por la descompresión ocurren durante o dentro de un período relativamente corto de horas, o en ocasiones días, después de una reducción significativa de la presión. [4]
El término “descompresión” deriva de la reducción de la presión ambiental que experimenta el organismo y se refiere tanto a la reducción de la presión como al proceso de permitir que los gases inertes disueltos se eliminen de los tejidos durante y después de esta reducción de la presión. La absorción de gas por los tejidos se produce en estado disuelto y la eliminación también requiere que el gas esté disuelto; sin embargo, una reducción suficiente de la presión ambiental puede provocar la formación de burbujas en los tejidos, lo que puede provocar daños en los tejidos y los síntomas conocidos como enfermedad por descompresión, y también retrasa la eliminación del gas. [1]
El modelado de descompresión intenta explicar y predecir el mecanismo de eliminación de gases y formación de burbujas dentro del organismo durante y después de los cambios en la presión ambiental, [5] y proporciona modelos matemáticos que intentan predecir procedimientos de descompresión en el campo con un riesgo aceptablemente bajo y razonablemente practicables. [6] Se han utilizado modelos tanto deterministas como probabilísticos, y todavía se utilizan.
Para que la descompresión sea eficaz, el buceador debe ascender con la suficiente rapidez como para establecer un gradiente de descompresión lo más alto posible en la mayor cantidad de tejidos y sin provocar el desarrollo de burbujas sintomáticas. Esto se facilita manteniendo la presión parcial de oxígeno en el gas respirable lo más alta posible y sin riesgos, y evitando cambios de gas que puedan provocar la formación o el crecimiento de burbujas por contradifusión. El desarrollo de programas que sean seguros y eficaces se ha complicado debido a la gran cantidad de variables e incertidumbres, incluida la variación personal en la respuesta a distintas condiciones ambientales y cargas de trabajo.

El gas se respira a presión ambiental y parte de este gas se disuelve en la sangre y otros fluidos. El gas inerte continúa absorbiéndose hasta que el gas disuelto en los tejidos se encuentra en un estado de equilibrio con el gas en los pulmones (ver buceo de saturación ), o la presión ambiental se reduce hasta que los gases inertes disueltos en los tejidos se encuentran en una concentración más alta que el estado de equilibrio y comienzan a difundirse nuevamente. [1]
La absorción de gases en líquidos depende de la solubilidad del gas específico en el líquido específico, la concentración de gas, medida habitualmente por la presión parcial , y la temperatura. [1] En el estudio de la teoría de la descompresión se investiga el comportamiento de los gases disueltos en los tejidos y se modela para variaciones de presión a lo largo del tiempo. [7]
Una vez disuelto, la distribución del gas disuelto puede ser por difusión , donde no hay flujo masivo del solvente , o por perfusión , donde el solvente (sangre) circula alrededor del cuerpo del buceador, donde el gas puede difundirse a regiones locales de menor concentración . Si se da suficiente tiempo a una presión parcial específica en el gas respirable, la concentración en los tejidos se estabilizará o saturará a una velocidad que depende de la solubilidad, la velocidad de difusión y la perfusión. [1]
Si la concentración del gas inerte en el gas respirable se reduce por debajo de la de cualquiera de los tejidos, habrá una tendencia a que el gas regrese de los tejidos al gas respirable. Esto se conoce como desgasificación y ocurre durante la descompresión, cuando la reducción de la presión ambiental o un cambio de gas respirable reduce la presión parcial del gas inerte en los pulmones. [1]
Las concentraciones combinadas de gases en un tejido determinado dependerán de la historia de la presión y la composición del gas. En condiciones de equilibrio, la concentración total de gases disueltos será menor que la presión ambiental, ya que el oxígeno se metaboliza en los tejidos y el dióxido de carbono producido es mucho más soluble. Sin embargo, durante una reducción de la presión ambiental, la velocidad de reducción de la presión puede superar la velocidad a la que se puede eliminar el gas por difusión y perfusión, y si la concentración se vuelve demasiado alta, puede alcanzar una etapa en la que se pueden formar burbujas en los tejidos sobresaturados. Cuando la presión de los gases en una burbuja supera las presiones externas combinadas de la presión ambiental y la tensión superficial de la interfaz burbuja-líquido, la burbuja crecerá y este crecimiento puede causar daño a los tejidos. Los síntomas causados por este daño se conocen como enfermedad por descompresión . [1]
Las tasas reales de difusión y perfusión y la solubilidad de los gases en tejidos específicos no se conocen en general y varían considerablemente. Sin embargo, se han propuesto modelos matemáticos que se aproximan a la situación real en mayor o menor medida y estos modelos se utilizan para predecir si es probable que se produzca la formación de burbujas sintomáticas para un perfil de exposición a la presión determinado. [7] La descompresión implica una interacción compleja de solubilidad de gases, presiones parciales y gradientes de concentración, difusión, transporte masivo y mecánica de burbujas en tejidos vivos. [6]
La solubilidad de los gases en líquidos está influenciada por la naturaleza del líquido disolvente y el soluto, [8] la temperatura , [9] la presión , [10] [11] y la presencia de otros solutos en el disolvente. [12] La difusión es más rápida en moléculas más pequeñas y ligeras, de las cuales el helio es el ejemplo extremo. La difusividad del helio es 2,65 veces más rápida que la del nitrógeno. [13] El gradiente de concentración se puede utilizar como modelo para el mecanismo impulsor de la difusión. [14] En este contexto, gas inerte se refiere a un gas que no es metabólicamente activo . El nitrógeno atmosférico (N 2 ) es el ejemplo más común, y el helio (He) es el otro gas inerte comúnmente utilizado en mezclas respirables para buceadores . [15] El nitrógeno atmosférico tiene una presión parcial de aproximadamente 0,78 bar al nivel del mar. El aire de los alvéolos pulmonares se diluye con vapor de agua saturado (H 2 O) y dióxido de carbono (CO 2 ), un producto metabólico emitido por la sangre, y contiene menos oxígeno (O 2 ) que el aire atmosférico, ya que una parte de él es absorbido por la sangre para su uso metabólico. La presión parcial de nitrógeno resultante es de aproximadamente 0,758 bar. [16]
Por lo tanto, a presión atmosférica, los tejidos corporales están normalmente saturados con nitrógeno a 0,758 bar (569 mmHg). A presiones ambientales mayores debido a la profundidad o la presurización del hábitat , los pulmones de un buceador se llenan de gas respirable a la presión aumentada, y las presiones parciales de los gases constituyentes aumentarán proporcionalmente. [7] Los gases inertes del gas respirable en los pulmones se difunden en la sangre en los capilares alveolares y se distribuyen por el cuerpo por la circulación sistémica en el proceso conocido como perfusión . [7] Los materiales disueltos se transportan en la sangre mucho más rápido de lo que se distribuirían por difusión sola. [17] Desde los capilares sistémicos, los gases disueltos se difunden a través de las membranas celulares y hacia los tejidos, donde eventualmente pueden alcanzar el equilibrio. Cuanto mayor sea el suministro de sangre a un tejido, más rápido alcanzará el equilibrio con el gas a la nueva presión parcial. [7] [17] Este equilibrio se llama saturación . [7] La ingasificación parece seguir una simple ecuación exponencial inversa. El tiempo que tarda un tejido en absorber o liberar el 50% de la diferencia en la capacidad de gas disuelto a una presión parcial modificada se denomina tiempo medio para ese tejido y gas. [18] [19]
El gas permanece disuelto en los tejidos hasta que la presión parcial de ese gas en los pulmones se reduce lo suficiente como para provocar un gradiente de concentración con la sangre a una concentración menor que la de los tejidos relevantes. A medida que la concentración en la sangre cae por debajo de la concentración en el tejido adyacente, el gas se difundirá fuera del tejido hacia la sangre y luego será transportado de regreso a los pulmones, donde se difundirá hacia el gas pulmonar y luego será eliminado por exhalación. Si la reducción de la presión ambiental es limitada, esta desaturación tendrá lugar en la fase disuelta, pero si la presión ambiental se reduce lo suficiente, pueden formarse y crecer burbujas, tanto en la sangre como en otros tejidos sobresaturados. [7] Cuando la presión parcial de todo el gas disuelto en un tejido excede la presión ambiental total en el tejido, este está sobresaturado [20] y existe la posibilidad de formación de burbujas. [7]
La suma de las presiones parciales del gas que respira el buceador debe necesariamente equilibrarse con la suma de las presiones parciales en el gas pulmonar. En los alvéolos, el gas se ha humidificado y ha ganado dióxido de carbono de la sangre venosa. El oxígeno también se ha difundido en la sangre arterial, reduciendo la presión parcial de oxígeno en los alvéolos. Como la presión total en los alvéolos debe equilibrarse con la presión ambiental, esta dilución da como resultado una presión parcial efectiva de nitrógeno de aproximadamente 758 mb (569 mmHg) en el aire a presión atmosférica normal. [21] En un estado estacionario, cuando los tejidos se han saturado con los gases inertes de la mezcla respirable, los procesos metabólicos reducen la presión parcial del oxígeno menos soluble y lo reemplazan con dióxido de carbono, que es considerablemente más soluble en agua. En las células de un tejido típico, la presión parcial de oxígeno disminuirá, mientras que la presión parcial de dióxido de carbono aumentará. La suma de estas presiones parciales (agua, oxígeno, dióxido de carbono y nitrógeno) es menor que la presión total del gas respiratorio. Este es un déficit de saturación significativo, y proporciona un amortiguador contra la sobresaturación y una fuerza impulsora para disolver las burbujas. [21] Los experimentos sugieren que el grado de insaturación aumenta linealmente con la presión para una mezcla respirable de composición fija, y disminuye linealmente con la fracción de gas inerte en la mezcla respirable. [22] Como consecuencia, las condiciones para maximizar el grado de insaturación son un gas respirable con la fracción más baja posible de gas inerte, es decir, oxígeno puro, a la presión parcial máxima permisible. Este déficit de saturación también se conoce como insaturación inherente, la " ventana de oxígeno ". [23] o vacante de presión parcial. [24]
No se conoce la ubicación de los micronúcleos ni dónde se forman inicialmente las burbujas. [25] La incorporación de mecanismos de formación y crecimiento de burbujas en los modelos de descompresión puede hacer que los modelos sean más biofísicos y permitir una mejor extrapolación. [25] Las condiciones de flujo y las tasas de perfusión son parámetros dominantes en la competencia entre las burbujas de tejido y circulación, y entre múltiples burbujas, por el gas disuelto para el crecimiento de las burbujas. [25]
Para que exista una burbuja, es necesario que exista un equilibrio de fuerzas en la superficie. La suma de la presión ambiental y la presión debida a la distorsión del tejido, ejercida en el exterior de la superficie, con la tensión superficial del líquido en la interfaz entre la burbuja y el entorno, debe equilibrarse con la presión en el interior de la burbuja. Esta es la suma de las presiones parciales de los gases en el interior debido a la difusión neta de gas hacia y desde la burbuja. El equilibrio de fuerzas en la burbuja puede modificarse mediante una capa de moléculas activas superficiales que pueden estabilizar una microburbuja a un tamaño en el que la tensión superficial en una burbuja limpia haría que colapsara rápidamente, y esta capa superficial puede variar en permeabilidad , de modo que si la burbuja se comprime lo suficiente, puede volverse impermeable a la difusión. [26] Si el disolvente fuera de la burbuja está saturado o no, la presión parcial será menor que en la burbuja, y la tensión superficial aumentará la presión interna en proporción directa a la curvatura de la superficie, lo que proporciona un gradiente de presión para aumentar la difusión fuera de la burbuja, lo que efectivamente "exprime el gas fuera de la burbuja", y cuanto más pequeña sea la burbuja, más rápido se expulsará. Una burbuja de gas solo puede crecer a presión constante si el disolvente circundante está lo suficientemente sobresaturado como para superar la tensión superficial o si la capa superficial proporciona suficiente reacción para superar la tensión superficial. [26] Las burbujas limpias que son lo suficientemente pequeñas colapsarán debido a la tensión superficial si la sobresaturación es baja. Las burbujas con superficies semipermeables se estabilizarán en un radio específico dependiendo de la presión, la composición de la capa superficial y la sobresaturación, o continuarán creciendo indefinidamente, si son más grandes que el radio crítico. [27] La formación de burbujas puede ocurrir en la sangre u otros tejidos. [28]
Un disolvente puede llevar una carga sobresaturada de gas en solución. El que salga de la solución en la mayor parte del disolvente para formar burbujas dependerá de varios factores. Algo que reduzca la tensión superficial, o adsorba moléculas de gas, o reduzca localmente la solubilidad del gas, o cause una reducción local en la presión estática en un fluido puede dar como resultado la nucleación o el crecimiento de una burbuja. Esto puede incluir cambios de velocidad y turbulencia en fluidos y cargas de tensión locales en sólidos y semisólidos. Los lípidos y otras superficies hidrófobas pueden reducir la tensión superficial (las paredes de los vasos sanguíneos pueden tener este efecto). La deshidratación puede reducir la solubilidad del gas en un tejido debido a una mayor concentración de otros solutos y menos disolvente para retener el gas. [29] Otra teoría presupone que los núcleos de burbujas microscópicos siempre existen en medios acuosos, incluidos los tejidos vivos. Estos núcleos de burbujas son fases gaseosas esféricas que son lo suficientemente pequeñas para permanecer en suspensión pero lo suficientemente fuertes para resistir el colapso, y su estabilidad la proporciona una capa superficial elástica que consiste en moléculas tensioactivas que resisten el efecto de la tensión superficial. [30]
Una vez que se forma una microburbuja, puede seguir creciendo si los tejidos están suficientemente sobresaturados. A medida que la burbuja crece, puede distorsionar el tejido circundante y causar daño a las células y presión sobre los nervios, lo que produce dolor, o puede bloquear un vaso sanguíneo, cortando el flujo sanguíneo y causando hipoxia en los tejidos normalmente irrigados por el vaso. [31]
Si existe una burbuja o un objeto que recoge moléculas de gas, esta colección de moléculas de gas puede alcanzar un tamaño en el que la presión interna supere la tensión superficial y la presión externa combinadas y la burbuja crecerá. [32] Si el disolvente está suficientemente sobresaturado, la difusión del gas en la burbuja superará la velocidad a la que se difunde de nuevo en la solución, y si este exceso de presión es mayor que la presión debida a la tensión superficial, la burbuja seguirá creciendo. Cuando una burbuja crece, la tensión superficial disminuye y la presión interior cae, lo que permite que el gas se difunda hacia dentro más rápido y hacia fuera más lentamente, por lo que la burbuja crece o se encoge en una situación de retroalimentación positiva. La velocidad de crecimiento se reduce a medida que la burbuja crece porque el área de la superficie aumenta con el cuadrado del radio, mientras que el volumen aumenta con el cubo del radio. Si la presión externa se reduce debido a la presión hidrostática reducida durante el ascenso, la burbuja también crecerá y, a la inversa, un aumento de la presión externa hará que la burbuja se encoja, pero puede que no haga que se elimine por completo si existe una capa superficial resistente a la compresión. [32]
Las burbujas de descompresión parecen formarse principalmente en los capilares sistémicos, donde la concentración de gas es más alta, a menudo los que alimentan las venas que drenan las extremidades activas. Por lo general, no se forman en las arterias, siempre que la reducción de la presión ambiental no sea demasiado rápida, ya que la sangre arterial ha tenido recientemente la oportunidad de liberar el exceso de gas hacia los pulmones. Las burbujas transportadas de vuelta al corazón en las venas pueden transferirse a la circulación sistémica a través de un foramen oval permeable en buceadores con este defecto septal, después de lo cual existe el riesgo de oclusión de los capilares en cualquier parte del cuerpo en la que terminen. [33]
Las burbujas que son transportadas de vuelta al corazón por las venas pasarán al lado derecho del corazón y desde allí normalmente entrarán en la circulación pulmonar y pasarán o quedarán atrapadas en los capilares de los pulmones, que están alrededor de los alvéolos y muy cerca del gas respiratorio, donde el gas se difundirá desde las burbujas a través de las paredes capilares y alveolares hacia el gas del pulmón. Si el número de capilares pulmonares bloqueados por estas burbujas es relativamente pequeño, el buceador no mostrará síntomas y no se dañará ningún tejido (los tejidos pulmonares se oxigenan adecuadamente por difusión). [34] Las burbujas que son lo suficientemente pequeñas como para pasar a través de los capilares pulmonares pueden ser lo suficientemente pequeñas como para disolverse debido a una combinación de tensión superficial y difusión a una concentración reducida en la sangre circundante, aunque la teoría de nucleación del Modelo de Permeabilidad Variable implica que la mayoría de las burbujas que pasan a través de la circulación pulmonar perderán suficiente gas para pasar a través de los capilares y regresar a la circulación sistémica como núcleos reciclados pero estables. [35] Las burbujas que se forman dentro de los tejidos deben eliminarse in situ mediante difusión, lo que implica un gradiente de concentración adecuado. [34]
La contradifusión isobárica es la difusión de gases en direcciones opuestas causada por un cambio en la composición del gas ambiental externo o del gas respirable sin cambios en la presión ambiental. Durante la descompresión después de una inmersión, esto puede ocurrir cuando se realiza un cambio en el gas respirable o cuando el buceador se mueve hacia un entorno lleno de gas que difiere del gas respirable. [36] Si bien no es estrictamente un fenómeno de descompresión, es una complicación que puede ocurrir durante la descompresión y que puede resultar en la formación o el crecimiento de burbujas sin cambios en la presión ambiental. Lambertsen ha descrito dos formas de este fenómeno: [37] [36]
La contradifusión isobárica superficial (también conocida como contradifusión isobárica en estado estacionario) [38] se produce cuando el gas inerte respirado por el buceador se difunde más lentamente en el cuerpo que el gas inerte que lo rodea. [37] [36] [38] Un ejemplo de esto sería respirar aire en un entorno de heliox. El helio en el heliox se difunde en la piel rápidamente, mientras que el nitrógeno se difunde más lentamente desde los capilares hacia la piel y fuera del cuerpo. El efecto resultante genera sobresaturación en ciertos sitios de los tejidos superficiales y la formación de burbujas de gas inerte. [36]
La contradifusión isobárica transitoria (DCI) de tejido profundo [38] se produce cuando el buceador respira diferentes gases inertes en secuencia. [37] El gas que se difunde rápidamente se transporta hacia el tejido más rápido de lo que el gas que se difunde más lentamente se transporta fuera del tejido. [36] Esto puede ocurrir cuando los buceadores cambian de una mezcla de nitrógeno a una mezcla de helio o cuando los buceadores de saturación que respiran hidroxocobalto cambian a una mezcla de heliocobalto. [36] [39]
El estudio de Doolette y Mitchell sobre la enfermedad por descompresión del oído interno (EIOD) muestra que el oído interno puede no estar bien modelado por algoritmos comunes (por ejemplo, Bühlmann). Doolette y Mitchell proponen que un cambio de una mezcla rica en helio a una mezcla rica en nitrógeno, como es común en el buceo técnico cuando se cambia de trimix a nitrox en el ascenso, puede causar una sobresaturación transitoria de gas inerte dentro del oído interno y dar lugar a EIOD. [40] Sugieren que los cambios de gas respirable de mezclas ricas en helio a mezclas ricas en nitrógeno deben programarse cuidadosamente, ya sea en profundidad (con la debida consideración a la narcosis por nitrógeno) o en poca profundidad para evitar el período de máxima sobresaturación resultante de la descompresión. Los cambios también deben realizarse durante la respiración de la mayor presión parcial de oxígeno inspirado que se pueda tolerar de manera segura, con la debida consideración a la toxicidad del oxígeno. [40]
Aunque se cree comúnmente que la DCS es causada por la sobresaturación del gas inerte, Hempleman ha afirmado:
...Esto no condujo a una reducción suficiente en la relación de descompresión permitida y ahora se hace un margen en los cálculos para presiones parciales de oxígeno altas. Siempre que la presión parcial de oxígeno en el aire (o mezcla) exceda los 0,6 bar, se considera que hay cantidades significativas de oxígeno disuelto presentes en los tejidos y que existe un mayor riesgo de descompresión. Esto se calcula añadiendo un 25% a la profundidad de inmersión y procediendo con los cálculos como se acaba de describir utilizando el supuesto (1). De este modo, se obtiene una profundidad de primera parada de oxígeno y se pasan 5 minutos a esta profundidad para permitir el uso metabólico del exceso de gas de oxígeno disuelto. Después de esta "parada de oxígeno", los cálculos proceden como se describe anteriormente. [41]
Las burbujas vasculares formadas en los capilares sistémicos pueden quedar atrapadas en los capilares pulmonares, bloqueándolos temporalmente. Si esto es grave, puede aparecer el síntoma llamado "estrangulamiento". [33] Si el buceador tiene un foramen oval permeable (o un shunt en la circulación pulmonar), las burbujas pueden atravesarlo y eludir la circulación pulmonar para entrar en la sangre arterial. Si estas burbujas no son absorbidas en el plasma arterial y se alojan en los capilares sistémicos, bloquearán el flujo de sangre oxigenada a los tejidos abastecidos por esos capilares, y esos tejidos se verán privados de oxígeno. Moon y Kisslo (1988) concluyeron que "la evidencia sugiere que el riesgo de ED neurológica grave o ED de aparición temprana aumenta en buceadores con un shunt de derecha a izquierda en reposo a través de un FOP. Actualmente, no hay evidencia de que el FOP esté relacionado con ED leves o de aparición tardía". [42]
Las burbujas se forman dentro de otros tejidos, así como en los vasos sanguíneos. [33] El gas inerte puede difundirse en los núcleos de burbujas entre los tejidos. En este caso, las burbujas pueden distorsionar y dañar permanentemente el tejido. A medida que crecen, las burbujas también pueden comprimir los nervios a medida que crecen, causando dolor. [34] [43]
Las burbujas [a] extravasculares o autóctonas suelen formarse en tejidos lentos como articulaciones, tendones y vainas musculares. La expansión directa provoca daño tisular, con liberación de histaminas y sus efectos asociados. El daño bioquímico puede ser tan importante como los efectos mecánicos o más. [34] [33] [44]
El intercambio de gases disueltos entre la sangre y los tejidos está controlado por la perfusión y, en menor medida, por la difusión, en particular en tejidos heterogéneos. La distribución del flujo sanguíneo a los tejidos es variable y está sujeta a diversas influencias. Cuando el flujo es localmente alto, esa zona está dominada por la perfusión, y por la difusión cuando el flujo es bajo. La distribución del flujo está controlada por la presión arterial media y la resistencia vascular local, y la presión arterial depende del gasto cardíaco y de la resistencia vascular total. La resistencia vascular básica está controlada por el sistema nervioso simpático, y los metabolitos, la temperatura y las hormonas locales y sistémicas tienen efectos secundarios y a menudo localizados, que pueden variar considerablemente según las circunstancias. La vasoconstricción periférica en agua fría disminuye la pérdida total de calor sin aumentar el consumo de oxígeno hasta que comienzan los escalofríos, momento en el que el consumo de oxígeno aumentará, aunque la vasoconstricción puede persistir. [33]
La composición del gas respirable durante la exposición a la presión y la descompresión es significativa en la absorción y eliminación de gas inerte para un perfil de exposición a la presión dado. Las mezclas de gases respirables para buceo normalmente tendrán una fracción de gas de nitrógeno diferente a la del aire. La presión parcial de cada gas componente será diferente de la del nitrógeno en el aire a cualquier profundidad dada, y la absorción y eliminación de cada componente de gas inerte es proporcional a la presión parcial real a lo largo del tiempo. Las dos razones principales para el uso de gases respirables mixtos son la reducción de la presión parcial de nitrógeno por dilución con oxígeno, para hacer mezclas de Nitrox , principalmente para reducir la tasa de absorción de nitrógeno durante la exposición a la presión, y la sustitución del helio (y ocasionalmente otros gases) por el nitrógeno para reducir los efectos narcóticos bajo una exposición a alta presión parcial. Dependiendo de las proporciones de helio y nitrógeno, estos gases se denominan Heliox , si no hay nitrógeno, o Trimix , si hay nitrógeno y helio junto con el oxígeno esencial. [45] [46] Los gases inertes utilizados como sustitutos del nitrógeno tienen diferentes características de solubilidad y difusión en los tejidos vivos que el nitrógeno que reemplazan. Por ejemplo, el sustituto diluyente de gas inerte más común para el nitrógeno es el helio, que es significativamente menos soluble en el tejido vivo, [47] pero también se difunde más rápido debido al tamaño y la masa relativamente pequeños del átomo de He en comparación con la molécula de N 2 . [48]
El flujo sanguíneo a la piel y a la grasa se ve afectado por la temperatura de la piel y del núcleo, y la perfusión muscular en reposo está controlada por la temperatura del propio músculo. Durante el ejercicio, el aumento del flujo a los músculos que trabajan suele equilibrarse con una reducción del flujo a otros tejidos, como los riñones, el bazo y el hígado. [33] El flujo sanguíneo a los músculos también es menor en agua fría, pero el ejercicio mantiene el músculo caliente y el flujo elevado incluso cuando la piel está fría. El flujo sanguíneo a la grasa normalmente aumenta durante el ejercicio, pero esto se inhibe por la inmersión en agua fría. La adaptación al frío reduce la vasoconstricción extrema que suele producirse con la inmersión en agua fría. [33] Las variaciones en la distribución de la perfusión no afectan necesariamente al intercambio de gases inertes respiratorios, aunque algunos gases pueden quedar atrapados localmente por los cambios en la perfusión. El descanso en un entorno frío reducirá el intercambio de gases inertes de la piel, la grasa y los músculos, mientras que el ejercicio aumentará el intercambio de gases. El ejercicio durante la descompresión puede reducir el tiempo y el riesgo de descompresión, siempre que no haya burbujas, pero puede aumentar el riesgo si hay burbujas. [33] El intercambio de gases inertes es menos favorable para el buceador que está caliente y se ejercita en profundidad durante la fase de ingasificación, y descansa y está frío durante la descompresión. [33]
Otros factores que pueden afectar el riesgo de descompresión incluyen la concentración de oxígeno, los niveles de dióxido de carbono, la posición corporal, los vasodilatadores y constrictores, la respiración con presión positiva o negativa. [33] y la deshidratación (volumen sanguíneo). [49] La susceptibilidad individual a la enfermedad por descompresión tiene componentes que pueden atribuirse a una causa específica y componentes que parecen ser aleatorios. El componente aleatorio hace que las descompresiones sucesivas sean una prueba deficiente de susceptibilidad. [33] Algunos estudios han implicado a la obesidad y los altos niveles de lípidos séricos como factores de riesgo, y el riesgo parece aumentar con la edad. [50] Otro estudio también ha demostrado que los sujetos mayores tendían a formar más burbujas que los sujetos más jóvenes por razones aún no conocidas, pero no se identificaron tendencias entre el peso, la grasa corporal o el género y las burbujas, y la pregunta de por qué algunas personas son más propensas a formar burbujas que otras sigue sin estar clara. [51]


Se han utilizado dos conceptos bastante diferentes para el modelado de la descompresión. El primero supone que el gas disuelto se elimina mientras se encuentra en la fase disuelta y que no se forman burbujas durante la descompresión asintomática. El segundo, que se apoya en la observación experimental, supone que se forman burbujas durante la mayoría de las descompresiones asintomáticas y que la eliminación de gas debe tener en cuenta tanto la fase disuelta como la de burbujas. [32]
Los primeros modelos de descompresión tendían a utilizar los modelos de fase disuelta y los ajustaban mediante factores más o menos arbitrarios para reducir el riesgo de formación de burbujas sintomáticas. Los modelos de fase disuelta se dividen en dos grupos principales. Los modelos de compartimentos paralelos, en los que se considera que existen varios compartimentos con distintas tasas de absorción de gas (tiempo medio), independientemente unos de otros, y la condición límite está controlada por el compartimento que muestra el peor caso para un perfil de exposición específico. Estos compartimentos representan tejidos conceptuales y no están destinados a representar tejidos orgánicos específicos, sino simplemente a representar el rango de posibilidades para los tejidos orgánicos. El segundo grupo utiliza compartimentos en serie, en los que se supone que el gas se difunde a través de un compartimento antes de llegar al siguiente. [52] Una variación reciente del modelo de compartimentos en serie es el modelo de compartimentos interconectados de Goldman (ICM). [53]
Los modelos más recientes intentan modelar la dinámica de las burbujas, también mediante modelos simplificados, para facilitar el cálculo de tablas y, posteriormente, permitir predicciones en tiempo real durante una inmersión. Los modelos utilizados para aproximarse a la dinámica de las burbujas son variados y van desde aquellos que no son mucho más complejos que los modelos de fase disuelta hasta aquellos que requieren una capacidad computacional considerablemente mayor. [54]
Ninguno de los modelos de descompresión puede demostrar ser una representación precisa de los procesos fisiológicos, aunque se han propuesto interpretaciones de los modelos matemáticos que corresponden a diversas hipótesis. Todos ellos son aproximaciones que predicen la realidad en mayor o menor medida, y son aceptablemente confiables sólo dentro de los límites de calibración con los datos experimentales recopilados. [55]
El perfil de descompresión ideal crea el mayor gradiente posible para la eliminación de gas inerte de un tejido sin provocar la formación de burbujas [56], y los modelos de descompresión en fase disuelta se basan en el supuesto de que se puede evitar la formación de burbujas. Sin embargo, no es seguro que esto sea posible en la práctica: algunos de los modelos de descompresión suponen que siempre existen micronúcleos de burbujas estables [30] . Los modelos de burbujas parten del supuesto de que habrá burbujas, pero hay un volumen total de fase gaseosa tolerable [30] o un tamaño de burbuja de gas tolerable [57] , y limitan el gradiente máximo para tener en cuenta estas tolerancias [30] [57]
Los modelos de descompresión deberían predecir con precisión el riesgo en todo el rango de exposición a inmersiones cortas dentro de los límites sin paradas, inmersiones de rebote de descompresión en todo el rango de aplicabilidad práctica, incluidas inmersiones de exposición extrema e inmersiones repetitivas, gases de respiración alternativos, incluidos cambios de gas y PO2 constante , variaciones en el perfil de inmersión e inmersiones de saturación. Este no suele ser el caso, y la mayoría de los modelos están limitados a una parte del rango posible de profundidades y tiempos. También están limitados a un rango específico de gases de respiración y, a veces, restringidos al aire. [58]
Un problema fundamental en el diseño de tablas de descompresión es que las reglas simplificadas que rigen una única inmersión y ascenso no se aplican cuando ya existen algunas burbujas en el tejido, ya que éstas retrasarán la eliminación del gas inerte y la descompresión equivalente puede provocar enfermedad por descompresión. [58] El buceo repetitivo, los ascensos múltiples dentro de una única inmersión y los procedimientos de descompresión en superficie son factores de riesgo significativos para la enfermedad por descompresión en superficie. [56] Estos se han atribuido al desarrollo de un volumen de fase gaseosa relativamente alto que puede trasladarse en parte a inmersiones posteriores o al ascenso final de un perfil en dientes de sierra. [6]
La función de los modelos de descompresión ha cambiado con la disponibilidad de detectores de burbujas ultrasónicos Doppler, y ya no es simplemente limitar la aparición sintomática de la enfermedad por descompresión, sino también limitar las burbujas de gas venoso asintomáticas posteriores a la inmersión. [25] Se han realizado varias modificaciones empíricas a los modelos de fase disuelta desde la identificación de burbujas venosas mediante medición Doppler en buzos asintomáticos poco después de salir a la superficie. [59]
Un intento de encontrar una solución fue el desarrollo de modelos multi-tejidos, que suponían que las distintas partes del cuerpo absorbían y eliminaban gas a distintas velocidades. Se trata de tejidos hipotéticos que se designan como rápidos y lentos para describir la velocidad de saturación. Cada tejido, o compartimento, tiene una vida media diferente. Los tejidos reales también tardarán más o menos tiempo en saturarse, pero los modelos no necesitan utilizar valores de tejido reales para producir un resultado útil. Se han utilizado modelos con entre uno y 16 compartimentos de tejido [60] para generar tablas de descompresión, y los ordenadores de buceo han utilizado hasta 20 compartimentos. [61]
Por ejemplo: los tejidos con un alto contenido de lípidos pueden absorber una mayor cantidad de nitrógeno, pero a menudo tienen un suministro de sangre deficiente. Estos tardarán más en alcanzar el equilibrio y se describen como lentos, en comparación con los tejidos con un buen suministro de sangre y menor capacidad para el gas disuelto, que se describen como rápidos.
Los tejidos rápidos absorben gas con relativa rapidez, pero generalmente lo liberan rápidamente durante el ascenso. Un tejido rápido puede saturarse en el curso de una inmersión recreativa normal, mientras que un tejido lento puede haber absorbido solo una pequeña parte de su capacidad potencial de gas. Al calcular los niveles en cada compartimento por separado, los investigadores pueden construir algoritmos más efectivos. Además, cada compartimento puede tolerar más o menos sobresaturación que otros. La forma final es un modelo complicado, pero que permite la construcción de algoritmos y tablas adecuados para una amplia variedad de inmersiones. Un ordenador de buceo típico tiene un modelo de 8 a 12 tejidos, con tiempos medios que varían de 5 minutos a 400 minutos. [61] Las tablas de Bühlmann utilizan un algoritmo con 16 tejidos, con tiempos medios que varían de 4 minutos a 640 minutos. [60]
Se puede suponer que los tejidos están en serie, donde el gas disuelto debe difundirse a través de un tejido para llegar al siguiente, que tiene diferentes propiedades de solubilidad, en paralelo, donde la difusión dentro y fuera de cada tejido se considera independiente de los demás, y como combinaciones de tejidos en serie y en paralelo, lo que se vuelve computacionalmente complejo. [53]
El tiempo medio de un tejido es el tiempo que tarda el tejido en absorber o liberar el 50% de la diferencia en la capacidad de gas disuelto a una presión parcial modificada. Para cada medio tiempo consecutivo, el tejido absorberá o liberará nuevamente la mitad de la diferencia acumulada en la secuencia ½, ¾, 7/8, 15/16, 31/32, 63/64, etc. [19] Los medios tiempos del compartimento tisular varían de 1 minuto a al menos 720 minutos. [62] Un compartimento tisular específico tendrá diferentes medios tiempos para gases con diferentes solubilidades y velocidades de difusión. La ingasificación generalmente se modela siguiendo una ecuación exponencial inversa simple donde se supone la saturación después de aproximadamente cuatro (93,75%) a seis (98,44%) medios tiempos según el modelo de descompresión. [18] [63] [64] Este modelo puede no describir adecuadamente la dinámica de la desgasificación si hay burbujas en fase gaseosa. [65] [66]
Para una descompresión optimizada, la fuerza impulsora de la desaturación del tejido debe mantenerse al máximo, siempre que esto no cause daño tisular sintomático debido a la formación y crecimiento de burbujas (enfermedad de descompresión sintomática), o produzca una condición en la que la difusión se retrase por cualquier motivo. [67]
Existen dos formas fundamentalmente diferentes de abordar este problema. La primera se basa en la suposición de que existe un nivel de sobresaturación que no produce la formación de burbujas sintomáticas y se basa en observaciones empíricas de la tasa máxima de descompresión que no da como resultado una tasa inaceptable de síntomas. Este enfoque busca maximizar el gradiente de concentración siempre que no haya síntomas y, por lo general, utiliza un modelo de tiempo medio exponencial ligeramente modificado. El segundo supone que se formarán burbujas en cualquier nivel de sobresaturación donde la tensión total del gas en el tejido sea mayor que la presión ambiental y que el gas en las burbujas se elimine más lentamente que el gas disuelto. [64] Estas filosofías dan como resultado diferentes características de los perfiles de descompresión derivados para los dos modelos: el enfoque de sobresaturación crítica proporciona ascensos iniciales relativamente rápidos, que maximizan el gradiente de concentración, y paradas largas y poco profundas, mientras que los modelos de burbujas requieren ascensos más lentos, con primeras paradas más profundas, pero pueden tener paradas poco profundas más cortas. Este enfoque utiliza una variedad de modelos. [64] [68] [69] [67] [70]
JS Haldane utilizó originalmente una relación de presión crítica de 2 a 1 para la descompresión, basándose en el principio de que la saturación del cuerpo no debería exceder en ningún momento aproximadamente el doble de la presión del aire. [71] Este principio se aplicó como una relación de presión de la presión ambiental total y no tuvo en cuenta las presiones parciales de los gases componentes del aire respirable. Su trabajo experimental con cabras y las observaciones de buzos humanos parecieron apoyar esta suposición. Sin embargo, con el tiempo, se descubrió que esto no era coherente con la incidencia de la enfermedad por descompresión y se realizaron cambios en las suposiciones iniciales. Esto se cambió más tarde a una relación de 1,58:1 de presiones parciales de nitrógeno. [72]
Investigaciones posteriores realizadas por personas como Robert Workman sugirieron que el criterio no era la relación de presiones, sino las diferencias de presión reales. Aplicado al trabajo de Haldane, esto sugeriría que el límite no está determinado por la relación 1,58:1 sino por la diferencia de presión crítica de 0,58 atmósferas entre la presión del tejido y la presión ambiental. La mayoría de las tablas de Haldane desde mediados del siglo XX, incluidas las tablas de Bühlmann, se basan en el supuesto de la diferencia crítica. [73]
ElEl valor M es el valor máximo de presión absoluta de gas inerte que un compartimento tisular puede soportar a una presión ambiental dada sin presentar síntomas de enfermedad por descompresión. Los valores M son límites para el gradiente tolerado entre la presión del gas inerte y la presión ambiental en cada compartimento. La terminología alternativa para los valores M incluye "límites de sobresaturación", "límites de sobrepresión tolerada" y "tensiones críticas".[68][74]
Los factores de gradiente son una forma de modificar el valor M a un valor másconservadorpara su uso en un algoritmo de descompresión. El factor de gradiente es un porcentaje del valor M elegido por el diseñador del algoritmo y varía linealmente entre la profundidad máxima de la inmersión específica y la superficie. Se expresan como una designación de dos números, donde el primer número es el porcentaje del valor M profundo y el segundo es un porcentaje del valor M superficial.[69]Los factores de gradiente se aplican a todos los compartimentos de tejido por igual y producen un valor M que es linealmente variable en proporción a la presión ambiental.[69]
En efecto, el usuario está seleccionando una sobresaturación máxima menor que la que el diseñador consideró apropiada. El uso de factores de gradiente aumentará el tiempo de descompresión, particularmente en la zona de profundidad donde el valor M se reduce más. Los factores de gradiente se pueden utilizar para forzar paradas más profundas en un modelo que de otro modo tendería a producir paradas relativamente superficiales, utilizando un factor de gradiente con un primer número pequeño. [69] Varios modelos de computadoras de buceo permiten que el usuario ingrese factores de gradiente como una forma de inducir un perfil de descompresión más conservador y, por lo tanto, se presume de menor riesgo. [75] Forzar un factor de gradiente bajo en el valor M profundo puede tener el efecto de aumentar la ingestión de gas durante el ascenso, generalmente de los tejidos más lentos, que luego deben liberar una carga de gas mayor a profundidades menores. Se ha demostrado que esta es una estrategia de descompresión ineficiente. [76] [77]
El modelo de gradiente variable ajusta los factores de gradiente para adaptarse al perfil de profundidad asumiendo que un ajuste en línea recta utilizando el mismo factor en el valor M profundo independientemente de la profundidad real es menos apropiado que utilizar un valor M vinculado a la profundidad real. (el valor M superficial está vinculado a la profundidad real de cero en ambos casos) [78]
Según el modelo termodinámico de Hugh LeMessurier y Brian Andrew Hills , esta condición de fuerza impulsora óptima para la desgasificación se satisface cuando la presión ambiental es suficiente para evitar la separación de fases (formación de burbujas). [70]
La diferencia fundamental de este enfoque es equiparar la presión ambiental absoluta con el total de las tensiones parciales de los gases en el tejido para cada gas después de la descompresión como el punto límite más allá del cual se espera la formación de burbujas. [70]
El modelo supone que la insaturación natural de los tejidos debida a la reducción metabólica de la presión parcial de oxígeno proporciona un amortiguador contra la formación de burbujas, y que el tejido puede descomprimirse de forma segura siempre que la reducción de la presión ambiental no supere este valor de insaturación. Es evidente que cualquier método que aumente la insaturación permitiría una descompresión más rápida, ya que el gradiente de concentración sería mayor sin riesgo de formación de burbujas. [70]
La insaturación natural aumenta con la profundidad, por lo que es posible que haya una mayor diferencia de presión ambiental a mayor profundidad, y se reduce a medida que el buceador sale a la superficie. Este modelo conduce a velocidades de ascenso más lentas y primeras paradas más profundas, pero paradas superficiales más cortas, ya que hay menos gas en fase de burbuja que eliminar. [70]
El criterio del volumen crítico supone que siempre que el volumen total de la fase gaseosa acumulada en los tejidos supere un valor crítico, aparecerán signos o síntomas de DCS. Esta suposición está respaldada por estudios de detección de burbujas Doppler. Las consecuencias de este enfoque dependen en gran medida del modelo de formación y crecimiento de burbujas utilizado, principalmente de si la formación de burbujas es prácticamente evitable durante la descompresión. [32]
Este enfoque se utiliza en modelos de descompresión que suponen que durante los perfiles de descompresión prácticos habrá crecimiento de núcleos de burbujas microscópicas estables que siempre existen en medios acuosos, incluidos los tejidos vivos. [67]
Una descompresión eficiente minimizará el tiempo total de ascenso y limitará la acumulación total de burbujas a un valor crítico aceptable y no sintomático. La física y la fisiología del crecimiento y la eliminación de burbujas indican que es más eficiente eliminar las burbujas cuando son muy pequeñas. Los modelos que incluyen la fase de burbujas han producido perfiles de descompresión con ascensos más lentos y paradas iniciales de descompresión más profundas como una forma de reducir el crecimiento de las burbujas y facilitar la eliminación temprana, en comparación con los modelos que solo consideran el gas en fase disuelta. [79]
Una inmersión de rebote es cualquier inmersión en la que la exposición a la presión no es lo suficientemente prolongada para que todos los tejidos alcancen el equilibrio con los gases inertes del gas respirable. [80]
La exposición a la saturación es aquella en la que el tiempo de exposición a la presión es suficiente para que todos los tejidos alcancen el equilibrio con los gases inertes de la mezcla respirable. Para fines prácticos, esto se suele considerar como 6 veces el tiempo medio del tejido más lento del modelo. [80]
Un límite sin paradas, también llamado límite sin descompresión (NDL), es el contenido máximo teórico de gas disuelto de cada compartimento tisular de todo el cuerpo, que se puede descomprimir directamente a la presión de la superficie a la velocidad de ascenso elegida utilizada por el modelo, sin necesidad de detenerse para desgasificarse a cualquier profundidad, lo que tiene un riesgo aceptable de desarrollar enfermedad de descompresión sintomática. El término sin límite de descompresión es un nombre inapropiado, ya que el ascenso a la velocidad de ascenso especificada es descompresión, pero el término tiene inercia histórica y continúa utilizándose. [81] [82]
Una vez que la carga de gas de uno o más compartimentos tisulares excede el nivel máximo aceptado para el límite de no parada, existe una profundidad mínima a la que el buceador puede ascender a la velocidad de ascenso adecuada, con un riesgo aceptable de enfermedad descompresiva. Esta profundidad se conoce como el techo de descompresión. Puede considerarse una profundidad leve, en el sentido de que es físicamente trivial ascender por encima de ella, pero eso aumenta el riesgo de desarrollar enfermedad descompresiva sintomática según el modelo de descompresión. El tejido que alcanza su techo de descompresión primero se llama tejido limitante. [83]
Una obligación de descompresión es la presencia en los tejidos de suficiente gas disuelto como para que el riesgo de enfermedad de descompresión sintomática sea inaceptable si se realiza un ascenso directo a la presión de superficie a la velocidad de ascenso prescrita para el modelo de descompresión en uso. Se puede decir que un buceador con un techo de descompresión tiene una obligación de descompresión, lo que significa que debe dedicar tiempo a desgasificar durante el ascenso, además del tiempo que se dedica a ascender a la velocidad de ascenso adecuada. Este tiempo se dedica nominalmente y de manera más eficiente en las paradas de descompresión, aunque la desgasificación se producirá a cualquier profundidad en la que la sangre arterial y el gas pulmonar tengan una presión parcial del gas inerte menor que la del tejido limitante. [80]
El tiempo hasta la superficie (TTS) es el tiempo total estimado que necesita un buceador para salir a la superficie desde un punto determinado en un perfil de inmersión, utilizando un conjunto determinado de gases de descompresión, ascendiendo a la velocidad de ascenso nominal y haciendo todas las paradas a las profundidades especificadas. Este valor puede ser una estimación calculada a partir de un plan de inmersión y seguido por el buceador como programa de ascenso, o puede mostrarse en la pantalla de un ordenador de buceo como actualización en tiempo real. Puede basarse en el gas seleccionado actualmente o en la selección óptima de gas de todos los gases configurados como gases activos en el ordenador. [84]
La descompresión por etapas se realiza con paradas a profundidades específicas basadas en una serie de pasos fáciles de seguir. Para la mayoría de las tablas, este intervalo ha sido históricamente conveniente de 3 metros (10 pies), pero se puede utilizar cualquier espaciamiento arbitrario siempre que el cálculo de las paradas de descompresión lo utilice. El buceador debe permanecer en la profundidad de parada prescrita hasta que el techo disminuya a la siguiente profundidad de parada menos profunda, momento en el que el buceador asciende a esa profundidad para la siguiente parada. [83]
El cálculo del tiempo de parada también se puede realizar para seguir el techo de descompresión, lo que dará un gradiente de presión maximizado para la eliminación del gas inerte y reducirá la duración total de la descompresión en aproximadamente un 4 a 12 %. Esta estrategia se puede seguir aproximadamente cuando se utiliza una computadora de buceo con la opción habilitada. Se desconoce el efecto sobre el riesgo de descompresión con esta estrategia, ya que no se han realizado pruebas hasta 2022. [83]
Se ha demostrado experimentalmente que la formación de burbujas de gas inhibe significativamente la eliminación de gas inerte. [16] [85] Una cantidad considerable de gas inerte permanecerá en los tejidos después de que un buceador haya subido a la superficie, incluso si no se presentan síntomas de enfermedad por descompresión. Este gas residual puede estar disuelto o en forma de burbuja subclínica, y continuará desgasificándose mientras el buceador permanezca en la superficie. Si se realiza una inmersión repetida, los tejidos se cargan previamente con este gas residual, lo que hará que se saturen más rápido. [86] [87]
En el buceo repetitivo, los tejidos más lentos pueden acumular gas día tras día, si no hay tiempo suficiente para eliminarlo entre inmersiones. Esto puede ser un problema en situaciones de inmersiones múltiples de varios días. Varias descompresiones por día durante varios días pueden aumentar el riesgo de enfermedad por descompresión debido a la acumulación de burbujas asintomáticas, que reducen la tasa de desgasificación y no se tienen en cuenta en la mayoría de los algoritmos de descompresión. [88] En consecuencia, algunas organizaciones de formación de buceadores hacen recomendaciones adicionales, como tomarse "el séptimo día libre". [89]
Los modelos de descompresión deterministas son un enfoque basado en reglas para calcular la descompresión. [90] Estos modelos funcionan a partir de la idea de que la sobresaturación "excesiva" en varios tejidos es "insegura" (resultando en enfermedad por descompresión ). Los modelos generalmente contienen múltiples reglas dependientes de la profundidad y el tejido basadas en modelos matemáticos de compartimentos tisulares idealizados. No existe una forma matemática objetiva de evaluar las reglas o el riesgo general más allá de la comparación con los resultados de pruebas empíricas. Los modelos se comparan con resultados experimentales e informes de campo, y las reglas se revisan mediante un juicio cualitativo y un ajuste de curvas para que el modelo revisado prediga más de cerca la realidad observada, y luego se realizan más observaciones para evaluar la confiabilidad del modelo en extrapolaciones en rangos no probados previamente. La utilidad del modelo se juzga en función de su precisión y confiabilidad para predecir la aparición de enfermedad por descompresión sintomática y burbujas venosas asintomáticas durante el ascenso. [90]
Se puede suponer razonablemente que, en realidad, se produce tanto el transporte por perfusión a través de la circulación sanguínea como el transporte por difusión en los tejidos donde hay poco o ningún flujo sanguíneo. El problema con los intentos de modelar simultáneamente la perfusión y la difusión es que hay un gran número de variables debido a las interacciones entre todos los compartimentos tisulares y el problema se vuelve insoluble. Una forma de simplificar el modelado de la transferencia de gas hacia dentro y hacia fuera de los tejidos es hacer suposiciones sobre el mecanismo limitante del transporte de gas disuelto a los tejidos que controlan la descompresión. Suponiendo que la perfusión o la difusión tienen una influencia dominante, y que la otra puede ignorarse, se puede reducir en gran medida el número de variables. [67]
La suposición de que la perfusión es el mecanismo limitante conduce a un modelo que comprende un grupo de tejidos con diferentes tasas de perfusión, pero abastecidos por sangre con una concentración de gas aproximadamente equivalente. También se supone que no hay transferencia de gas entre compartimentos tisulares por difusión. Esto da como resultado un conjunto paralelo de tejidos independientes, cada uno con su propia tasa de entrada y salida de gases que depende de la velocidad del flujo de sangre a través del tejido. La absorción de gas para cada tejido se modela generalmente como una función exponencial, con un tiempo medio fijo para cada compartimento, y la eliminación de gas también puede modelarse mediante una función exponencial, con el mismo tiempo medio o uno más largo, o como una función más compleja, como en el modelo de eliminación exponencial-lineal. [86]
La hipótesis de la relación crítica predice que el desarrollo de burbujas ocurrirá en un tejido cuando la relación entre la presión parcial del gas disuelto y la presión ambiental exceda una relación particular para un tejido determinado. La relación puede ser la misma para todos los compartimentos del tejido o puede variar, y a cada compartimento se le asigna una relación crítica de sobresaturación específica, en función de las observaciones experimentales. [18]
John Scott Haldane introdujo el concepto de tiempos medios para modelar la absorción y liberación de nitrógeno en la sangre. Sugirió 5 compartimentos tisulares con tiempos medios de 5, 10, 20, 40 y 75 minutos. [18] En esta hipótesis inicial se predijo que si la velocidad de ascenso no permite que la presión parcial del gas inerte en cada uno de los tejidos hipotéticos supere la presión ambiental en más de 2:1, no se formarán burbujas. [71] Básicamente, esto significaba que uno podría ascender de 30 m (4 bar) a 10 m (2 bar), o de 10 m (2 bar) a la superficie (1 bar) cuando está saturado, sin un problema de descompresión. Para garantizar esto, se incorporaron varias paradas de descompresión en los programas de ascenso. La velocidad de ascenso y el tejido más rápido en el modelo determinan el tiempo y la profundidad de la primera parada. A partir de entonces, los tejidos más lentos determinan cuándo es seguro ascender más. [71] Se descubrió que esta relación 2:1 era demasiado conservadora para los tejidos rápidos (inmersiones cortas) y no lo suficientemente conservadora para los tejidos lentos (inmersiones largas). La relación también parecía variar con la profundidad. [91] El enfoque de Haldane para el modelado de la descompresión se utilizó desde 1908 hasta la década de 1960 con modificaciones menores, principalmente cambios en el número de compartimentos y los medios tiempos utilizados. Las tablas de la Marina de los EE. UU. de 1937 se basaron en la investigación de OD Yarbrough y utilizaron 3 compartimentos: se eliminaron los compartimentos de 5 y 10 minutos. En la década de 1950, se revisaron las tablas y se restauraron los compartimentos de 5 y 10 minutos, y se agregó un compartimento de 120 minutos. [92]
En la década de 1960, Robert D. Workman, de la Unidad de Buceo Experimental (NEDU) de la Armada de los EE. UU., revisó la base del modelo y las investigaciones posteriores realizadas por la Armada de los EE. UU. Las tablas basadas en el trabajo de Haldane y los refinamientos posteriores seguían siendo inadecuadas para inmersiones más prolongadas y profundas. Workman propuso que el cambio tolerable en la presión se describía mejor como una diferencia de presión crítica y revisó el modelo de Haldane para permitir que cada compartimento tisular tolerara una cantidad diferente de sobresaturación que varía con la profundidad. Introdujo el término "valor M" para indicar la cantidad máxima de sobresaturación que cada compartimento podía tolerar a una profundidad determinada y agregó tres compartimentos adicionales con tiempos medios de 160, 200 y 240 minutos. Workman presentó sus hallazgos como una ecuación que podría usarse para calcular los resultados para cualquier profundidad y afirmó que una proyección lineal de los valores M sería útil para la programación informática. [92]
Una gran parte de la investigación de Albert A. Bühlmann fue determinar los compartimentos de tiempo medio más largos para el nitrógeno y el helio, y aumentó el número de compartimentos a 16. Investigó las implicaciones de la descompresión después de bucear en altitud y publicó tablas de descompresión que podrían usarse en un rango de altitudes. Bühlmann utilizó un método para el cálculo de la descompresión similar al propuesto por Workman, que incluía valores M que expresaban una relación lineal entre la presión máxima del gas inerte en los compartimentos de tejido y la presión ambiental, pero basados en la presión absoluta, lo que los hacía más fáciles de adaptar para el buceo en altitud. [52] El algoritmo de Bühlmann se utilizó para generar las tablas de descompresión estándar para varias asociaciones de buceo deportivo, y se utiliza en varias computadoras personales de descompresión, a veces en una forma modificada. [52]
BA Hills y DH LeMessurier estudiaron las prácticas empíricas de descompresión de los buceadores de perlas de Okinawa en el estrecho de Torres y observaron que hacían paradas más profundas pero reducían el tiempo total de descompresión en comparación con las tablas de uso generalizado en la época. Su análisis sugirió firmemente que la presencia de burbujas limita las tasas de eliminación de gases y enfatizó la importancia de la insaturación inherente de los tejidos debido al procesamiento metabólico del oxígeno. Esto se conoció como el modelo termodinámico. [70] Más recientemente, los buceadores técnicos recreativos desarrollaron procedimientos de descompresión utilizando paradas más profundas que las requeridas por las tablas de descompresión en uso. Esto condujo a los modelos de burbujas RGBM y VPM. [93] Una parada profunda era originalmente una parada adicional introducida por los buceadores durante el ascenso, a una profundidad mayor que la parada más profunda requerida por su algoritmo informático. También hay algoritmos informáticos que afirman utilizar paradas profundas, pero estos algoritmos y la práctica de paradas profundas no han sido adecuadamente validados. [94]
Una " parada Pyle " es una parada profunda que recibe su nombre en honor a Richard Pyle , uno de los primeros defensores de las paradas profundas, [95] en las profundidades intermedias entre el fondo y la primera parada de descompresión convencional, y intermedias entre la parada Pyle anterior y la parada convencional más profunda, siempre que la parada convencional sea más de 9 m más superficial. Una parada Pyle dura unos 2 minutos. El tiempo de ascenso adicional necesario para las paradas Pyle se incluye en el perfil de inmersión antes de finalizar el programa de descompresión. [96] Pyle descubrió que en las inmersiones en las que se detenía periódicamente para ventilar las vejigas natatorias de sus ejemplares de peces, se sentía mejor después de la inmersión, y basó el procedimiento de parada profunda en las profundidades y la duración de estas pausas. [94] La hipótesis es que estas paradas proporcionan una oportunidad para eliminar el gas mientras aún está disuelto, o al menos mientras las burbujas son todavía lo suficientemente pequeñas como para eliminarse fácilmente, y el resultado es que habrá considerablemente menos burbujas venosas o más pequeñas para eliminar en las paradas más superficiales, como predice el modelo termodinámico de Hills. [97]
No está claro el valor y la seguridad de las paradas profundas adicionales al programa de descompresión derivado de un algoritmo de descompresión. Los expertos en descompresión han señalado que es probable que se realicen paradas profundas a profundidades en las que continúa la insuflación de gases en algunos tejidos lentos, y que la adición de paradas profundas de cualquier tipo debe incluirse en la exposición hiperbárica para la que se calcula el programa de descompresión, y no añadirse después, de modo que se pueda tener en cuenta dicha insuflación de gases en los tejidos más lentos. [94] Las paradas profundas realizadas durante una inmersión en la que la descompresión se calcula en tiempo real son simplemente parte de una inmersión de varios niveles para la computadora, y no agregan ningún riesgo más allá del que es inherente al algoritmo.
Existe un límite a la profundidad de una "parada profunda". Debe producirse cierta liberación de gases y debe minimizarse la liberación continua de gases para lograr una descompresión aceptablemente eficaz. La "parada de descompresión más profunda posible" para un perfil determinado puede definirse como la profundidad en la que la carga de gas del compartimento principal cruza la línea de presión ambiental. Esta no es una profundidad de parada útil: es necesario un exceso de concentración de gas en el tejido para impulsar la difusión de la desgasificación; sin embargo, esta profundidad es un indicador útil del comienzo de la zona de descompresión, en la que la velocidad de ascenso es parte de la descompresión planificada. [99]
Un estudio realizado por DAN en 2004 descubrió que la incidencia de burbujas de alto grado se podía reducir a cero siempre que la concentración de nitrógeno del tejido más saturado se mantuviera por debajo del 80 por ciento del valor M permitido y que una parada profunda adicional era una forma simple y práctica de hacerlo, manteniendo al mismo tiempo la velocidad de ascenso original. [93]
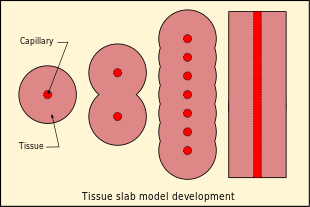
La suposición de que la difusión es el mecanismo limitante del transporte de gas disuelto en los tejidos da como resultado un modelo de compartimentos tisulares bastante diferente. En este caso se ha postulado una serie de compartimentos, con transporte por perfusión hacia un compartimento y difusión entre los compartimentos, que para simplificar están dispuestos en serie, de modo que para el compartimento generalizado, la difusión se produce hacia y desde solo los dos compartimentos adyacentes en lados opuestos, y los casos límite son el primer compartimento donde el gas se suministra y se retira mediante perfusión, y el final de la línea, donde solo hay un compartimento vecino. [52] El modelo en serie más simple es un compartimento único, y esto se puede reducir aún más a un modelo de "losa de tejido" unidimensional. [52]
Los modelos de descompresión de burbujas son un enfoque basado en reglas para calcular la descompresión, que se basa en la idea de que siempre existen núcleos de burbujas microscópicos en el agua y en los tejidos que contienen agua, y que al predecir y controlar el crecimiento de las burbujas, se puede evitar la enfermedad por descompresión. La mayoría de los modelos de burbujas suponen que se formarán burbujas durante la descompresión y que se produce la eliminación de gas en fase mixta, que es más lenta que la eliminación en fase disuelta. Los modelos de burbujas tienden a tener primeras paradas más profundas para deshacerse de más gas disuelto a una sobresaturación menor para reducir el volumen total de la fase de burbujas y, potencialmente, reducir el tiempo necesario a profundidades más bajas para eliminar las burbujas. [30] [57] [97]
Los modelos de descompresión que suponen la eliminación de gases en fase mixta incluyen:
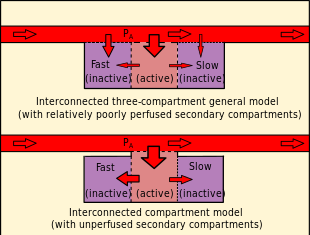
A diferencia de los compartimentos paralelos independientes de los modelos de Haldan, en los que todos los compartimentos se consideran portadores de riesgo, el modelo de Goldman postula un compartimento "activo" o "portador de riesgo" relativamente bien perfundido en serie con compartimentos "de reserva" o "amortiguadores" adyacentes relativamente mal perfundidos, que no se consideran sitios potenciales para la formación de burbujas, pero que afectan la probabilidad de formación de burbujas en el compartimento activo mediante el intercambio de gas inerte difusivo con el compartimento activo. [53] [100] Durante la compresión, el gas se difunde en el compartimento activo y a través de él en los compartimentos amortiguadores, lo que aumenta la cantidad total de gas disuelto que pasa a través del compartimento activo. Durante la descompresión, este gas amortiguado debe pasar nuevamente por el compartimento activo antes de poder eliminarse. Si la carga de gas de los compartimentos amortiguadores es pequeña, la difusión de gas adicional a través del compartimento activo es lenta. [100] Los modelos interconectados predicen una reducción en la tasa de lavado de gas con el tiempo durante la descompresión en comparación con la tasa predicha para el modelo de compartimento paralelo independiente utilizado para la comparación. [53]
El modelo de Goldman difiere del modelo de descompresión de la serie Kidd-Stubbs en que el modelo de Goldman supone una cinética lineal, mientras que el modelo KS incluye un componente cuadrático y el modelo de Goldman considera que solo el compartimento central bien perfundido contribuye explícitamente al riesgo, mientras que el modelo KS supone que todos los compartimentos conllevan un riesgo potencial. El modelo DCIEM 1983 asocia el riesgo con los dos compartimentos más externos de una serie de cuatro compartimentos. [53] Goldman afirma que el modelo matemático basado en este concepto no solo se ajusta a los datos del perfil cuadrado de la Marina utilizados para la calibración, sino que también predice el riesgo con relativa precisión para los perfiles de saturación. Una versión de burbuja del modelo ICM no fue significativamente diferente en las predicciones y se descartó por ser más compleja y sin ventajas significativas. El ICM también predijo la incidencia de la enfermedad por descompresión con mayor precisión en las exposiciones de buceo recreativo de bajo riesgo registradas en el conjunto de datos del Proyecto Dive Exploration de DAN. Los modelos alternativos utilizados en este estudio fueron los modelos LE1 (lineal-exponencial) y Haldanean recto. [100] El modelo de Goldman predice una reducción significativa del riesgo después de una parada de seguridad en una inmersión de bajo riesgo [101] y una reducción significativa del riesgo mediante el uso de nitrox (más de lo que sugieren las tablas PADI). [102]
Los modelos de descompresión probabilística están diseñados para calcular el riesgo (o probabilidad) de que ocurra una enfermedad por descompresión (EDC) en un perfil de descompresión dado. [103] [90] El análisis estadístico es muy adecuado para el trabajo con aire comprimido en operaciones de construcción de túneles debido a la gran cantidad de sujetos que se someten a exposiciones similares a la misma presión y temperatura ambiente, con cargas de trabajo y tiempos de exposición similares, con el mismo programa de descompresión. [104] Un gran número de descompresiones en circunstancias similares han demostrado que no es razonablemente factible eliminar todo el riesgo de EDC, por lo que es necesario establecer un riesgo aceptable, en función de los demás factores relevantes para la aplicación. Por ejemplo, el fácil acceso a un tratamiento eficaz en forma de tratamiento con oxígeno hiperbárico en el sitio, o una mayor ventaja para sacar al buceador del agua antes, pueden hacer que una mayor incidencia sea aceptable, mientras que la interferencia con el horario de trabajo, los efectos adversos en la moral de los trabajadores o una alta expectativa de litigio cambiarían la tasa de incidencia aceptable hacia abajo. La eficiencia también es un factor, ya que la descompresión de los empleados se produce durante las horas de trabajo. [104]
Estos métodos pueden variar las profundidades y los tiempos de las paradas de descompresión para llegar a un programa de descompresión que suponga una probabilidad específica de que se produzca una DCS, al tiempo que se minimiza el tiempo total de descompresión. Este proceso también puede funcionar a la inversa, lo que permite calcular la probabilidad de que se produzca una DCS para cualquier programa de descompresión, siempre que se cuente con datos suficientes y fiables. [104]
En 1936, una tasa de incidencia del 2% se consideró aceptable para los trabajadores de aire comprimido en el Reino Unido. En 2000, la Marina de los EE. UU. aceptó una incidencia del 2% de síntomas leves, pero solo del 0,1% de síntomas graves. El buceo comercial en el Mar del Norte en la década de 1990 aceptó un 0,5% de síntomas leves, pero casi ningún síntoma grave, y el buceo comercial en el Golfo de México también durante la década de 1990 aceptó un 0,1% de casos leves y un 0,025% de casos graves. Las autoridades de salud y seguridad tienden a especificar el riesgo aceptable como el más bajo que sea razonablemente posible teniendo en cuenta todos los factores relevantes, incluidos los factores económicos. [104] [103] Para analizar la probabilidad de síntomas leves y graves, primero es necesario definir estas clases de manifestación, según corresponda al análisis. [105]
Las herramientas necesarias para la estimación de la probabilidad de enfermedad por descompresión son un modelo biofísico que describe el intercambio de gases inertes y la formación de burbujas durante la descompresión, datos de exposición en forma de perfiles de presión/tiempo para las mezclas de gases respirables y los resultados de DCS para estas exposiciones, métodos estadísticos, como el análisis de supervivencia o el análisis bayesiano para encontrar un mejor ajuste entre el modelo y los datos experimentales, después de lo cual los modelos se pueden comparar cuantitativamente y el modelo que mejor se ajusta se utiliza para predecir la probabilidad de DCS para el modelo. Este proceso se complica por la influencia de las condiciones ambientales en la probabilidad de DCS. Los factores que afectan la perfusión de los tejidos durante la entrada y salida de gases, que afectan las tasas de absorción y eliminación de gases inertes respectivamente, incluyen la inmersión, la temperatura y el ejercicio. También se sabe que el ejercicio promueve la formación de burbujas durante la descompresión. [104]
También se sabe que la distribución de las paradas de descompresión afecta el riesgo de DCS. Un experimento de la USN que utilizó la enfermedad de descompresión sintomática como punto final comparó dos modelos para exposiciones laborales de buceo con aire utilizando el mismo tiempo de fondo, temperatura del agua y carga de trabajo, con el mismo tiempo total de descompresión, para dos distribuciones de profundidad diferentes de paradas de descompresión, también con aire, y descubrió que las paradas menos profundas conllevaban un riesgo estadísticamente muy significativamente menor. El modelo no intentó optimizar la distribución de profundidad del tiempo de descompresión, o el uso del cambio de gas, solo comparó la efectividad de dos modelos específicos, pero para esos modelos los resultados fueron convincentes. [104]
Se llevó a cabo otro conjunto de experimentos para una serie de exposiciones de tiempo de fondo cada vez mayores a una profundidad constante, con una temperatura ambiente variable. Se compararon cuatro condiciones de temperatura: cálida durante el sector de fondo y la descompresión, fría durante el sector de fondo y la descompresión, cálida en el fondo y fría durante la descompresión, y fría en el fondo y cálida durante la descompresión. Los efectos fueron muy claros: la incidencia de DCS fue mucho menor para los buzos que estaban más fríos durante la fase de ingestión de gases y más cálidos durante la descompresión que a la inversa, lo que se ha interpretado como un indicador de los efectos de la temperatura en la perfusión sobre la absorción y eliminación de gases. [104]
Un análisis estadístico retrospectivo de un gran conjunto de datos de informes de casos de inmersiones con aire y nitrox publicado en 2017 indicó que para un riesgo aceptable del 2 % para síntomas leves y del 0,1 % para síntomas graves, utilizando un modelo de desgasificación exponencial lineal, el riesgo de síntomas graves era el factor limitante. Uno de los factores que complicaron este análisis fue la variabilidad en los métodos para distinguir entre casos leves y graves. [103]
La descompresión por saturación es un proceso fisiológico de transición desde un estado estable de saturación total con gas inerte a presión elevada a condiciones estándar a presión atmosférica normal en la superficie. Es un proceso largo durante el cual los gases inertes se eliminan a una velocidad muy lenta, limitada por los tejidos afectados más lentamente, y una desviación puede provocar la formación de burbujas de gas que pueden producir enfermedad por descompresión. La mayoría de los procedimientos operativos se basan en parámetros derivados experimentalmente que describen una velocidad de descompresión lenta y continua, que puede depender de la profundidad y la mezcla de gases. [106]
En el buceo de saturación, todos los tejidos se consideran saturados y la descompresión, que es segura para los tejidos más lentos, teóricamente será segura para todos los tejidos más rápidos en un modelo paralelo. El ascenso directo desde la saturación de aire a aproximadamente 7 msw produce burbujas de gas venoso, pero no DCS sintomático. Las exposiciones a saturaciones más profundas requieren programas de descompresión a saturación. [107]
La tasa segura de descompresión de una inmersión de saturación está controlada por la presión parcial de oxígeno en el gas de respiración inspirado. [108] La insaturación inherente debida a la ventana de oxígeno permite una fase inicial relativamente rápida de descompresión de saturación en proporción a la presión parcial de oxígeno y luego controla la tasa de descompresión adicional limitada por el tiempo medio de eliminación de gas inerte del compartimento más lento. [109] Sin embargo, algunos programas de descompresión de saturación específicamente no permiten que una descompresión comience con una excursión hacia arriba. [110] No se ha encontrado que ni las excursiones ni los procedimientos de descompresión actualmente en uso (2016) causen problemas de descompresión de forma aislada, pero parece haber un riesgo significativamente mayor cuando las excursiones son seguidas por descompresión antes de que las burbujas asintomáticas resultantes de las excursiones se hayan resuelto por completo. Comenzar la descompresión mientras hay burbujas parece ser el factor significativo en muchos casos de enfermedad por descompresión inesperada durante la descompresión de saturación de rutina. [111]
La aplicación de un modelo de burbujas en 1985 permitió modelar con éxito descompresiones convencionales, descompresión de altitud, umbrales sin paradas e inmersiones de saturación utilizando una configuración de cuatro parámetros de nucleación global. [112]
La investigación continúa en el modelado de descompresión de saturación y en la programación de pruebas. En 2015, se utilizó un concepto llamado Ventana de Oxígeno Extendida en pruebas preliminares para un modelo de descompresión de saturación modificado. Este modelo permite una tasa más rápida de descompresión al inicio del ascenso para aprovechar la insaturación inherente debido al uso metabólico del oxígeno, seguida de una tasa constante limitada por la presión parcial de oxígeno del gas respirable. El período de tasa de descompresión constante también está limitado por la fracción máxima de oxígeno permitida y, cuando se alcanza este límite, la tasa de descompresión se reduce nuevamente a medida que se reduce la presión parcial de oxígeno. El procedimiento sigue siendo experimental a partir de mayo de 2016. El objetivo es una reducción aceptablemente segura del tiempo total de descompresión para una profundidad de saturación y una mezcla de gases determinadas. [106]
Es importante que cualquier teoría sea validada mediante procedimientos de prueba cuidadosamente controlados. A medida que los procedimientos y equipos de prueba se vuelven más sofisticados, los investigadores aprenden más sobre los efectos de la descompresión en el cuerpo. La investigación inicial se centró en producir inmersiones que estuvieran libres de síntomas reconocibles de enfermedad por descompresión (EDC). Con el uso posterior de pruebas de ultrasonido Doppler, se observó que se formaban burbujas dentro del cuerpo incluso en inmersiones en las que no se encontraron signos o síntomas de ED. Este fenómeno se conoce como "burbujas silenciosas". La presencia de émbolos de gas venoso se considera un predictor de baja especificidad de enfermedad por descompresión, pero su ausencia se reconoce como un indicador sensible de descompresión de bajo riesgo, por lo tanto, se cree que la detección cuantitativa de EGV es útil como indicador de estrés de descompresión al comparar estrategias de descompresión o evaluar la eficiencia de los procedimientos. [113]
Las tablas de la Marina de los EE. UU. de 1956 se basaban en límites determinados por signos y síntomas externos de DCS. Los investigadores posteriores pudieron mejorar este trabajo ajustando las limitaciones en función de las pruebas Doppler. Sin embargo, las tablas CCR de la Marina de los EE. UU. basadas en el algoritmo de Thalmann también utilizaron solo síntomas reconocibles de DCS como criterio de prueba. [114] [115] Dado que los procedimientos de prueba son largos y costosos, y existen limitaciones éticas en el trabajo experimental en sujetos humanos con lesiones como punto final, es una práctica común que los investigadores realicen validaciones iniciales de nuevos modelos basados en resultados experimentales de ensayos anteriores. Esto tiene algunas implicaciones al comparar modelos. [116]
Las inmersiones profundas y de corta duración requieren una descompresión prolongada en comparación con el tiempo en profundidad, lo que es inherentemente ineficiente en comparación con el buceo de saturación. Se han utilizado varias modificaciones de los algoritmos de descompresión con un rendimiento razonablemente validado en inmersiones a menor profundidad en el esfuerzo por desarrollar una descompresión más corta o segura, pero generalmente no están respaldadas por experimentos controlados y, en cierta medida, se basan en evidencia anecdótica. Se desarrolló una creencia generalizada de que los algoritmos basados en modelos de burbujas y que distribuyen las paradas de descompresión en un rango mayor de profundidades son más eficientes que los modelos tradicionales de contenido de gas disuelto al minimizar la formación temprana de burbujas, basándose en consideraciones teóricas, en gran parte en ausencia de evidencia de efectividad, aunque hubo bajas incidencias de enfermedad de descompresión sintomática. Existe cierta evidencia relevante para algunas de estas modificaciones y se ha analizado, y generalmente respalda la opinión opuesta de que las paradas profundas pueden conducir a mayores tasas de formación y crecimiento de burbujas en comparación con los sistemas establecidos que utilizan paradas a menor profundidad distribuidas en el mismo tiempo total de descompresión para un perfil profundo determinado. [117] [76]
La integral de la sobresaturación a lo largo del tiempo puede ser un indicador de estrés de descompresión, ya sea para un grupo de tejidos determinado o para todos los grupos de tejidos. La comparación de este indicador calculado para los grupos de tejidos Bühlmann combinados para un rango de programas de descompresión de igual duración para la misma profundidad, tiempo de fondo y mezclas de gases, ha sugerido un mayor estrés de descompresión general para inmersiones con paradas profundas, al menos en parte debido a la continua ingestión de gases de tejidos más lentos durante las paradas profundas. [76]
El cambio de gas durante la descompresión en circuito abierto se realiza principalmente para aumentar la presión parcial de oxígeno y aumentar el efecto ventana de oxígeno , mientras se mantienen los niveles de toxicidad aguda por debajo de los niveles normales. Está bien establecido tanto en la teoría como en la práctica que una presión parcial de oxígeno más alta facilita una eliminación más rápida y efectiva del gas inerte, tanto en estado disuelto como en forma de burbujas. En el buceo con rebreather de circuito cerrado, la presión parcial de oxígeno durante toda la inmersión se mantiene a un nivel relativamente alto pero tolerable para reducir la liberación de gases y acelerar la liberación de gases del gas diluyente. Los cambios de diluyentes a base de helio a nitrógeno durante el ascenso son deseables para reducir el uso de helio costoso, pero tienen otras implicaciones. Es poco probable que los cambios al gas de descompresión a base de nitrógeno aceleren la descompresión en los perfiles típicos de buceo técnico con rebote, pero hay alguna evidencia de que la descompresión con mezclas de helio y oxígeno tiene más probabilidades de resultar en una DCS neurológica, mientras que la descompresión a base de nitrógeno tiene más probabilidades de producir otros síntomas si se produce una DCS. Sin embargo, el cambio de un gas de descompresión rico en helio a uno rico en nitrógeno está implicado en la DCS del oído interno, relacionada con los efectos de contradifusión. Este riesgo se puede reducir mediante una descompresión inicial suficiente, utilizando una presión parcial de oxígeno alta y haciendo que el cambio de helio a nitrógeno sea relativamente superficial. [117]
En 1982, la USAF realizó experimentos con sujetos humanos para validar los programas de buceo con aire sin límites de descompresión antes de excursiones inmediatas a la altitud y para el buceo en altitud que permitiera volar inmediatamente después de la inmersión a una altitud de 8.500 pies (2.600 m). [118] En 2004 se realizó otra serie de pruebas para validar las predicciones de un modelo de burbuja para la descompresión en altitud utilizando perfiles de exposición no probados previamente. Los parámetros incluyeron el esfuerzo, altitudes de 18.000 a 35.000 pies (5.500 a 10.700 m), tiempo de pre-respiración y tiempo de exposición, pero estas exposiciones no incluyeron inmersiones recientes. [119]
Experiments with an endpoint of DCS symptoms using profiles near the no-decompression exposure limits for recreational diving were carried out to determine how DCS occurrence during or after flight relates to the length of pre-flight surface interval (PFSI). The dives and PFSI were followed by a four-hour exposure at 75 kPa, equivalent to the maximum permitted commercial aircraft cabin altitude of 8,000 feet (2,400 m). DCS incidence decreased as surface interval increased, with no incidence for a 17 hour surface interval. Repetitive dives profiles usually needed longer surface intervals than single dives to minimise incidence. These tests have helped inform recommendations on time to fly.[120]
In-flight transthoracic echocardiography has shown that there is a low but non-zero probability of decompression sickness in commercial pressurised aircraft after a 24 hour pre-flight surface interval following a week of multiple repetitive recreational dives, indicated by detection of venous gas bubbles in a significant number of the divers tested.[121]
Research on decompression continues. Data is not generally available on the specifics, however Divers Alert Network (DAN) has an ongoing citizen science based programme run by DAN (Europe) which gathers data from volunteer recreational divers for analysis by DAN research staff and other researchers. This research is funded by subscription fees of DAN Europe members.[122] The Diving Safety Laboratory is a database to which members can upload dive profiles from a wide range of dive computers converted to a standard format and other data about the dive.[123] Data on hundreds of thousands of real dives is analysed to investigate aspects of diving safety.[124] The large amounts of data gathered is used for probabilistic analysis of decompression risk. The data donors can get immediate feedback in the form of a simple risk analysis of their dive profiles rated as one of three nominal levels of risk (high, medium and low) based on comparison with Bühlmann ZH16c M-values computed for the same profile.
Listed projects (not all directly related to decompression) include:[125]
Bubble models for decompression were popular among technical divers in the early 2000s, although there was little data to support the effectiveness of the models in practice. Since then, several comparative studies have indicated relatively larger numbers of venous gas emboli after decompression based on bubble models, and one study reported a higher rate of decompression sickness. The deeper decompression stops earlier in the ascent appear to be less effective at controlling bubble formation than the hypotheses suggested. This failure may be due to continued ingassing of slower tissues during the extended time at greater depth, resulting in these tissues being more supersaturated at shallower depths. The optimal decompression strategy for deep bounce dives remains unknown (2016).[126]
The practical efficacy of gas switches from helium-based diluent to nitrox for accelerating decompression has not been demonstrated convincingly. These switches increase risk of inner ear decompression sickness due to counterdiffusion effects.[126]
Decompression is an area where you discover that, the more you learn, the more you know that you really don't know what is going on. For behind the "black-and-white" exactness of table entries, the second-by-second countdowns of dive computers, and beneath the mathematical purity of decompression models, lurks a dark and mysterious physiological jungle that has barely been explored.
— Karl E. Huggins, 1992[128]
Exposure to the various theories, models, tables and algorithms is needed to allow the diver to make educated and knowledgeable decisions regarding their personal decompression needs.[55] Basic decompression theory and use of decompression tables is part of the theory component of training for commercial divers,[129] and dive planning based on decompression tables, and the practice and field management of decompression is a significant part of the work of the diving supervisor.[130][81] Recreational divers are trained in the theory and practice of decompression to the extent that the certifying agency specifies in the training standard for each certification. This may vary from a rudimentary overview sufficient to allow the diver to avoid decompression obligation for entry level divers, to competence in the use of several decompression algorithms by way of personal dive computers, decompression software, and tables for advanced technical divers.[73] The detailed understanding of decompression theory is not generally required of either commercial or recreational divers.
The SAA recommends that you to [sic] take at least the seventh day off to allow your body to off-gas and return to some level of normality