Los fotones del continuo de Lyman (abreviado. LyC), abreviados como fotones del continuo de Ly o fotones Lyc , son los fotones emitidos por estrellas o núcleos galácticos activos con energías fotónicas superiores al límite de Lyman . El hidrógeno se ioniza absorbiendo LyC. A partir del descubrimiento de la luz ultravioleta por Victor Schumann , de 1906 a 1914, Theodore Lyman observó que el hidrógeno atómico absorbe luz sólo en frecuencias (o longitudes de onda ) específicas y, por lo tanto, la serie de Lyman lleva su nombre. [1] [2] Todas las longitudes de onda de la serie Lyman están en la banda ultravioleta. Este comportamiento de absorción cuantificado se produce sólo hasta un límite de energía, conocido como energía de ionización . En el caso del hidrógeno atómico neutro, la energía mínima de ionización es igual al límite de Lyman, donde el fotón tiene energía suficiente para ionizar completamente el átomo, dando como resultado un protón libre y un electrón libre . Por encima de esta energía (por debajo de esta longitud de onda), se pueden absorber todas las longitudes de onda de la luz. Esto forma un continuo en el espectro energético; el espectro es continuo en lugar de estar compuesto por muchas líneas discretas, que se ven a energías más bajas. [3] [4]
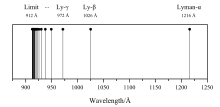
El límite de Lyman se encuentra en la longitud de onda de 91,2 nm (912 Å ), correspondiente a una frecuencia de 3,29 millones de GHz y una energía fotónica de 13,6 eV . [3] Las energías LyC se encuentran principalmente en la porción ultravioleta C del espectro electromagnético (ver serie Lyman ). Aunque los rayos X y los rayos gamma también ionizan un átomo de hidrógeno, son muchos menos los emitidos desde la fotosfera de una estrella : los LyC son predominantemente UV-C. El proceso de absorción de fotones que conduce a la ionización del hidrógeno atómico puede ocurrir a la inversa: un electrón y un protón pueden chocar y formar hidrógeno atómico. Si las dos partículas viajaban lentamente (de modo que se puede ignorar la energía cinética ), entonces el fotón que emite el átomo en el momento de su creación será teóricamente de 13,6 eV (en realidad, la energía será menor si el átomo se forma en un estado excitado). . A velocidades más rápidas, el exceso de energía (cinética) se irradia (pero se debe conservar el impulso ) en forma de fotones de menor longitud de onda (mayor energía). Por lo tanto, los fotones con energías superiores a 13,6 eV son emitidos por la combinación de protones y electrones energéticos que forman hidrógeno atómico y la emisión del hidrógeno fotoionizado .
En un artículo preliminar 1 , el autor ha dado la longitud de onda de más de ciento treinta líneas en la región del espectro que se encuentra entre las valores 1850 y 1030 décimas de metro. Es objeto del presente artículo comparar los resultados obtenidos por el autor con los dados por Schumann; describir el aparato utilizado en esta investigación y llamar la atención sobre algunos hechos nuevos que han salido a la luz desde la publicación del primer aviso.
En la mayoría de las situaciones, la emisión total mediante el proceso libre-libre excede con creces la radiación de recombinación, pero la radiación de recombinación puede introducir rasgos espectrales característicos en los umbrales de ionización en la radiación continua.
Para el hidrógeno, el umbral de ionización más alto, llamado límite de Lyman, corresponde a una energía de 13,6 eV o una longitud de onda de 912 Å.
La radiación de recombinación del hidrógeno en longitudes de onda más cortas que ésta se denomina "continuo de Lyman".
Límite de Lyman El extremo de longitud de onda corta de la serie de Lyman del hidrógeno, a 91,2 nm.
Corresponde a la energía necesaria para que un electrón en el estado fundamental de hidrógeno salte completamente fuera del átomo, dejando el átomo ionizado.