La ley de Davis se utiliza en anatomía y fisiología para describir cómo los tejidos blandos se adaptan a las demandas impuestas. Es similar a la ley de Wolff , que se aplica al tejido óseo . Es un principio fisiológico que establece que los tejidos blandos se curan de acuerdo con la forma en que se someten a un esfuerzo mecánico. [1]
También es una aplicación del modelo Mecanostat de Harold Frost , que se desarrolló originalmente para describir la respuesta adaptativa de los huesos; sin embargo, como lo describe el propio Harold Frost, también se aplica a los tejidos conectivos colágenos fibrosos, como los ligamentos, los tendones y la fascia. [2] [3] La "regla de estiramiento-hipertrofia" de ese modelo establece: "El estiramiento intermitente hace que los tejidos colágenos se hipertrofien hasta que el aumento resultante en la fuerza reduce la elongación en tensión a un nivel mínimo". [4] De manera similar al comportamiento de los tejidos óseos, esta respuesta adaptativa ocurre solo si la tensión mecánica excede un cierto valor umbral. Harold Frost propuso que para los tejidos conectivos colágenos densos los valores umbral relacionados están alrededor de 23 Newton/mm2 o 4% de elongación por deformación. [5]
El término ley de Davis recibe su nombre de Henry Gassett Davis , un cirujano ortopédico estadounidense conocido por su trabajo en el desarrollo de métodos de tracción . Su primera aparición conocida se encuentra en el libro de John Joseph Nutt de 1913, Enfermedades y deformidades del pie , donde Nutt describe la ley citando un pasaje del libro de Davis de 1867, Cirugía conservadora :
Los escritos de Davis sobre el tema exponen una larga cadena de teorías en competencia sobre el tema de la contractura de los tejidos blandos y las causas de la escoliosis . Los comentarios de Davis en Conservative Surgery tenían la forma de una dura reprimenda a las conferencias publicadas por Louis Bauer del Brooklyn Medical and Surgical Institute en 1862. [7] En su escrito, Bauer afirmó que "una contracción de los ligamentos es una imposibilidad fisiológica". [8] Bauer se puso del lado del trabajo publicado en 1851 por Julius Konrad Werner, director del Instituto Ortopédico de Königsberg, Prusia. Bauer y Werner, a su vez, contradecían la investigación publicada por Jacques Mathieu Delpech en 1823. [9] [10]
Los tendones son estructuras de tejido blando que responden a los cambios en la carga mecánica. Las propiedades mecánicas en masa, como el módulo , la deformación por falla y la resistencia máxima a la tracción , disminuyen durante largos períodos de desuso como resultado de cambios microestructurales en el nivel de la fibra de colágeno . En simulaciones de microgravedad , los sujetos de prueba humanos pueden experimentar una pérdida de fuerza del tendón gastrocnemio de hasta el 58% durante un período de 90 días. [11] Los sujetos de prueba a los que se les permitió participar en entrenamiento de resistencia mostraron una magnitud menor de pérdida de fuerza del tendón en el mismo entorno de microgravedad, pero la disminución de la fuerza del módulo aún fue significativa.
Por el contrario, los tendones que han perdido su fuerza original debido a períodos prolongados de inactividad pueden recuperar la mayoría de sus propiedades mecánicas a través de una recarga gradual del tendón, [12] debido a la respuesta del tendón a la carga mecánica. Los eventos de señalización biológica inician el recrecimiento en el sitio, mientras que los estímulos mecánicos promueven aún más la reconstrucción. Este proceso de 6 a 8 semanas da como resultado un aumento de las propiedades mecánicas del tendón hasta que recupera su fuerza original. [13] Sin embargo, la carga excesiva durante el proceso de recuperación puede provocar una falla del material, es decir, desgarros parciales o ruptura completa. Además, los estudios muestran que los tendones tienen un módulo máximo de aproximadamente 800 MPa; por lo tanto, cualquier carga adicional no dará como resultado un aumento significativo en la resistencia del módulo. [12] Estos resultados pueden cambiar las prácticas actuales de fisioterapia, ya que el entrenamiento agresivo del tendón no fortalece la estructura más allá de sus propiedades mecánicas de referencia; por lo tanto, los pacientes siguen siendo tan susceptibles al uso excesivo del tendón y las lesiones.
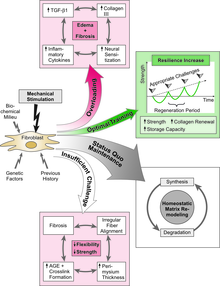
Ley de Davis.