
El splicing alternativo , o splicing alternativo de ARN , o splicing diferencial , es un proceso de splicing alternativo durante la expresión génica que permite que un solo gen produzca diferentes variantes de splicing. Por ejemplo, algunos exones de un gen pueden incluirse dentro del producto de ARN final del gen o excluirse del mismo. [1] Esto significa que los exones se unen en diferentes combinaciones, lo que da lugar a diferentes variantes de splicing. En el caso de los genes codificadores de proteínas, las proteínas traducidas a partir de estas variantes de splicing pueden contener diferencias en su secuencia de aminoácidos y en sus funciones biológicas (véase la Figura).
El empalme alternativo biológicamente relevante ocurre como un fenómeno normal en los eucariotas , donde aumenta la cantidad de proteínas que pueden ser codificadas por el genoma. [1] En los humanos, se cree ampliamente que ~95% de los genes multiexónicos se empalman alternativamente para producir productos alternativos funcionales a partir del mismo gen [2] pero muchos científicos creen que la mayoría de las variantes de empalme observadas se deben a errores de empalme y la cantidad real de genes empalmados alternativamente biológicamente relevantes es mucho menor. [3] [4]
El empalme alternativo se observó por primera vez en 1977. [5] [6] El adenovirus produce cinco transcripciones primarias al principio de su ciclo infeccioso, antes de la replicación del ADN viral, y una adicional más tarde, después de que comienza la replicación del ADN. Las primeras transcripciones primarias continúan produciéndose después de que comienza la replicación del ADN. La transcripción primaria adicional producida al final de la infección es grande y proviene de 5/6 del genoma del adenovirus de 32 kb. Esto es mucho más grande que cualquiera de los ARNm de adenovirus individuales presentes en las células infectadas. Los investigadores descubrieron que la transcripción de ARN primaria producida por el adenovirus tipo 2 en la fase tardía se empalmó de muchas formas diferentes, lo que dio como resultado ARNm que codificaban diferentes proteínas virales. Además, la transcripción primaria contenía múltiples sitios de poliadenilación , lo que daba diferentes extremos 3' para los ARNm procesados. [7] [8] [9]
En 1981 se caracterizó el primer ejemplo de splicing alternativo en una transcripción de un gen endógeno normal . [7] Se descubrió que el gen que codifica la hormona tiroidea calcitonina se empalmaba alternativamente en células de mamíferos. La transcripción primaria de este gen contiene 6 exones; el ARNm de calcitonina contiene los exones 1 a 4 y termina después de un sitio de poliadenilación en el exón 4. Otro ARNm se produce a partir de este pre-ARNm saltando el exón 4, e incluye los exones 1 a 3, 5 y 6. Codifica una proteína conocida como CGRP ( péptido relacionado con el gen de la calcitonina ). [10] [11] También se observaron ejemplos de splicing alternativo en transcripciones de genes de inmunoglobulina en mamíferos a principios de la década de 1980. [7] [12]
Desde entonces, se han encontrado muchos otros ejemplos de empalme alternativo biológicamente relevante en eucariotas. [1] El "poseedor del récord" de empalme alternativo es un gen de D. melanogaster llamado Dscam , que potencialmente podría tener 38.016 variantes de empalme. [13]
En 2021, se descubrió que el genoma del adenovirus tipo 2, el adenovirus en el que se identificó por primera vez el splicing alternativo, era capaz de producir una variedad mucho mayor de variantes de empalme de lo que se creía anteriormente. [14] Mediante el uso de tecnología de secuenciación de próxima generación, los investigadores pudieron actualizar el transcriptoma del adenovirus humano tipo 2 y documentar la presencia de 904 variantes de empalme producidas por el virus a través de un patrón complejo de splicing alternativo. Se ha demostrado que muy pocas de estas variantes de empalme son funcionales, un punto que los autores plantean en su artículo.


En general, se reconocen cinco modos básicos de empalme alternativo. [1] [2] [16] [15]
Además de estos modos primarios de splicing alternativo, existen otros dos mecanismos principales por los cuales se pueden generar diferentes ARNm a partir del mismo gen: múltiples promotores y múltiples sitios de poliadenilación . El uso de múltiples promotores se describe adecuadamente como un mecanismo de regulación transcripcional en lugar de splicing alternativo; al iniciar la transcripción en diferentes puntos, se pueden generar transcripciones con diferentes exones en el extremo 5'. En el otro extremo, múltiples sitios de poliadenilación proporcionan diferentes puntos finales 3' para la transcripción. Ambos mecanismos se encuentran en combinación con el splicing alternativo y proporcionan una variedad adicional en los ARNm derivados de un gen. [1] [16]
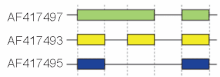
Estos modos describen mecanismos básicos de empalme, pero pueden ser inadecuados para describir eventos de empalme complejos. Por ejemplo, la figura de la derecha muestra 3 formas de empalme del gen de la hialuronidasa 3 del ratón. La comparación de la estructura exónica que se muestra en la primera línea (verde) con la de la segunda línea (amarilla) muestra retención de intrones, mientras que la comparación entre la segunda y la tercera forma de empalme (amarilla vs. azul) muestra omisión de exones. Recientemente se ha propuesto una nomenclatura modelo para designar de forma única todos los posibles patrones de empalme. [15]

Cuando el pre-ARNm se ha transcrito a partir del ADN , incluye varios intrones y exones . (En los nematodos , la media es de 4-5 exones e intrones; en la mosca de la fruta Drosophila puede haber más de 100 intrones y exones en un pre-ARNm transcrito). Los exones que se conservarán en el ARNm se determinan durante el proceso de empalme. La regulación y selección de los sitios de empalme se realiza mediante proteínas activadoras y represoras de empalme que actúan en trans, así como elementos que actúan en cis dentro del propio pre-ARNm, como potenciadores de empalme exónico y silenciadores de empalme exónico.
El intrón nuclear eucariota típico tiene secuencias de consenso que definen regiones importantes. Cada intrón tiene la secuencia GU en su extremo 5'. Cerca del extremo 3' hay un sitio de ramificación. El nucleótido en el punto de ramificación es siempre una A; el consenso en torno a esta secuencia varía un poco. En los humanos, la secuencia de consenso del sitio de ramificación es yUnAy. [18] El sitio de ramificación es seguido por una serie de pirimidinas (el tracto de polipirimidinas ) y luego por AG en el extremo 3'. [16]
El empalme del ARNm se realiza mediante un complejo de ARN y proteína conocido como espliceosoma , que contiene snRNP designados U1, U2 , U4, U5 y U6 (U3 no está involucrado en el empalme del ARNm). [19] U1 se une al GU 5' y U2, con la ayuda de los factores proteicos U2AF , se une al punto de ramificación A dentro del sitio de ramificación. El complejo en esta etapa se conoce como complejo espliceosoma A. La formación del complejo A suele ser el paso clave para determinar los extremos del intrón que se deben empalmar y definir los extremos del exón que se deben conservar. [16] (La nomenclatura U deriva de su alto contenido de uridina).
El complejo U4,U5,U6 se une y U6 reemplaza la posición U1. U1 y U4 se van. El complejo restante realiza entonces dos reacciones de transesterificación . En la primera transesterificación, el extremo 5' del intrón se escinde del exón anterior y se une al sitio de ramificación A mediante un enlace fosfodiéster 2',5' . En la segunda transesterificación, el extremo 3' del intrón se escinde del exón posterior y los dos exones se unen mediante un enlace fosfodiéster. A continuación, el intrón se libera en forma de lazo y se degrada. [1]

El empalme está regulado por proteínas transactivas (represores y activadores) y sitios reguladores cisactivadores correspondientes (silenciadores y potenciadores) en el pre-ARNm. Sin embargo, como parte de la complejidad del empalme alternativo, se observa que los efectos de un factor de empalme dependen frecuentemente de la posición. Es decir, un factor de empalme que actúa como activador del empalme cuando se une a un elemento potenciador intrónico puede actuar como represor cuando se une a su elemento de empalme en el contexto de un exón, y viceversa. [20] La estructura secundaria de la transcripción del pre-ARNm también desempeña un papel en la regulación del empalme, por ejemplo, reuniendo elementos de empalme o enmascarando una secuencia que de otro modo serviría como elemento de unión para un factor de empalme. [21] [22] Juntos, estos elementos forman un "código de empalme" que gobierna cómo se producirá el empalme en diferentes condiciones celulares. [23] [24]
Hay dos tipos principales de elementos de secuencia de ARN que actúan en cis presentes en los pre-ARNm y tienen proteínas de unión al ARN que actúan en trans correspondientes . Los silenciadores de empalme son sitios a los que se unen las proteínas represoras de empalme, lo que reduce la probabilidad de que un sitio cercano se use como unión de empalme. Estos pueden estar ubicados en el propio intrón (silenciadores de empalme intrónico, ISS) o en un exón vecino ( silenciadores de empalme exónico , ESS). Varían en secuencia, así como en los tipos de proteínas que se unen a ellos. La mayoría de los represores de empalme son ribonucleoproteínas nucleares heterogéneas (hnRNP) como hnRNPA1 y la proteína de unión al tracto de polipirimidina (PTB). [16] [23] Los potenciadores de empalme son sitios a los que se unen las proteínas activadoras de empalme, lo que aumenta la probabilidad de que un sitio cercano se use como unión de empalme. Estos también pueden ocurrir en el intrón (potenciadores de empalme intrónico, ISE) o en el exón ( potenciadores de empalme exónico , ESE). La mayoría de las proteínas activadoras que se unen a los ISE y ESE son miembros de la familia de proteínas SR . Dichas proteínas contienen motivos de reconocimiento de ARN y dominios ricos en arginina y serina (RS). [16] [23]

En general, los determinantes del empalme funcionan de una manera interdependiente que depende del contexto, de modo que las reglas que gobiernan cómo se regula el empalme forman un código de empalme. [24] La presencia de un elemento particular de la secuencia de ARN que actúa en cis puede aumentar la probabilidad de que un sitio cercano se empalme en algunos casos, pero disminuir la probabilidad en otros casos, dependiendo del contexto. El contexto dentro del cual actúan los elementos reguladores incluye el contexto que actúa en cis que se establece por la presencia de otras características de la secuencia de ARN y el contexto que actúa en trans que se establece por las condiciones celulares. Por ejemplo, algunos elementos de la secuencia de ARN que actúan en cis influyen en el empalme solo si hay múltiples elementos presentes en la misma región para establecer el contexto. Como otro ejemplo, un elemento que actúa en cis puede tener efectos opuestos en el empalme, dependiendo de qué proteínas se expresen en la célula (por ejemplo, PTB neuronal versus no neuronal). La importancia adaptativa de los silenciadores y potenciadores del empalme está atestiguada por estudios que muestran que existe una fuerte selección en los genes humanos contra las mutaciones que producen nuevos silenciadores o alteran los potenciadores existentes. [25] [26]

Los pre-ARNm del gen dsx de D. melanogaster contienen 6 exones. En los machos, los exones 1, 2, 3, 5 y 6 se unen para formar el ARNm, que codifica una proteína reguladora de la transcripción necesaria para el desarrollo masculino. En las hembras, los exones 1, 2, 3 y 4 se unen, y una señal de poliadenilación en el exón 4 provoca la escisión del ARNm en ese punto. El ARNm resultante es una proteína reguladora de la transcripción necesaria para el desarrollo femenino. [27]
Este es un ejemplo de omisión de exón. El intrón aguas arriba del exón 4 tiene un tracto de polipirimidina que no coincide bien con la secuencia de consenso , de modo que las proteínas U2AF se unen mal a él sin la ayuda de activadores de empalme. Por lo tanto, este sitio aceptor de empalme 3' no se utiliza en los machos. Las hembras, sin embargo, producen el activador de empalme Transformer (Tra) (ver más abajo). La proteína SR Tra2 se produce en ambos sexos y se une a un ESE en el exón 4; si Tra está presente, se une a Tra2 y, junto con otra proteína SR, forma un complejo que ayuda a las proteínas U2AF a unirse al tracto de polipirimidina débil. U2 es reclutado al punto de ramificación asociado, y esto conduce a la inclusión del exón 4 en el ARNm. [27] [28]
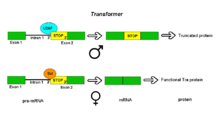
Los pre-ARNm del gen Transformer (Tra) de Drosophila melanogaster experimentan un empalme alternativo a través del modo de sitio aceptor alternativo. El gen Tra codifica una proteína que se expresa solo en hembras. La transcripción primaria de este gen contiene un intrón con dos posibles sitios aceptores. En los machos, se utiliza el sitio aceptor aguas arriba. Esto hace que se incluya una versión más larga del exón 2 en la transcripción procesada, incluido un codón de terminación temprano . El ARNm resultante codifica un producto proteico truncado que está inactivo. Las hembras producen la proteína maestra de determinación sexual Sex lethal (Sxl). La proteína Sxl es un represor de empalme que se une a una ISS en el ARN de la transcripción Tra cerca del sitio aceptor aguas arriba, lo que evita que la proteína U2AF se una al tracto de polipirimidina. Esto evita el uso de esta unión, desplazando la unión del espliceosoma al sitio aceptor aguas abajo. El empalme en este punto pasa por alto el codón de terminación, que se escinde como parte del intrón. El ARNm resultante codifica una proteína Tra activa, que a su vez es un regulador del empalme alternativo de otros genes relacionados con el sexo (ver dsx arriba). [1]

Se producen múltiples isoformas de la proteína del receptor Fas mediante empalme alternativo. Dos isoformas que se dan normalmente en los seres humanos se producen mediante un mecanismo de omisión de exón. Un ARNm que incluye el exón 6 codifica la forma unida a la membrana del receptor Fas, que promueve la apoptosis o muerte celular programada. El aumento de la expresión del receptor Fas en las células de la piel expuestas crónicamente al sol y la ausencia de expresión en las células del cáncer de piel sugieren que este mecanismo puede ser importante en la eliminación de células precancerosas en los seres humanos. [29] Si se omite el exón 6, el ARNm resultante codifica una proteína Fas soluble que no promueve la apoptosis. La inclusión o la omisión del exón depende de dos proteínas antagonistas, TIA-1 y la proteína de unión al tracto de polipirimidina (PTB).
Este mecanismo es un ejemplo de definición de exón en el splicing. Un spliceosoma se ensambla en un intrón y las subunidades snRNP pliegan el ARN de manera que los extremos 5' y 3' del intrón se unen. Sin embargo, ejemplos estudiados recientemente como este muestran que también hay interacciones entre los extremos del exón. En este caso particular, estas interacciones de definición de exón son necesarias para permitir la unión de factores de splicing centrales antes del ensamblaje de los spliceosomas en los dos intrones flanqueantes. [30]

El VIH , el retrovirus que causa el SIDA en los seres humanos, produce una única transcripción primaria de ARN, que se empalma alternativamente de múltiples maneras para producir más de 40 ARNm diferentes. [31] El equilibrio entre las transcripciones empalmadas diferencialmente proporciona múltiples ARNm que codifican diferentes productos que son necesarios para la multiplicación viral. [32] Una de las transcripciones empalmadas diferencialmente contiene el gen tat , en el que el exón 2 es un exón de casete que puede omitirse o incluirse. La inclusión del exón 2 de tat en el ARN está regulada por la competencia entre el represor de empalme hnRNP A1 y la proteína SR SC35. Dentro del exón 2 se superponen una secuencia silenciadora de empalme exónico (ESS) y una secuencia potenciadora de empalme exónico (ESE). Si la proteína represora A1 se une al ESS, inicia la unión cooperativa de múltiples moléculas A1, extendiéndose hacia el sitio donante 5' aguas arriba del exón 2 y evitando la unión del factor de empalme central U2AF35 al tracto de polipirimidina. Si SC35 se une al ESE, evita la unión de A1 y mantiene el sitio donante 5' en un estado accesible para el ensamblaje del espliceosoma. La competencia entre el activador y el represor asegura que se produzcan ambos tipos de ARNm (con y sin exón 2). [31]
El empalme alternativo genuino se produce tanto en genes codificantes de proteínas como en genes no codificantes para producir múltiples productos (proteínas o ARN no codificantes). Se necesita información externa para decidir qué producto se obtiene, dada una secuencia de ADN y la transcripción inicial. Dado que los métodos de regulación son hereditarios, esto proporciona nuevas formas para que las mutaciones afecten la expresión genética. [33]
El empalme alternativo puede proporcionar flexibilidad evolutiva. Una única mutación puntual puede hacer que un exón determinado se excluya o incluya ocasionalmente de una transcripción durante el empalme, lo que permite la producción de una nueva isoforma de proteína sin pérdida de la proteína original. [1] Los estudios han identificado regiones intrínsecamente desordenadas (ver Proteínas intrínsecamente no estructuradas ) como enriquecidas en los exones no constitutivos [34], lo que sugiere que las isoformas de proteínas pueden mostrar diversidad funcional debido a la alteración de los módulos funcionales dentro de estas regiones. Dicha diversidad funcional lograda por las isoformas se refleja en sus patrones de expresión y se puede predecir mediante enfoques de aprendizaje automático. [35] [36] Los estudios comparativos indican que el empalme alternativo precedió a la multicelularidad en la evolución y sugieren que este mecanismo podría haber sido cooptado para ayudar en el desarrollo de organismos multicelulares. [37]
Las investigaciones basadas en el Proyecto Genoma Humano y otras secuenciaciones genómicas han demostrado que los humanos tienen solo un 30% más de genes que el gusano redondo Caenorhabditis elegans , y solo el doble que la mosca Drosophila melanogaster . Este hallazgo llevó a la especulación de que la mayor complejidad percibida de los humanos, o de los vertebrados en general, podría deberse a tasas más altas de empalme alternativo en los humanos que las que se encuentran en los invertebrados. [38] [39] Sin embargo, un estudio sobre muestras de 100.000 etiquetas de secuencia expresada (EST) de humanos, ratones, ratas, vacas, moscas ( D. melanogaster ), gusanos ( C. elegans ) y la planta Arabidopsis thaliana no encontró grandes diferencias en la frecuencia de genes empalmados alternativamente entre los humanos y cualquiera de los otros animales probados. [40] Sin embargo, otro estudio propuso que estos resultados eran un artefacto de los diferentes números de EST disponibles para los diversos organismos. Cuando compararon frecuencias de empalme alternativo en subconjuntos aleatorios de genes de cada organismo, los autores concluyeron que los vertebrados tienen tasas más altas de empalme alternativo que los invertebrados. [41]
Los cambios en la maquinaria de procesamiento del ARN pueden provocar un empalme incorrecto de múltiples transcripciones, mientras que las alteraciones de un solo nucleótido en los sitios de empalme o en los sitios reguladores del empalme que actúan en cis pueden provocar diferencias en el empalme de un solo gen y, por lo tanto, en el ARNm producido a partir de las transcripciones de un gen mutante. Un estudio de 2005 que incluía análisis probabilísticos indicó que más del 60% de las mutaciones que causan enfermedades humanas afectan al empalme en lugar de afectar directamente a las secuencias codificantes. [42] Un estudio más reciente indica que es probable que un tercio de todas las enfermedades hereditarias tengan un componente de empalme. [20] Independientemente del porcentaje exacto, existen varias enfermedades relacionadas con el empalme. [43] Como se describe a continuación, un ejemplo destacado de enfermedades relacionadas con el empalme es el cáncer.
Los ARNm empalmados anormalmente también se encuentran en una alta proporción de células cancerosas. [44] [45] [46] Los análisis combinados de RNA-Seq y proteómica han revelado una sorprendente expresión diferencial de isoformas de empalme de proteínas clave en vías importantes del cáncer. [47] No siempre está claro si estos patrones aberrantes de empalme contribuyen al crecimiento canceroso o son simplemente consecuencia de anomalías celulares asociadas con el cáncer. Para ciertos tipos de cáncer, como el colorrectal y el de próstata, se ha demostrado que el número de errores de empalme por cáncer varía mucho entre cánceres individuales, un fenómeno conocido como inestabilidad del transcriptoma . [48] [49] Además, se ha demostrado que la inestabilidad del transcriptoma se correlaciona en gran medida con un nivel de expresión reducido de genes de factores de empalme. Se ha demostrado que la mutación de DNMT3A contribuye a las neoplasias hematológicas y que las líneas celulares mutadas en DNMT3A exhiben inestabilidad del transcriptoma en comparación con sus contrapartes de tipo salvaje isogénicas. [50]
De hecho, en realidad hay una reducción del empalme alternativo en las células cancerosas en comparación con las normales, y los tipos de empalme difieren; por ejemplo, las células cancerosas muestran niveles más altos de retención de intrones que las células normales, pero niveles más bajos de omisión de exones. [51] Algunas de las diferencias en el empalme en células cancerosas pueden deberse a la alta frecuencia de mutaciones somáticas en los genes de factores de empalme, [46] y algunas pueden resultar de cambios en la fosforilación de factores de empalme que actúan en trans. [33] Otras pueden producirse por cambios en las cantidades relativas de factores de empalme producidos; por ejemplo, se ha demostrado que las células de cáncer de mama tienen niveles aumentados del factor de empalme SF2/ASF . [52] Un estudio encontró que un porcentaje relativamente pequeño (383 de más de 26000) de variantes de empalme alternativo tenían una frecuencia significativamente mayor en las células tumorales que en las células normales, lo que sugiere que hay un conjunto limitado de genes que, cuando se empalman incorrectamente, contribuyen al desarrollo de tumores. [53] Sin embargo, se cree que los efectos nocivos de las transcripciones empalmadas incorrectamente suelen estar protegidos y eliminados por un mecanismo de control de calidad postranscripcional celular denominado desintegración del ARNm mediada por sinsentidos [NMD]. [54]
Un ejemplo de una variante de empalme específica asociada con los cánceres se encuentra en uno de los genes DNMT humanos . Tres genes DNMT codifican enzimas que añaden grupos metilo al ADN, una modificación que a menudo tiene efectos reguladores. Varios ARNm DNMT3B empalmados de forma anormal se encuentran en tumores y líneas celulares cancerosas. En dos estudios separados, la expresión de dos de estos ARNm empalmados de forma anormal en células de mamíferos provocó cambios en los patrones de metilación del ADN en esas células. Las células con uno de los ARNm anormales también crecieron dos veces más rápido que las células de control, lo que indica una contribución directa al desarrollo del tumor por parte de este producto. [33]
Otro ejemplo es el protooncogén Ron ( MST1R ) . Una propiedad importante de las células cancerosas es su capacidad de moverse e invadir el tejido normal. Se ha descubierto que la producción de una transcripción empalmada de manera anormal de Ron está asociada con mayores niveles de SF2/ASF en las células de cáncer de mama. La isoforma anormal de la proteína Ron codificada por este ARNm conduce a la motilidad celular . [52]
La sobreexpresión de una variante de empalme truncada del gen FOSB – ΔFosB – en una población específica de neuronas en el núcleo accumbens se ha identificado como el mecanismo causal involucrado en la inducción y mantenimiento de una adicción a las drogas y las recompensas naturales . [55] [56] [57] [58]
Estudios recientes y provocadores apuntan a una función clave de la estructura de la cromatina y las modificaciones de las histonas en la regulación del splicing alternativo. Estos hallazgos sugieren que la regulación epigenética determina no solo qué partes del genoma se expresan, sino también cómo se empalman. [59]
El análisis de empalme alternativo a nivel del transcriptoma se realiza normalmente mediante secuenciación de ARN de alto rendimiento. Lo más habitual es que se realice mediante secuenciación de lectura corta, como la que se realiza con instrumentación Illumina. Pero resulta aún más informativo que esto se haga mediante secuenciación de lectura larga, como la que se realiza con instrumentación Nanopore o PacBio. Los análisis a nivel del transcriptoma se pueden utilizar, por ejemplo, para medir la cantidad de empalme alternativo desviado, como en una cohorte de pacientes con cáncer. [60]
Las tecnologías de secuenciación profunda se han utilizado para realizar análisis de todo el genoma de ARNm procesados y no procesados, lo que ha proporcionado información sobre el empalme alternativo. Por ejemplo, los resultados del uso de la secuenciación profunda indican que, en los seres humanos, se estima que el 95 % de las transcripciones de genes multiexónicos sufren un empalme alternativo, y varias transcripciones de pre-ARNm se empalman de una manera específica para cada tejido. [2] También se han desarrollado enfoques computacionales y genómicos funcionales basados en el aprendizaje de múltiples instancias para integrar datos de secuenciación de ARN para predecir funciones de isoformas empalmadas de manera alternativa. [36] La secuenciación profunda también ha ayudado a la detección in vivo de los lazos transitorios que se liberan durante el empalme, la determinación de secuencias de sitios de ramificación y el mapeo a gran escala de puntos de ramificación en transcripciones de pre-ARNm humanas. [61]
Más históricamente, se han encontrado transcripciones empalmadas alternativamente comparando secuencias de EST , pero esto requiere la secuenciación de un gran número de EST. La mayoría de las bibliotecas de EST provienen de un número muy limitado de tejidos, por lo que es probable que se pasen por alto variantes de empalme específicas de tejido en cualquier caso. Sin embargo, se han desarrollado enfoques de alto rendimiento para investigar el empalme, como: análisis basados en microarrays de ADN , ensayos de unión de ARN y secuenciación profunda . Estos métodos se pueden utilizar para detectar polimorfismos o mutaciones en o alrededor de elementos de empalme que afectan la unión de proteínas. Cuando se combinan con ensayos de empalme, incluidos ensayos de genes reporteros in vivo , se pueden analizar los efectos funcionales de los polimorfismos o mutaciones en el empalme de transcripciones de pre-ARNm. [20] [23] [62]
En el análisis de microarrays, se han utilizado arrays de fragmentos de ADN que representan exones individuales ( por ejemplo, microarray de exones de Affymetrix ) o límites exón/exón ( por ejemplo, arrays de ExonHit o Jivan ). Luego, el array se sondea con ADNc marcado de tejidos de interés. Los ADNc de sonda se unen al ADN de los exones que están incluidos en los ARNm en su tejido de origen, o al ADN del límite donde se han unido dos exones. Esto puede revelar la presencia de ARNm empalmados alternativamente particulares. [63]
CLIP ( entrecruzamiento e inmunoprecipitación ) utiliza radiación UV para unir proteínas a moléculas de ARN en un tejido durante el empalme. Luego, se precipita una proteína reguladora del empalme que actúa en trans de interés utilizando anticuerpos específicos. Cuando se aísla y clona el ARN unido a esa proteína, revela las secuencias diana para esa proteína. [64] Otro método para identificar proteínas de unión al ARN y mapear su unión a transcripciones de pre-ARNm es "Microarray Evaluation of Genomic Aptamers by shift (MEGAshift)".net [65] Este método implica una adaptación del método "Systematic Evolution of Ligands by Exponential Enrichment (SELEX)" [66] junto con una lectura basada en microarrays. El uso del método MEGAshift ha proporcionado información sobre la regulación del empalme alternativo al permitir la identificación de secuencias en transcripciones de pre-ARNm que rodean exones empalmados alternativamente que median la unión a diferentes factores de empalme, como ASF/SF2 y PTB. [67] Este enfoque también se ha utilizado para ayudar a determinar la relación entre la estructura secundaria del ARN y la unión de factores de empalme. [22]
El uso de ensayos de reporteros permite encontrar las proteínas de empalme involucradas en un evento de empalme alternativo específico mediante la construcción de genes reporteros que expresarán una de dos proteínas fluorescentes diferentes según la reacción de empalme que ocurra. Este método se ha utilizado para aislar mutantes que afectan el empalme y, por lo tanto, para identificar nuevas proteínas reguladoras del empalme inactivadas en esos mutantes. [64]
Los recientes avances en la predicción de la estructura de las proteínas han facilitado el desarrollo de nuevas herramientas para la anotación genómica y el análisis de empalmes alternativos. Por ejemplo, isoform.io, una plataforma guiada por predicciones de la estructura de las proteínas, ha evaluado cientos de miles de isoformas de genes codificantes de proteínas humanas ensambladas a partir de numerosos experimentos de secuenciación de ARN en una variedad de tejidos humanos. Este análisis exhaustivo ha llevado a la identificación de numerosas isoformas con una estructura predicha con mayor confianza y una función potencialmente superior en comparación con las isoformas canónicas en la última base de datos de genes humanos. Al integrar las predicciones estructurales con la expresión y la evidencia evolutiva, este enfoque ha demostrado el potencial de la predicción de la estructura de las proteínas como una herramienta para refinar la anotación del genoma humano. [68]
Existe una colección de bases de datos de empalme alternativo. [69] [70] [71] Estas bases de datos son útiles para encontrar genes que tienen pre-ARNm que experimentan empalme alternativo y eventos de empalme alternativo o para estudiar el impacto funcional del empalme alternativo.
A PESAR DE LA IMPORTANCIA DE NUMEROSOS FACTORES PSICOSOCIALES, EN SU BASE, LA ADICCIÓN A LAS DROGAS IMPLICA UN PROCESO BIOLÓGICO: la capacidad de la exposición repetida a una droga de abuso para inducir cambios en un cerebro vulnerable que impulsan la búsqueda y el consumo compulsivo de drogas, y la pérdida de control sobre el consumo de drogas, que definen un estado de adicción. ... Una gran cantidad de literatura ha demostrado que dicha inducción de ΔFosB en las neuronas NAc de tipo D1 aumenta la sensibilidad de un animal al fármaco, así como a las recompensas naturales, y promueve la autoadministración del fármaco, presumiblemente a través de un proceso de refuerzo positivo.
ΔFosB es un factor de transcripción esencial implicado en las vías moleculares y conductuales de la adicción después de la exposición repetida a drogas. La formación de ΔFosB en múltiples regiones cerebrales y la vía molecular que conduce a la formación de complejos AP-1 se entienden bien. El establecimiento de un propósito funcional para ΔFosB ha permitido una mayor determinación de algunos de los aspectos clave de sus cascadas moleculares, que involucran efectores como GluR2 (87,88), Cdk5 (93) y NFkB (100). Además, muchos de estos cambios moleculares identificados ahora están directamente relacionados con los cambios estructurales, fisiológicos y conductuales observados después de la exposición crónica a drogas (60,95,97,102). Los estudios epigenéticos han abierto nuevas fronteras de investigación que investigan los roles moleculares de ΔFosB, y los avances recientes han ilustrado el papel de ΔFosB actuando sobre el ADN y las histonas, realmente como un
interruptor molecular
(34). Como consecuencia de nuestra mejor comprensión de ΔFosB en la adicción, es posible evaluar el potencial adictivo de los medicamentos actuales (119), así como usarlo como un biomarcador para evaluar la eficacia de las intervenciones terapéuticas (121,122,124). Algunas de estas intervenciones propuestas tienen limitaciones (125) o están en sus primeras etapas (75). Sin embargo, se espera que algunos de estos hallazgos preliminares puedan conducir a tratamientos innovadores, que son muy necesarios en el ámbito de la adicción.
Por estas razones, ΔFosB se considera un factor de transcripción primario y causal en la creación de nuevas conexiones neuronales en el centro de recompensa, la corteza prefrontal y otras regiones del sistema límbico. Esto se refleja en el nivel aumentado, estable y duradero de sensibilidad a la cocaína y otras drogas, y la tendencia a la recaída incluso después de largos períodos de abstinencia. Estas redes recién construidas funcionan de manera muy eficiente a través de nuevas vías tan pronto como se siguen consumiendo drogas de abuso.