Las ADN topoisomerasas (o topoisomerasas ) son enzimas que catalizan cambios en el estado topológico del ADN , interconvirtiendo formas relajadas y superenrolladas, especies unidas (catenadas) y no unidas, y ADN anudado y no anudado. [1] [2] Los problemas topológicos en el ADN surgen debido a la naturaleza entrelazada de su estructura de doble hélice, que, por ejemplo, puede provocar un enrollamiento excesivo del dúplex de ADN durante la replicación y transcripción del ADN . Si no se modifica, esta torsión eventualmente impediría que las ADN o ARN polimerasas involucradas en estos procesos continúen a lo largo de la hélice del ADN. Un segundo desafío topológico resulta del enlace o enredo del ADN durante la replicación. Si no se resuelven, los vínculos entre el ADN replicado impedirán la división celular. Las ADN topoisomerasas previenen y corrigen este tipo de problemas topológicos. Lo hacen uniéndose al ADN y cortando la columna vertebral de azúcar-fosfato de una (topoisomerasas tipo I) o de ambas (topoisomerasas tipo II) de las cadenas de ADN. Esta ruptura transitoria permite que el ADN se desenrede o desenrolle y, al final de estos procesos, se vuelve a sellar la columna vertebral del ADN. Dado que la composición química general y la conectividad del ADN no cambian, el sustrato y el producto del ADN son isómeros químicos que difieren sólo en su topología.
La primera ADN topoisomerasa fue descubierta en bacterias por James C. Wang en 1971 y inicialmente recibió el nombre de proteína ω (omega); [3] ahora se llama topoisomerasa I (topo I) de Escherichia coli ( E. coli ) y es un representante de la familia de enzimas tipo IA. Posteriormente, James Champoux y Renato Dulbecco encontraron una actividad similar en células eucariotas (hígado de rata) ; [4] la enzima responsable, la topo I eucariota, tiene un mecanismo distinto y es representativa de la familia tipo IB. La primera topoisomerasa de tipo II descubierta fue la ADN girasa de bacterias, por Martin Gellert y colaboradores en 1976, [5] y también caracterizada por Nicholas Cozzarelli y colaboradores. [6] La ADN girasa cataliza la introducción de superenrollamientos negativos en el ADN y es la única enzima de tipo II que hace esto; todas las demás catalizan la relajación del ADN. Las enzimas de tipo II son mecánicamente distintas de las de tipo I porque dependen de ATP y escinden transitoriamente ambas cadenas de ADN en lugar de solo una. Posteriormente se identificaron topoisomerasas de tipo II a partir de virus bacterianos y eucariotas. [7] [8] [9] Los códigos Topo EC son los siguientes: independiente de ATP (tipo I), EC 5.6.2.1; Dependiente de ATP (tipo II): EC 5.6.2.2. La excepción entre las topoisomerasas de tipo I, la girasa inversa, que contiene un dominio helicasa (EC 3.6.4.12) e introduce un superenrollamiento positivo de manera dependiente de ATP. Por lo tanto, es la única topoisomerasa de tipo I clasificada como EC 5.6.2.2 (Tabla 1).
La estructura de doble hélice del ADN implica el entrelazamiento de las dos cadenas de polinucleótidos entre sí, lo que potencialmente da lugar a problemas topológicos. La topología del ADN se refiere al cruce de las dos hebras de ADN que altera la torsión de la doble hélice y da lugar a conformaciones terciarias del ADN, como superenrollamientos, nudos y catenanos. [10] Los posibles problemas topológicos asociados con la estructura de doble hélice del ADN se reconocieron poco después de que James Watson, Francis Crick y Rosalind Franklin dilucidaran por primera vez su estructura en 1953 [11] [12] [13] y se desarrollaron aún más mediante el trabajo. de Max Delbruck y John Cairns. [14] [15] El ADN bicatenario de círculo cerrado se puede describir mediante 3 parámetros: número de enlace (Lk), torsión (Tw) y contorsión (Wr) (Fig. 1). Donde Lk se refiere al número de veces que se unen las dos hebras, Tw se refiere al número de vueltas helicoidales en el ADN, medidas en relación con el eje helicoidal, y Wr cuantifica el enrollamiento de la trayectoria de la hélice del ADN en el espacio y, a menudo, se equiparado con "superenrollamiento".

Los 3 parámetros están relacionados de la siguiente manera: Lk = Tw +Wr. Esta es una identidad matemática obtenida originalmente por Călugăreanu en 1959 [16] y se conoce como teorema de Călugăreanu o Călugăreanu-White-Fuller. [17] [18] Lk no se puede alterar sin romper una o ambas hebras de la hélice; Tw y Wr son interconvertibles y dependen de las condiciones de la solución. Superenrollamiento es un término vernáculo para el ADN con una diferencia de enlace distinta de cero, más correctamente denominado diferencia de enlace específica (σ = ΔLk/Lk 0 , donde Lk 0 es el número de enlace medio del círculo de ADN relajado). Se dice que el ADN está superenrollado positivamente si su Lk es mayor que Lk 0 para el estado relajado (Lk-Lk o = ΔLk, ΔLk>0); eso significa que Tw y/o Wr aumentan en relación con la molécula relajada. Por el contrario, el ADN está superenrollado negativamente si la Lk de la molécula es inferior a la Lk 0 (ΔLk<0).
Las consecuencias de las perturbaciones topológicas en el ADN se ejemplifican en la replicación del ADN durante la cual se separan las hebras del dúplex; esta separación conduce a la formación de superenrollamientos positivos (ADN sobreenrollado o sobretorcido) delante de la bifurcación de replicación y entrelazamiento de las hebras hijas (precatenanes) detrás [10] [19] (Fig. 2). Si las superenrollamientos positivas no se relajan, se impide la progresión de la bifurcación de replicación, mientras que la falta de desconexión de las cadenas hijas impide la segregación del genoma, que es necesaria para la división celular. [20] La transcripción mediante ARN polimerasa también genera un superenrollamiento positivo delante y un superenrollamiento negativo detrás del complejo transcripcional (Fig. 2). Este efecto se conoce como modelo de dominio gemelo superenrollado, como lo describieron Leroy Liu y James Wang en 1987. [21] Estas perturbaciones topológicas deben resolverse para que el metabolismo del ADN continúe, permitiendo a la célula replicar, transcribir y dividir el genoma de manera eficiente. para permitir la división celular y la vitalidad. Los nudos en el ADN se pueden encontrar en bacteriófagos y como productos de reacciones de recombinación. [10] En general, los nudos en el ADN son perjudiciales y deben eliminarse (mediante topoisomerasas). Los catenanos de ADN se forman durante la replicación de moléculas circulares y deben resolverse mediante topoisomerasas o recombinasas para permitir la separación adecuada de las moléculas hijas durante la división celular. Además de los aspectos perjudiciales de la topología del ADN que requieren resolución, también existen aspectos beneficiosos. Por ejemplo, la replicación del plásmido requiere un superenrollamiento negativo del origen, lo que facilita la fusión local y expone el ADN monocatenario necesario para iniciar la replicación. De manera similar, el inicio de la replicación desde el origen bacteriano principal oriC también requiere un superenrollamiento negativo. [22] [23] Además, la compactación del genoma de E. coli se logra en parte mediante superenrollamiento negativo.

Las ADN topoisomerasas son enzimas que han evolucionado para resolver problemas topológicos en el ADN (Tabla 2). [10] Lo hacen mediante la rotura transitoria de una o ambas cadenas de ADN. Esto ha llevado a la clasificación de topos en dos tipos: tipo I, que cataliza reacciones que implican roturas monocatenarias transitorias, y tipo II, que cataliza reacciones que implican roturas bicatenarias transitorias (Fig. 3; Tabla 2). Existen subtipos dentro de estas clasificaciones.
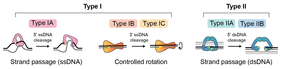
Estas enzimas catalizan cambios en la topología del ADN mediante roturas monocatenarias transitorias en el ADN. Las reacciones pueden ocurrir en sustratos de ADN tanto monocatenarios como bicatenarios y pueden proceder mediante un mecanismo de "giro" o de "paso de cadena" (Fig. 3). La gama de reacciones incluye: relajación del superenrollamiento del ADN, desanudado de círculos monocatenarios y decatenación, siempre que al menos uno de los socios tenga una región monocatenaria. En el caso de la enzima arqueal, la girasa inversa, es posible un superenrollamiento positivo del ADN. [24]
Los tipos IA son monoméricos y se unen a segmentos monocatenarios de ADN. Introducen una ruptura monocatenaria transitoria mediante la formación de un enlace tirosil-fosfato entre una tirosina en la enzima y un 5′-fosfato en el ADN. El segmento de ADN dentro del cual se produce la ruptura se llama "puerta" o segmento G, y su escisión permite el paso de otro segmento de ADN, el "transporte" o segmento T, que pasa a través de una "cadena". proceso de paso. [25] A esto le sigue la ligadura del segmento G. Para que se produzca el paso de la cadena, la topo IA debe sufrir un cambio conformacional para abrir la puerta del ADN y permitir la transferencia del segmento T. Durante una reacción de relajación del ADN, este proceso cambia el número de enlace del ADN en +/-1 (Fig. 4). Ejemplos de topoisomerasas de tipo IA incluyen la topo I y III procariótica, la topo IIIα y IIIβ eucariota y la enzima arqueal girasa inversa. La girasa inversa, que se produce en arqueas termófilas, comprende un topo tipo IA acoplado a una helicasa y es la única enzima conocida que puede introducir superenrollamientos positivos en el ADN. [24] El gen que codifica la girasa inversa también se encuentra en algunos grupos de bacterias termófilas, donde probablemente fue transferido mediante transferencia horizontal de genes desde Archaea. [26]

Las topoisomerasas de tipo IB catalizan reacciones que implican roturas monocatenarias transitorias en el ADN mediante la formación de un enlace tirosil-fosfato entre una tirosina en la enzima y un 3'-fosfato en el ADN. En lugar de utilizar un mecanismo de paso de cadena, estas enzimas operan mediante un "giro" o "rotación controlada" de la cadena escindida alrededor de la cadena intacta. [27] Este mecanismo de rotación controlada se describió por primera vez para Vaccinia topo I [27] [28] y permite la rotación del extremo libre del ADN alrededor de la hebra intacta; la velocidad se controla mediante la "fricción" dentro de la cavidad de la enzima, antes de que se produzca la mella. se vuelve a ligar (Fig. 3). Esto da como resultado un cambio variable del número de enlaces por evento de escisión y religación. Este mecanismo es distinto del de las enzimas de tipo IA, y los dos grupos de enzimas no están relacionados estructural ni evolutivamente. Ejemplos de topoisomerasas de tipo IB incluyen la topo I nuclear y mitocondrial eucariota además de la topo I viral , aunque se han identificado en los tres dominios de la vida.
Las topoisomerasas de tipo IC comparten un mecanismo similar a las enzimas de tipo IB pero son estructuralmente distintas. El único representante es el topo V, que se encuentra en el hipertermófilo Methanopyrus kandleri . [29]
Las topoisomerasas de tipo II catalizan cambios en la topología del ADN mediante roturas transitorias de doble cadena en el ADN. Las reacciones ocurren en sustratos de ADN de doble hebra y se desarrollan mediante un mecanismo de paso de hebra (Fig. 5). La gama de reacciones incluye relajación del ADN, superenrollamiento del ADN, desanudado y decatenación. Mientras que todas las topoisomerasas de tipo II pueden catalizar la relajación del ADN, la girasa, una topoisomerasa bacteriana arquetípica, también puede introducir superenrollamientos negativos. A diferencia de las topoisomerasas de tipo I que son generalmente monoméricas, las topoisomerasas de tipo II son homodímeros o heterotetrámeros. Se clasifican en dos subtipos según consideraciones evolutivas, estructurales y mecanicistas. El mecanismo general de paso de cadena para el topos tipo II comienza con la unión de un dúplex de ADN, denominado segmento de puerta (segmento G), en la puerta del ADN. Otro dúplex, denominado segmento de transporte (segmento T), es capturado por una pinza operada por ATP y pasa a través de una ruptura transitoria en el segmento G, que involucra enlaces 5' fosfotirosina en ambas hebras, antes de ser liberado a través de la puerta C. y se vuelve a ligar el segmento G (Fig. 5). El recambio enzimático requiere la unión e hidrólisis del ATP.

Las topoisomerasas de tipo IIA catalizan roturas transitorias de doble hebra en el ADN mediante la formación de enlaces tirosil-fosfato entre las tirosinas de la enzima (una en cada subunidad) y los 5'-fosfatos escalonados por 4 bases en hebras opuestas de ADN. La reacción de paso de la hebra puede ser intra o intermolecular (Fig. 5), lo que permite cambios en el superenrollamiento y el anudamiento o desconexión, respectivamente. Este proceso cambia el número de enlace del ADN en +/-2. Ejemplos de topoisomerasas de tipo IIA incluyen topo IIα y topo IIβ eucariotas , además de girasa bacteriana y topo IV. La ADN girasa sigue el mismo mecanismo de paso de doble hebra que otras enzimas de tipo II, pero tiene características únicas relacionadas con su capacidad para introducir superenrollamientos negativos en el ADN. El segmento G es parte de un trozo de ADN mucho más largo (>100 pb) que está envuelto alrededor de la enzima, uno de cuyos brazos forma el segmento T que pasa a través de la rotura de doble cadena (Fig. 5). En el caso de la girasa, una cantidad sustancial de la energía libre procedente de la hidrólisis del ATP se transforma en tensión de torsión en el ADN, es decir, el superenrollamiento es un proceso que requiere energía. [30] Además, en ausencia de ATP, la girasa es capaz de eliminar superenrollamientos negativos en una reacción de relajación del ADN más lenta.
El tipo IIB también cataliza roturas bicatenarias transitorias mediante la formación de enlaces tirosil-fosfato entre tirosinas en la enzima y 5'-fosfatos en hebras opuestas del ADN, pero en el caso de las enzimas IIB las roturas bicatenarias tienen un efecto 2- tambaleo de base. Las enzimas de tipo IIB muestran importantes diferencias estructurales, pero están relacionadas evolutivamente con las enzimas de tipo IIA. Estas diferencias incluyen la falta de una de las "puertas" de la proteína (la puerta C) (Fig. 5). Se encontraron originalmente en arqueas, pero también se han encontrado en eucariotas y, en particular, en plantas; los ejemplos incluyen topo VI y topo VIII. Topo VI es la enzima mejor estudiada de este subtipo y se cree que es una decatenasa preferencial. [31]
Para los no especialistas, quizás el aspecto más importante de las topoisomerasas sea su papel como dianas farmacológicas tanto para la quimioterapia antibacteriana como para la quimioterapia anticancerígena; Varios medicamentos antibacterianos y anticancerígenos dirigidos a la topoisomerasa figuran en la Lista Modelo de Medicamentos Esenciales de la Organización Mundial de la Salud de 2019. La razón de esta prominencia es que sus reacciones se producen a través de roturas transitorias en el ADN que, si se estabilizan mediante la unión de fármacos, pueden provocar la muerte celular debido a la generación de roturas tóxicas de una o dos cadenas en el ADN genómico. La mayoría de los fármacos topo-dirigidos actúan de esta manera, es decir, estabilizan el intermediario de escisión covalente enzima-ADN. [32] [33] [34]
Aunque los topos de tipo I, como el topo I bacteriano, son objetivos antibióticos viables, [35] actualmente no existen compuestos de uso clínico que se dirijan a estas enzimas. Sin embargo, las enzimas de tipo II, la ADN girasa y la ADN topoisomerasa IV, han tenido un enorme éxito como dianas para los antibióticos fluoroquinolonas ampliamente utilizados (Fig. 6).
Los compuestos antibacterianos de quinolona se desarrollaron por primera vez en la década de 1960 y han estado en uso clínico desde la década de 1980. [36] Los derivados de FQ, como la ciprofloxacina, la levofloxacina y la moxifloxacina (Fig. 6) han tenido un gran éxito. Estos compuestos funcionan interactuando con su objetivo (girasa o topo IV) y el ADN en el sitio de escisión para estabilizar el intermediario de escisión covalente ADN-proteína. Específicamente, se intercalan en el ADN e impiden el paso de religación del ADN de la reacción de la topoisomerasa (Fig. 5). Se trata de un mecanismo de inhibición muy eficaz que también utilizan varios fármacos anticancerígenos dirigidos a la topoisomerasa. A pesar de su espectacular éxito, la resistencia a las FQ es un problema grave. [36] Una variedad de otros compuestos, como las quinazolinedionas y las imidazolpirazinonas, [37] funcionan de manera similar y se espera que algunos de ellos reemplacen a las FQ en el futuro.
Las aminocumarinas (Fig. 6), como la novobiocina, la clorobiocina y la cumermicina A 1 , son productos naturales de Streptomyces que inhiben la reacción ATPasa de la girasa y la topo IV. [37] Aunque pueden ser muy potentes contra su objetivo, sufren problemas de permeabilidad y toxicidad y, por lo tanto, no han disfrutado del nivel de éxito clínico de los FQ.
Hay una serie de inhibidores de proteínas de la girasa, incluidas las toxinas bacterianas CcdB, MccB17 y ParE, [38] [39] [40] que estabilizan el complejo de escisión, de manera similar a las FQ. Aunque estas proteínas no son viables como antibacterianos, su modo de acción podría inspirar el desarrollo de nuevos compuestos antibacterianos. Otros inhibidores proteicos de la girasa impiden la unión del ADN por parte de la topoisomerasa en lugar de estabilizar los complejos de escisión. Estos incluyen YacG [41] y proteínas repetidas pentapeptídicas, como QnrB1 y MfpA; [42] [43] estos inhibidores de proteínas también confieren resistencia a las fluoroquinolonas.

Tanto la topo I como la topo II humanas (ambas isoformas α y β) pueden ser objetivo de la quimioterapia anticancerígena (Fig. 7). [32] [33] [44] [45] [46] [47] La mayoría de estos compuestos actúan de manera similar a las FQ, es decir, estabilizando el complejo de escisión covalente ADN-proteína; por ello se les conoce como venenos de topoisomerasa, distintos de los inhibidores catalíticos. [33] [34] [48] Varios inhibidores de la topoisomerasa humana están incluidos en la Lista de medicamentos esenciales de la Organización Mundial de la Salud .
La camptotecina (Fig. 7), derivada originalmente del árbol Camptotheca acuminata , se dirige a la topo I humana y derivados como el topotecán y el irinotecán se utilizan ampliamente en la quimioterapia contra el cáncer. [33] La camptotecina y sus derivados actúan estabilizando el complejo de escisión topo I, evitando la religación de la mella mediada por proteínas en el ADN. Estos inhibidores interfaciales se estabilizan mediante interacciones de apilamiento con el ADN mellado y enlaces de hidrógeno a la enzima. Aunque los derivados de CPT estabilizan un complejo de escisión monocatenario, se cree que las colisiones posteriores con la maquinaria de replicación o transcripción generan roturas tóxicas del ADN bicatenario. Estos compuestos se utilizan como terapias de primera o segunda línea para tratar cánceres, incluidos el colorrectal, el de ovario, el de pulmón, el de mama y el de cuello uterino. Sin embargo, los derivados de CPT adolecen de limitaciones asociadas con la toxicidad y vidas medias terapéuticas limitadas debido a la inestabilidad química. Los nuevos inhibidores de topo I, las indenoisoquinolinas y las fluoroindenoisoquinolinas, superan las limitaciones de los derivados de CPT y actualmente se encuentran en ensayos clínicos. [49]
El etopósido (Fig. 7) y su pariente cercano tenipósido (VM-26) son derivados de epipodofilotoxina obtenidos del rizoma de la mandrágora silvestre que se dirigen al topo II estabilizando el complejo de escisión covalente y previniendo la religación del ADN escindido. [46] Por lo general, se usan junto con otros medicamentos de quimioterapia para tratar cánceres, incluidos tumores testiculares, cáncer de pulmón de células pequeñas y leucemia. El tratamiento con etopósido puede provocar leucemias secundarias que surgen de translocaciones genómicas específicas, que afectan principalmente a topo IIβ. [46]

La doxorrubicina (Fig. 7) y los derivados relacionados daunorrubicina, epirrubicina e idarrubicina son antraciclinas obtenidas de la bacteria Streptomyces [48] que se dirigen a la topo II humana, estabilizando el complejo de escisión de manera similar a otros venenos de topoisomerasa. La mitoxantrona es una antracenodiona sintética que es química y funcionalmente similar a las antraciclinas. [47] Las antraciclinas fueron los primeros inhibidores de la topoisomerasa utilizados para tratar el cáncer y siguen estando entre los tratamientos más utilizados y eficaces para una amplia gama de cánceres, incluidos el cáncer de mama, el linfoma, las leucemias, los carcinomas, los sarcomas y otros tumores. [47] Estos compuestos son agentes intercalantes del ADN y, como tales, pueden afectar una amplia gama de procesos del ADN celular, además de envenenar específicamente el topo II. [33] La citotoxicidad adicional proviene de reacciones redox que involucran antraciclinas que generan especies reactivas de oxígeno. La generación de oxígeno reactivo, junto con el envenenamiento de topo IIβ, da como resultado una cardiotoxicidad limitante de la dosis de las antraciclinas. [33]
La merbarona es un derivado del ácido tiobarbitúrico, y el dexrazoxano (ICRF-187), uno de varios derivados de bisdioxopiperazina relacionados, (Fig. 7) son ejemplos de inhibidores catalíticos de topo II, es decir, evitan que se complete el ciclo catalítico de topo II pero no estabilizar el complejo de escisión del ADN. Si bien estos inhibidores catalíticos presentan citotoxicidad y han sido probados en ensayos clínicos, actualmente no se utilizan clínicamente para la terapia del cáncer. [47] Sin embargo, el dexrazoxano, que bloquea la hidrólisis del ATP por topo II, se utiliza para prevenir la cardiotoxicidad asociada con las antraciclinas. [50] [51]
Al menos una topoisomerasa, la ADN topoisomerasa II beta (topo IIβ), tiene un papel regulador en la transcripción genética. Las roturas del ADN de doble cadena dependientes de Topo IIβ y los componentes de la maquinaria de reparación del daño del ADN son importantes para la expresión rápida de genes tempranos inmediatos , así como para la regulación genética que responde a señales. [52] [53] [54] [55] Topo IIβ, con otras enzimas asociadas, [54] parece ser importante para la liberación de ARN polimerasa pausada en genes largos o altamente transcritos. [56] [57] [58]
Las roturas de doble cadena del ADN (DSB) inducidas por estímulos que se limitan a un corto plazo (de 10 minutos a 2 horas) son inducidas por topo IIβ en las regiones promotoras de genes regulados por señales. Estos DSB permiten una rápida regulación positiva de la expresión de dichos genes que responden a señales en varios sistemas (consulte la tabla a continuación). Estos genes regulados por señales incluyen genes activados en respuesta a la estimulación con estrógenos , suero , insulina , glucocorticoides (como la dexametasona ) y activación de neuronas. Cuando se ha reparado la rotura inducida de la doble cadena del ADN, la transcripción del gen que responde a la señal vuelve a un nivel basal bajo. [52]

Se encontró que Topo IIβ y PARP-1 estaban constitutivamente presentes en un nivel moderado cerca del sitio de inicio de la transcripción de un promotor de un gen que responde a señales. Después de que se produjo la señal, topo IIβ provocó una rotura de la doble hebra y PARP-1 participó en la sustitución de la histona H1 por HMGB1 / HMGA2 , que puede promover la transcripción. [55] Topo IIβ y PARP-1 aumentaron en el sitio de la rotura de la doble hebra y los componentes de la vía de reparación del ADN que se une al extremo no homólogo , incluidos DNA-PKcs, Ku70/Ku80 y ADN ligasa IV ensamblados con topo IIβ y PARP. -1. Todo este conjunto estaba presente en el ADN conector adyacente a un único nucleosoma en la región promotora de un gen (ver Figura). El nucleosoma estaba cerca del sitio de inicio de la transcripción del gen. [55] Los componentes del extremo no homólogo que une la vía de reparación del ADN fueron esenciales para el cierre de la rotura de la doble hebra del ADN. [52]
La ARN polimerasa II con frecuencia tiene un sitio de pausa que se encuentra aproximadamente entre 30 y 60 nucleótidos aguas abajo del sitio de inicio de la transcripción de un gen. [64] [65] Se cree que la pausa de la ARN polimerasa II en estos sitios y la liberación controlada de la pausa tienen un papel regulador en la transcripción genética. Como señalaron Singh et al., [58] "alrededor del 80% de los genes altamente expresados en las células HeLa están en pausa". Se producen roturas de doble hebra de ADN inducidas por topo IIβ a muy corto plazo, pero no reselladas de inmediato, en los sitios de pausa de la ARN polimerasa II, y parecen ser necesarias para la liberación eficiente del estado de pausa y la progresión hacia la transcripción genética. [56] [57] [58] Para los genes en los que ocurre, se cree que la rotura de doble cadena del ADN inducida por TOP2B es parte del proceso de regulación de la expresión génica.