La riboflavina sintasa es una enzima que cataliza la reacción final de la biosíntesis de riboflavina . Cataliza la transferencia de una unidad de cuatro carbonos de una molécula de 6,7-dimetil-8-ribitillumazina a otra, lo que da como resultado la síntesis de riboflavina y 5-amino-6-ribitilamino-2,4(1 H ,3 H. )-pirimidindiona :
El monómero de riboflavina sintasa tiene un peso molecular de aproximadamente 23 kDa. Cada monómero contiene dos barriles beta y una hélice α en el extremo C (residuos 186-206). El monómero se pliega en una pseudosimetría doble, predicha por la similitud de secuencia entre el cilindro del extremo N (residuos 4-86) y el cilindro del extremo C (residuos 101-184). [1] La interfaz entre estos barriles de dos subunidades diferentes es la ubicación del sitio activo . [3] La enzima de diferentes especies adopta diferentes estructuras cuaternarias , que contienen hasta 120 subunidades. [4]
La riboflavina sintasa arqueal se forma como un homopentámero, mientras que la riboflavina sintasa eubacteriana , fúngica y vegetal existe como un homotrímero. Sus secuencias no tienen ninguna relación, la enzima arqueal es análoga a la 6,7-dimetil-8-ribitillumazina sintasa . [3] Las reacciones catalizadas por estos dos tipos de riboflavina sintasa proceden a través de intermediarios "enantioméricos". [3]
Dos moléculas de 6,7-dimetil-8-ribitillumazina (sintetizadas por lumazina sintasa ) están unidas por hidrógeno a cada monómero, ya que los dos dominios son topológicamente similares. [5] El sitio activo está ubicado en la interfaz de los sustratos entre pares de monómeros y se han creado estructuras modeladas del dímero del sitio activo. [2] Solo uno de los sitios activos de la enzima cataliza la formación de riboflavina a la vez, mientras que los otros dos sitios miran hacia afuera y están expuestos al solvente . [1] Se muestran los residuos de aminoácidos involucrados en el enlace de hidrógeno al ligando ; los residuos participantes pueden incluir Thr148, Met160, Ile162, Thr165, Val6, Tyr164, Ser146 y Gly96 en el dominio C-terminal y Ser41, Thr50, Gly 62. , Ala64, Ser64, Val103, Cys48, His102 en el dominio N-terminal. [3]
No se necesitan cofactores para la catálisis. Además, la formación de riboflavina a partir de 6,7-dimetil-8-ribitillumazina puede ocurrir en una solución acuosa hirviendo en ausencia de riboflavina sintasa. [6] La reacción es la siguiente:
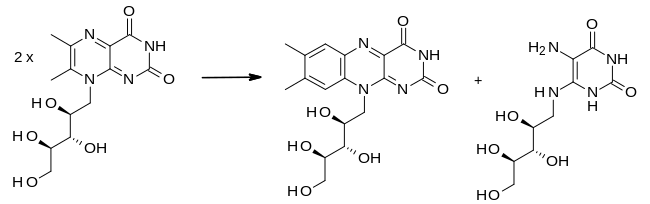
En la interfaz del sustrato entre pares de monómeros, la enzima mantiene las dos moléculas de 6,7-dimetil-8-ribitillumazina en posición mediante enlaces de hidrógeno para catalizar la reacción de dismutación . [6] Además, se ha sugerido la catálisis ácido/base por los residuos de aminoácidos. Los residuos específicos pueden incluir la díada His102/Thr148 como base para la desprotonación del grupo metilo C7a . De la díada, His102 es del barril N y Thr148 es del barril C, destacando la importancia de la proximidad de las dos subunidades de la enzima en las primeras etapas de la reacción. [7] También se ha sugerido que la identidad del nucleófilo es uno de los siguientes residuos conservados: Ser146, Ser41, Cys48 o Thr148, o agua en la reacción no catalizada. [1] En estudios sobre el papel de Cys48 como posible nucleófilo, no se ha determinado si el desplazamiento nucleofílico se produce mediante una reacción SN1 o SN2 . [7]
Durante la reacción de dismutación, se intercambia una unidad de cuatro carbonos entre las dos moléculas de 6,7-dimetil-8-ribitillumazina. Durante la reacción se crea una molécula pentacíclica que luego se descompone en riboflavina y 5-amino-6-ribitilamino-2,4(1 H ,3 H )-pirimidindiona. Curiosamente, la riboflavina sintasa arqueal crea un intermedio "enantiomérico" a diferencia de la riboflavina sintasa eubacteriana, fúngica y vegetal, donde el ataque de una molécula procede de la cara opuesta en comparación con la otra enzima. [3] Se desconoce el mecanismo exacto de formación del aducto cíclico. También se desconoce cómo se produce exactamente el mecanismo cuando no está catalizado por una enzima. [3]
Los científicos han planteado la hipótesis de que las enzimas implicadas en la vía de biosíntesis de la riboflavina, incluida la riboflavina sintasa, pueden utilizarse para desarrollar fármacos antibacterianos con el fin de tratar infecciones causadas por bacterias y levaduras gramnegativas . Esta hipótesis se basa en la incapacidad de las bacterias Gram-negativas, como E. coli y S. typhimurium , de absorber riboflavina del ambiente externo. [3] [8] Como las bacterias Gram-negativas necesitan producir su propia riboflavina, la inhibición de la riboflavina sintasa u otras enzimas involucradas en la vía pueden ser herramientas útiles en el desarrollo de fármacos antibacterianos.
El inhibidor más potente de la riboflavina sintasa es la 9- D- ribitil-1,3,7-trihidropurina-2,6,8-triona, con un valor Ki de 0,61 μM. Se cree que actúa mediante inhibición competitiva con 6,7-dimetil-8-ribitillumazina. [8]