La capacitancia de doble capa es la característica importante de la doble capa eléctrica [1] [2] que aparece en la interfaz entre una superficie y un fluido (por ejemplo, entre un electrodo conductor y un electrolito líquido adyacente ). En este límite se forman dos capas de carga eléctrica con polaridad opuesta, una en la superficie del electrodo y otra en el electrolito. Estas dos capas, electrones en el electrodo e iones en el electrolito, suelen estar separadas por una sola capa de moléculas de disolvente que se adhieren a la superficie del electrodo y actúan como un dieléctrico en un condensador convencional . La cantidad de carga almacenada en un condensador de doble capa depende del voltaje aplicado .
La capacitancia de doble capa es el principio físico detrás del tipo de supercondensadores de doble capa electrostáticos .
Helmholtz sentó las bases teóricas para comprender el fenómeno de la doble capa. La formación de dobles capas se aprovecha en todos los condensadores electroquímicos para almacenar energía eléctrica.
Cada condensador tiene dos electrodos, separados mecánicamente por un separador. Estos están conectados eléctricamente a través del electrolito, una mezcla de iones positivos y negativos disueltos en un disolvente como el agua. Allí donde el electrolito líquido entra en contacto con la superficie metálica conductora del electrodo, se forma una interfaz que representa un límite común entre las dos fases de la materia. Es en esta interfaz donde se produce el efecto de doble capa. [1] [2]
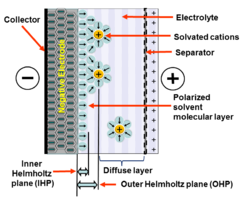
Cuando se aplica un voltaje al condensador, se generan dos capas de iones polarizados en las interfaces de los electrodos. Una capa está dentro del electrodo sólido (en las superficies de los granos de cristal de los que está hecho que están en contacto con el electrolito). La otra capa, con polaridad opuesta, se forma a partir de iones disueltos y solvatados distribuidos en el electrolito que se han movido hacia el electrodo polarizado. Estas dos capas de iones polarizados están separadas por una monocapa de moléculas de disolvente . La monocapa molecular forma el plano interno de Helmholtz (IHP). Se adhiere por adsorción física en la superficie del electrodo y separa los iones polarizados opuestamente entre sí, formando un dieléctrico molecular .
La cantidad de carga en el electrodo se corresponde con la magnitud de las contracargas en el plano de Helmholtz externo (OHP). Esta es la zona cercana al IHP, en la que se recogen los iones polarizados del electrolito. Esta separación de dos capas de iones polarizados a través de la doble capa almacena cargas eléctricas de la misma manera que en un condensador convencional. La carga de la doble capa forma un campo eléctrico estático en la capa molecular IHP de las moléculas de disolvente que corresponde a la intensidad del voltaje aplicado.
El "espesor" de una capa cargada en el electrodo metálico, es decir, la extensión media perpendicular a la superficie, es de aproximadamente 0,1 nm, y depende principalmente de la densidad electrónica porque los átomos en los electrodos sólidos son estacionarios. En el electrolito, el espesor depende del tamaño de las moléculas del disolvente y del movimiento y concentración de iones en el disolvente. Varía de 0,1 a 10 nm, como se describe mediante la longitud de Debye . La suma de los espesores es el espesor total de una doble capa.
El pequeño espesor del IHP crea un fuerte campo eléctrico E sobre las moléculas de disolvente que se separan. Con una diferencia de potencial de, por ejemplo, U = 2 V y un espesor molecular de d = 0,4 nm, la intensidad del campo eléctrico es
Para comparar esta cifra con los valores de otros tipos de condensadores es necesario hacer una estimación para los condensadores electrolíticos , los condensadores con el dieléctrico más delgado entre los condensadores convencionales. La resistencia a la tensión del óxido de aluminio , la capa dieléctrica de los condensadores electrolíticos de aluminio, es de aproximadamente 1,4 nm/V. Por tanto, para un condensador de 6,3 V, la capa es de 8,8 nm. El campo eléctrico es de 6,3 V/8,8 nm = 716 kV/mm, alrededor de 7 veces inferior al de la doble capa. La intensidad de campo de unos 5000 kV/mm es irrealizable en los condensadores convencionales. Ningún material dieléctrico convencional podría impedir la ruptura de los portadores de carga. En un condensador de doble capa, la estabilidad química de los enlaces moleculares del disolvente impide la ruptura. [3]
Las fuerzas que provocan la adhesión de las moléculas de disolvente en el IHP son fuerzas físicas, no enlaces químicos. Los enlaces químicos existen dentro de las moléculas adsorbidas, pero están polarizados.
La magnitud de la carga eléctrica que puede acumularse en las capas corresponde a la concentración de iones adsorbidos y a la superficie de los electrodos. Hasta el voltaje de descomposición del electrolito , esta disposición se comporta como un condensador en el que la carga eléctrica almacenada depende linealmente del voltaje .

La doble capa es como la capa dieléctrica de un condensador convencional, pero con el espesor de una sola molécula. Utilizando el modelo temprano de Helmholtz para calcular la capacitancia, el modelo predice una capacitancia diferencial constante C d independiente de la densidad de carga, incluso dependiendo de la constante dieléctrica ε y de la separación de las capas de carga δ .
Si el disolvente electrolítico es agua, la influencia de la alta intensidad de campo crea una permitividad ε de 6 (en lugar de 80 sin un campo eléctrico aplicado) y la separación de capas δ de aproximadamente 0,3 nm, el modelo de Helmholtz predice un valor de capacitancia diferencial de aproximadamente 18 μF/cm 2 . [4] Este valor se puede utilizar para calcular valores de capacitancia utilizando la fórmula estándar para capacitores de placa convencionales si solo se conoce la superficie de los electrodos. Esta capacitancia se puede calcular con:
La capacitancia C es mayor en los componentes fabricados con materiales con una permitividad ε alta , áreas de superficie de placa de electrodos grandes A y una distancia d pequeña entre placas. Debido a que los electrodos de carbón activado tienen un área de superficie muy alta y una distancia de doble capa extremadamente delgada que es del orden de unos pocos ångströms (0,3-0,8 nm), es comprensible por qué los supercondensadores tienen los valores de capacitancia más altos entre los condensadores (en el rango de 10 a 40 μF/cm 2 ). [5] [6]
En los supercondensadores producidos realmente con una gran cantidad de capacidad de doble capa, el valor de la capacidad depende en primer lugar de la superficie del electrodo y de la distancia DL. Parámetros como el material y la estructura del electrodo, la mezcla de electrolitos y la cantidad de pseudocapacidad también contribuyen al valor de la capacidad. [1]
Como un condensador electroquímico está compuesto por dos electrodos, la carga eléctrica en la capa de Helmholtz de un electrodo se refleja (con polaridad opuesta) en la segunda capa de Helmholtz del segundo electrodo. Por lo tanto, el valor de capacitancia total de un condensador de doble capa es el resultado de dos condensadores conectados en serie. Si ambos electrodos tienen aproximadamente el mismo valor de capacitancia, como en los supercondensadores simétricos, el valor total es aproximadamente la mitad del de un electrodo.
{{cite book}}: |work=ignorado ( ayuda )