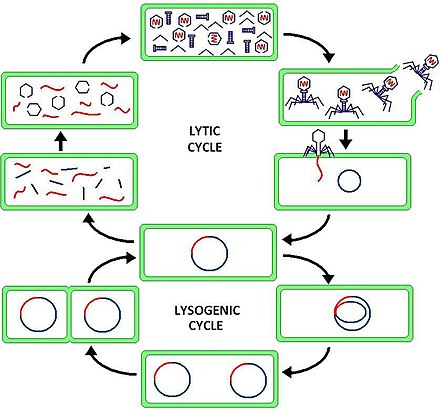
El ciclo lítico ( / ˈlɪtɪk / LIT -ik ) es uno de los dos ciclos de reproducción viral (refiriéndose a los virus bacterianos o bacteriófagos ) , siendo el otro el ciclo lisogénico . El ciclo lítico resulta en la destrucción de la célula infectada y su membrana. Los bacteriófagos que solo pueden pasar por el ciclo lítico se denominan fagos virulentos (en contraste con los fagos templados ).
En el ciclo lítico, el ADN viral existe como una molécula independiente que flota libremente dentro de la célula bacteriana y se replica por separado del ADN bacteriano del huésped, mientras que en el ciclo lisogénico, el ADN viral se integra en el genoma del huésped. Esta es la diferencia clave entre los ciclos lítico y lisogénico. Sin embargo, en ambos casos, el virus/fago se replica utilizando la maquinaria del ADN del huésped.
El ciclo lítico suele dividirse en seis etapas: unión, penetración, transcripción, biosíntesis, maduración y lisis.
Para infectar una célula huésped, el virus primero debe inyectar su propio ácido nucleico en la célula a través de la membrana plasmática y (si está presente) la pared celular. El virus lo hace ya sea uniéndose a un receptor en la superficie de la célula o por simple fuerza mecánica. La unión se debe a interacciones electrostáticas y está influenciada por el pH y la presencia de iones. Luego, el virus libera su material genético ( ARN o ADN monocatenario o bicatenario ) en la célula. En algunos virus, este material genético es circular e imita un plásmido bacteriano . En esta etapa, la célula se infecta y también puede ser el objetivo del sistema inmunológico. En su mayoría, es ayudado por receptores en la superficie de la célula. [ cita requerida ] La secuencia de eventos que ocurren durante el inicio de la infección por bacteriófagos , desde la adsorción (fijación) hasta la expulsión de ADN del virión hacia la célula huésped (penetración), fue revisada por Molineux. [1]
Durante las etapas de transcripción y biosíntesis, el virus secuestra los mecanismos de replicación y traducción de la célula y los utiliza para crear más virus. El ácido nucleico del virus utiliza la maquinaria metabólica de la célula huésped para producir grandes cantidades de componentes virales. [2]
En el caso de los virus de ADN, el ADN se transcribe a sí mismo en moléculas de ARN mensajero (ARNm) que luego se utilizan para dirigir los ribosomas de la célula. Uno de los primeros polipéptidos que se traducen destruye el ADN del huésped. En los retrovirus (que inyectan una cadena de ARN), una enzima única llamada transcriptasa inversa transcribe el ARN viral en ADN, que luego se transcribe nuevamente en ARN. Una vez que el ADN viral ha tomado el control, induce a la maquinaria de la célula huésped a sintetizar ADN viral, proteína y comienza a multiplicarse. [ cita requerida ]
La biosíntesis se regula (por ejemplo, T4 ) en tres fases de producción de ARNm seguida de una fase de producción de proteínas. [3]
Aproximadamente 25 minutos después de la infección inicial, se forman aproximadamente 200 nuevos viriones (cuerpos virales). Una vez que han madurado y acumulado suficientes viriones, se utilizan proteínas virales especializadas para disolver las paredes celulares. La célula estalla (es decir, sufre lisis ) debido a la alta presión osmótica interna (presión del agua) que ya no puede ser restringida por la pared celular. Esto libera viriones progenie en el entorno circundante, donde pueden continuar infectando otras células y comienza otro ciclo lítico. El fago que causa la lisis del huésped se llama fago lítico o virulento. [5]
Existen tres clases de genes en el genoma del fago que regulan si surgirán los ciclos líticos o lisogénicos. La primera clase son los genes tempranos inmediatos, la segunda son los genes tempranos retrasados y la tercera son los genes tardíos. A continuación se hace referencia al fago templado lambda de E. coli, bien estudiado. [ cita requerida ]
La activación mediada por Q de la transcripción tardía comienza aproximadamente entre 6 y 8 minutos después de la infección si se elige la vía lítica. Más de 25 genes se expresan a partir del promotor tardío único, lo que da como resultado cuatro vías biosintéticas paralelas. Tres de las vías son para la producción de los tres componentes del virión: la cabeza llena de ADN, la cola y las fibras laterales de la cola. Los viriones se autoensamblan a partir de estos componentes, y el primer virión aparece aproximadamente 20 minutos después de la infección. La cuarta vía es para la lisis. En lambda, 5 proteínas están involucradas en la lisis: la holina y la antiholina del gen S , la endolisina del gen R y las proteínas spanina de los genes Rz y Rz1 . En lambda de tipo salvaje, la lisis ocurre aproximadamente a los 50 minutos, liberando aproximadamente 100 viriones completos. El momento de la lisis está determinado por las proteínas holina y antiholina, y la última inhibe a la primera. En resumen, la proteína holina se acumula en la membrana citoplasmática hasta formar repentinamente agujeros a escala micrométrica, lo que desencadena la lisis. La endolisina R se libera al periplasma, donde ataca al peptidoglicano. Las proteínas spanina Rz y Rz1 se acumulan en las membranas citoplasmática y externa, respectivamente, y forman un complejo que abarca el periplasma a través de la red del peptidoglicano. Cuando la endolisina degrada el peptidoglicano, los complejos spanina se liberan y causan la ruptura de la membrana externa. La destrucción del peptidoglicano por la endolisina y la ruptura de la membrana externa por el complejo spanina son necesarias para la lisis en las infecciones lambda. [ cita requerida ]
Inhibición de la lisis: los fagos similares a T4 tienen dos genes, rI y rIII , que inhiben la holina T4 si la célula infectada sufre una superinfección por otro virión T4 (o uno estrechamente relacionado). La superinfección repetida puede hacer que la infección T4 continúe sin lisis durante horas, lo que lleva a la acumulación de viriones a niveles diez veces superiores a lo normal. [6] [ se necesita una mejor fuente ]