En química , hidronio ( hidroxonio en inglés británico tradicional ) es el nombre común del catión [H 3 O] + , también escrito como H 3 O + , el tipo de ion oxonio producido por la protonación del agua . A menudo se lo considera el ion positivo presente cuando un ácido de Arrhenius se disuelve en agua, ya que las moléculas de ácido de Arrhenius en solución ceden un protón (un ion de hidrógeno positivo , H + ) a las moléculas de agua circundantes ( H 2 O ). De hecho, los ácidos deben estar rodeados por más de una molécula de agua para poder ionizarse, produciendo H + acuoso y una base conjugada. Tres estructuras principales para el protón acuoso han obtenido apoyo experimental: el catión Eigen, que es un tetrahidrato, H 3 O + (H 2 O) 3 , el catión Zundel, que es un dihidrato simétrico, H + (H 2 O) 2. , y el catión Stoyanov, un catión Zundel expandido, que es un hexahidrato: H + (H 2 O) 2 (H 2 O) 4 . [1] [2] La evidencia espectroscópica de espectros IR bien definidos apoya abrumadoramente al catión de Stoyanov como la forma predominante. [3] [4] [5] [6] Por esta razón, se ha sugerido que siempre que sea posible, se debe utilizar el símbolo H + (aq) en lugar del ion hidronio. [2]
La concentración molar de hidronio o iones H + determina el pH de una solución según
donde M = mol/L. La concentración de iones hidróxido determina de manera análoga el pOH de una solución . Las moléculas del agua pura se autodisocian en protones acuosos e iones de hidróxido en el siguiente equilibrio:
En el agua pura hay la misma cantidad de hidróxido e iones H + , por lo que es una solución neutra. A 25 °C (77 °F), el agua pura tiene un pH de 7 y un pOH de 7 (esto varía cuando cambia la temperatura: ver autoionización del agua ). Un valor de pH inferior a 7 indica una solución ácida y un valor de pH superior a 7 indica una solución básica. [7]
Según la nomenclatura de química orgánica de la IUPAC , el ion hidronio debe denominarse oxonio . [8] El hidroxonio también se puede utilizar sin ambigüedades para identificarlo. [ cita necesaria ]
Un ion oxonio es cualquier catión que contiene un átomo de oxígeno trivalente.
Dado que O + y N tienen el mismo número de electrones, el H3O + es isoelectrónico con el amoníaco . Como se muestra en las imágenes de arriba, el H 3 O + tiene una geometría molecular piramidal trigonal con el átomo de oxígeno en su vértice. El ángulo del enlace H-O-H es de aproximadamente 113°, [9] y el centro de masa está muy cerca del átomo de oxígeno. Debido a que la base de la pirámide está formada por tres átomos de hidrógeno idénticos, la configuración superior simétrica de la molécula de H 3 O + es tal que pertenece al grupo de puntos C 3v . Debido a esta simetría y al hecho de que tiene un momento dipolar, las reglas de selección rotacional son Δ J = ±1 y Δ K = 0. El dipolo de transición se encuentra a lo largo del eje c y, debido a que la carga negativa está localizada cerca del oxígeno átomo, el momento dipolar apunta al vértice, perpendicular al plano de la base. [ cita necesaria ]
El protón hidratado es muy ácido: a 25 °C, su p K a es aproximadamente 0. [10] Los valores comúnmente dados para p K a aq (H 3 O + ) son 0 o –1,74. El primero utiliza la convención de que la actividad del disolvente en una solución diluida (en este caso, agua) es 1, mientras que el segundo utiliza el valor de la concentración de agua en el líquido puro de 55,5 M. Silverstein ha demostrado que el segundo El valor es termodinámicamente insoportable. [11] El desacuerdo proviene de la ambigüedad de que para definir p K a de H 3 O + en agua, el H 2 O tiene que actuar simultáneamente como soluto y disolvente. La IUPAC no ha dado una definición oficial de p K a que resuelva esta ambigüedad. Burgot ha argumentado que H 3 O + (aq) + H 2 O (l) ⇄ H 2 O (aq) + H 3 O + (aq) simplemente no es un proceso termodinámicamente bien definido. Para una estimación de p K a aq (H 3 O + ), Burgot sugiere tomar el valor medido p K a EtOH (H 3 O + ) = 0,3, el p K a de H 3 O + en etanol, y aplicar la correlación ecuación p K a aq = p K a EtOH – 1,0 (± 0,3) para convertir el etanol p K a a un valor acuoso, para dar un valor de p K a aq (H 3 O + ) = –0,7 (± 0,3) . [12] Por otro lado, Silverstein ha demostrado que los resultados experimentales de Ballinger y Long [13] apoyan una p K a de 0,0 para el protón acuoso. [14] Neils y Schaertel proporcionan argumentos adicionales para ap K a de 0,0 [15]
El protón acuoso es la especie más ácida que puede existir en el agua (suponiendo que haya suficiente agua para la disolución): cualquier ácido más fuerte se ionizará y producirá un protón hidratado. La acidez de H + (aq) es el estándar implícito utilizado para juzgar la fuerza de un ácido en agua: los ácidos fuertes deben ser mejores donantes de protones que H + (aq), ya que de lo contrario una porción significativa de ácido existirá en un medio no ácido. estado ionizado (es decir: un ácido débil). A diferencia del H + (aq) en soluciones neutras que resultan de la autodisociación del agua, en soluciones ácidas, el H + (aq) es duradero y concentrado, en proporción a la fuerza del ácido disuelto. [ cita necesaria ]
El pH se concibió originalmente como una medida de la concentración de iones de hidrógeno en una solución acuosa. [16] Prácticamente todos estos protones libres se hidratan rápidamente; Por lo tanto, la acidez de una solución acuosa se caracteriza con mayor precisión por su concentración de H + (aq). En síntesis orgánicas, como reacciones catalizadas por ácidos, el ion hidronio ( H 3 O + ) se usa indistintamente con el ion H + ; elegir uno sobre el otro no tiene ningún efecto significativo sobre el mecanismo de reacción. [ cita necesaria ]
Los investigadores aún tienen que caracterizar completamente la solvatación del ion hidronio en agua, en parte porque existen muchos significados diferentes de solvatación. Un estudio de depresión del punto de congelación determinó que el ion de hidratación medio en agua fría es aproximadamente H 3 O + (H 2 O) 6 : [17] en promedio, cada ion hidronio está solvatado por 6 moléculas de agua que no pueden solvatar otros solutos. moléculas. [ cita necesaria ]
Algunas estructuras de hidratación son bastante grandes: la estructura del número de iones mágicos H 3 O + (H 2 O) 20 (llamada número mágico debido a su mayor estabilidad con respecto a las estructuras de hidratación que involucran un número comparable de moléculas de agua; este es un uso similar de el término número mágico como en la física nuclear ) podría colocar el hidronio dentro de una jaula dodecaédrica . [18] Sin embargo, simulaciones de dinámica molecular del método ab initio más recientes han demostrado que, en promedio, el protón hidratado reside en la superficie del grupo H 3 O + (H 2 O) 20 . [19] Además, varias características dispares de estas simulaciones concuerdan con sus contrapartes experimentales, lo que sugiere una interpretación alternativa de los resultados experimentales. [ cita necesaria ]

Otras dos estructuras bien conocidas son el catión Zundel y el catión Eigen . La estructura de solvatación propia tiene el ion hidronio en el centro de un H 9 O+4complejo en el que el hidronio está fuertemente unido por enlaces de hidrógeno a tres moléculas de agua vecinas. [20] En el Zundel H 5 O+2complejo: el protón es compartido equitativamente por dos moléculas de agua en un enlace de hidrógeno simétrico . [21] Trabajos recientes indican que ambos complejos representan estructuras ideales en un defecto de red de enlaces de hidrógeno más general. [22]
El aislamiento del monómero del ion hidronio en fase líquida se logró en una solución superácida no acuosa de baja nucleofilicidad ( HF − SbF 5 SO 2 ). El ion se caracterizó mediante resonancia magnética nuclear de 17 O de alta resolución . [23]
Un cálculo realizado en 2007 de las entalpías y energías libres de los diversos enlaces de hidrógeno alrededor del catión hidronio en agua líquida protonada [24] a temperatura ambiente y un estudio del mecanismo de salto de protones utilizando dinámica molecular mostraron que los enlaces de hidrógeno alrededor del ion hidronio ( formados con los tres ligandos de agua en la primera capa de solvatación del hidronio) son bastante fuertes en comparación con los del agua en masa. [ cita necesaria ]
Stoyanov propuso un nuevo modelo basado en espectroscopia infrarroja en el que el protón existe como H 13 O+6ion. La carga positiva se deslocaliza así en 6 moléculas de agua. [25]
Para muchos ácidos fuertes , es posible formar cristales de su sal de hidronio que son relativamente estables. Estas sales a veces se denominan monohidratos ácidos . Como regla general, cualquier ácido con una constante de ionización de 109 o superior pueden hacer esto. Ácidos cuyas constantes de ionización son inferiores a 109 generalmente no pueden formar sales estables de H 3 O + . Por ejemplo, el ácido nítrico tiene una constante de ionización de 101,4 , y las mezclas con agua en todas las proporciones son líquidas a temperatura ambiente. Sin embargo, el ácido perclórico tiene una constante de ionización de 1010 , y si se combinan ácido perclórico anhidro líquido y agua en una proporción molar de 1:1, reaccionan para formar perclorato de hidronio sólido ( H 3 O + ·ClO−4). [ cita necesaria ]
El ion hidronio también forma compuestos estables con el superácido carborano H(CB 11 H(CH 3 ) 5 Br 6 ) . [26] La cristalografía de rayos X muestra una simetría C 3v para el ion hidronio con cada protón interactuando con un átomo de bromo, cada uno de tres aniones carborano separados por 320 pm en promedio. La sal [H 3 O] [H(CB 11 HCl 11 )] también es soluble en benceno . En los cristales que crecen a partir de una solución de benceno, el disolvente cocristaliza y un catión H 3 O·(C 6 H 6 ) 3 se separa completamente del anión. En el catión, tres moléculas de benceno rodean el hidronio formando interacciones pi-catión con los átomos de hidrógeno. La aproximación más cercana (sin enlace) del anión en el cloro al catión en el oxígeno es 348 pm.
También hay muchos ejemplos conocidos de sales que contienen iones hidronio hidratados, como el H 5 O+2ion en HCl·2H 2 O , el H 7 O+3y H9O _ _+4Ambos iones se encuentran en HBr·4H 2 O . [27]
También se sabe que el ácido sulfúrico forma una sal de hidronio H 3 O + HSO.−4a temperaturas inferiores a 8,49 °C (47,28 °F). [28]
El hidronio es un ion molecular abundante en el medio interestelar y se encuentra en nubes moleculares difusas [29] y densas [30] , así como en las colas de plasma de los cometas. [31] Las fuentes interestelares de observaciones de hidronio incluyen las regiones de Sagitario B2, Orion OMC-1, Orion BN-IRc2, Orion KL y el cometa Hale-Bopp.
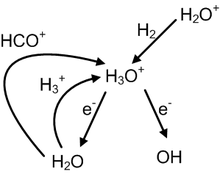
El hidronio interestelar se forma mediante una cadena de reacciones iniciadas por la ionización de H 2 en H.+2por la radiación cósmica. [32] El H 3 O + puede producir OH − o H 2 O mediante reacciones de recombinación disociativa , que ocurren muy rápidamente incluso a temperaturas bajas (≥10 K) de nubes densas. [33] Esto lleva a que el hidronio desempeñe un papel muy importante en la química interestelar de iones neutros. [ cita necesaria ]
Los astrónomos están especialmente interesados en determinar la abundancia de agua en diversos climas interestelares debido a su papel clave en el enfriamiento de gases moleculares densos mediante procesos radiativos. [34] Sin embargo, el H 2 O no tiene muchas transiciones favorables para las observaciones terrestres. [35] Aunque las observaciones de HDO (la versión deuterada del agua [36] ) podrían usarse potencialmente para estimar la abundancia de H 2 O , la proporción de HDO a H 2 O no se conoce con mucha precisión. [35]
Hydronium, por otro lado, tiene varias transiciones que lo convierten en un candidato superior para la detección e identificación en una variedad de situaciones. [35] Esta información se ha utilizado junto con mediciones de laboratorio de las relaciones de ramificación de las diversas reacciones de recombinación disociativa de H 3 O + [33] para proporcionar lo que se cree que son abundancias de OH − y H 2 O relativamente precisas sin requerir observación directa. de estas especies. [37] [38]
Como se mencionó anteriormente, el H 3 O + se encuentra tanto en nubes moleculares densas como difusas. Aplicando las constantes de velocidad de reacción ( α , β y γ ) correspondientes a todas las reacciones caracterizadas actualmente disponibles que involucran H 3 O + , es posible calcular k ( T ) para cada una de estas reacciones. Multiplicando estos k ( T ) por las abundancias relativas de los productos, se pueden determinar las velocidades relativas (en cm 3 /s) para cada reacción a una temperatura dada. Estas tasas relativas se pueden convertir en tasas absolutas multiplicándolas por [H 2 ] 2 . [39] Al suponer T = 10 K para una nube densa y T = 50 K para una nube difusa, los resultados indican que los mecanismos de formación y destrucción más dominantes fueron los mismos en ambos casos. Cabe mencionar que las abundancias relativas utilizadas en estos cálculos corresponden a TMC-1, una nube molecular densa, y que, por lo tanto, se espera que las tasas relativas calculadas sean más precisas en T = 10 K. Los tres mecanismos de formación y destrucción más rápidos se enumeran en la siguiente tabla, junto con sus tasas relativas. Tenga en cuenta que las velocidades de estas seis reacciones son tales que constituyen aproximadamente el 99% de las interacciones químicas del ion hidronio en estas condiciones. [31] Los tres mecanismos de destrucción en la siguiente tabla se clasifican como reacciones de recombinación disociativa . [40]
También vale la pena señalar que las velocidades relativas de las reacciones de formación en la tabla anterior son las mismas para una reacción determinada a ambas temperaturas. Esto se debe a que las constantes de velocidad de reacción para estas reacciones tienen constantes β y γ de 0, lo que da como resultado k = α , que es independiente de la temperatura. [ cita necesaria ]
Dado que estas tres reacciones producen H 2 O u OH, estos resultados refuerzan la fuerte conexión entre sus abundancias relativas y la de H 3 O + . Las velocidades de estas seis reacciones son tales que constituyen aproximadamente el 99% de las interacciones químicas del ion hidronio en estas condiciones. [ cita necesaria ]
Ya en 1973 y antes de la primera detección interestelar, los modelos químicos del medio interestelar (el primero correspondiente a una nube densa) predijeron que el hidronio era un ion molecular abundante y que desempeñaba un papel importante en la química iónica neutra. [41] Sin embargo, antes de que pudiera iniciarse una búsqueda astronómica, todavía quedaba la cuestión de determinar las características espectroscópicas del hidronio en la fase gaseosa, que en ese momento se desconocían. Los primeros estudios de estas características se produjeron en 1977, [42] a los que siguieron otros experimentos de espectroscopia de mayor resolución. Una vez identificadas varias líneas en el laboratorio, la primera detección interestelar de H 3 O + fue realizada por dos grupos casi simultáneamente en 1986. [30] [35] El primero, publicado en junio de 1986, informó sobre la observación del Jvt
k = 1−
1 − 2+
1transición en307 192 , 41 MHz en OMC-1 y Sgr B2. El segundo, publicado en agosto, informó sobre la observación de la misma transición hacia la nebulosa Orión-KL. [ cita necesaria ]
Estas primeras detecciones han sido seguidas por observaciones de una serie de transiciones adicionales de H 3 O + . Las primeras observaciones de cada detección de transición posterior se dan a continuación en orden cronológico:
En 1991, los 3+
2 − 2−
2transición enSe observó 364 797 , 427 MHz en OMC-1 y Sgr B2. [43] Un año después, el 3+
0 − 2−
0transición en396 272 , 412 MHz se observó en varias regiones, la más clara de las cuales fue la nube W3 IRS 5. [38]
El primer IR lejano 4−
3 − 3+
3La transición a 69,524 µm (4,3121 THz) se realizó en 1996 cerca de Orion BN-IRc2. [44] En 2001, se observaron tres transiciones adicionales de H 3 O + en el infrarrojo lejano en Sgr B2; 2−
1 − 1+
1transición a 100,577 µm (2,98073 THz), 1−
1 − 1+
1a 181,054 µm (1,65582 THz) y 2−
0 − 1+
0a 100,869 µm (2,9721 THz). [45]