El fenil-litio es un agente organometálico con la fórmula empírica C6H5Li . Se utiliza más comúnmente como agente metalante en síntesis orgánicas y como sustituto de los reactivos de Grignard para introducir grupos fenilo en síntesis orgánicas. [3] El fenil-litio cristalino es incoloro; sin embargo, las soluciones de fenil-litio tienen varios tonos de marrón o rojo según el disolvente utilizado y las impurezas presentes en el soluto. [4]
El fenil-litio se produjo por primera vez mediante la reacción del metal litio con difenilmercurio : [5]
La reacción de un haluro de fenilo con litio metálico produce fenil-litio:
El fenil-litio también se puede sintetizar mediante una reacción de intercambio metal-halógeno:
El método predominante para producir fenil-litio hoy en día son las dos últimas síntesis.
El uso principal de PhLi es facilitar la formación de enlaces carbono-carbono mediante reacciones de adición y sustitución nucleofílica:
La 2-fenilpiridina se prepara mediante la reacción de fenil litio con piridina, un proceso que implica una vía de adición-eliminación: [6]
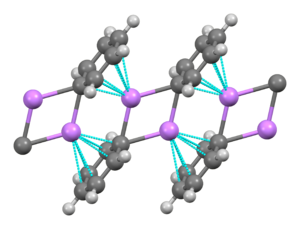
El fenil-litio es un compuesto de organolitio que forma cristales monoclínicos . El fenil-litio sólido puede describirse como formado por subunidades diméricas de Li2Ph2. Los átomos de Li y los carbonos ipso de los anillos de fenilo forman un anillo plano de cuatro miembros. El plano de los grupos fenilo es perpendicular al plano de este anillo de Li2C2 . Se produce una fuerte unión intermolecular adicional entre estos dímeros de fenil-litio y los electrones π de los grupos fenilo en los dímeros adyacentes, lo que da como resultado una estructura polimérica en escalera infinita. [7]
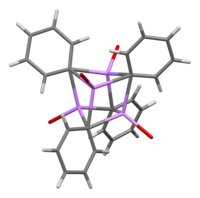
En solución, adopta una variedad de estructuras que dependen del disolvente orgánico. En tetrahidrofurano , se equilibra entre estados monómero y dímero. En éter, como se vende comúnmente, el fenil-litio existe como un tetrámero. Cuatro átomos de litio y cuatro centros de carbono ipso ocupan vértices alternos de un cubo distorsionado. Los grupos fenilo están en las caras del tetraedro y se unen a tres de los átomos de litio más cercanos.
Las longitudes de enlace C–Li son, en promedio, de 2,33 Å. Una molécula de éter se une a cada uno de los sitios de Li a través de su átomo de oxígeno. En presencia de LiBr, un subproducto de la reacción directa del litio con un haluro de fenilo, el complejo [(PhLi•Et 2 O) 4 ] se convierte en [(PhLi•Et 2 O) 3 •LiBr]. El átomo de Li de LiBr ocupa uno de los sitios de litio en el grupo de tipo cubano y el átomo de Br se encuentra en un sitio de carbono adyacente. [8]