La faujasita (zeolita tipo FAU) es un grupo mineral de la familia de las zeolitas de minerales de silicato . El grupo está formado por faujasita-Na, faujasita-Mg y faujasita-Ca. Todos comparten la misma fórmula básica (Na 2 ,Ca,Mg) 3,5 [Al 7 Si 17 O 48 ]·32(H 2 O) variando las cantidades de sodio, magnesio y calcio. [1] La faujasita se encuentra como un mineral raro en varios lugares del mundo.
Los materiales de faujasita se sintetizan ampliamente industrialmente. La faujasita sintética con relativamente bajo contenido de sílice (Si/Al<2) se llama Zeolita X y la que tiene alto contenido de sílice (Si/Al>2) se llama Zeolita Y. Además, el componente de aluminio de la zeolita Y se puede eliminar mediante tratamiento con ácido y/o tratamiento con vapor, y la faujasita resultante se denomina USY (zeolita Y ultraestable). USY se utiliza en el proceso de craqueo catalítico fluido como catalizador.
La faujasita se describió por primera vez en 1842 a partir de un hallazgo en las canteras de Limberg, Sasbach , Kaiserstuhl , Baden-Württemberg , Alemania . El modificador de sodio faujasita-Na se añadió tras el descubrimiento de las fases ricas en magnesio y calcio en la década de 1990. Lleva el nombre de Barthélemy Faujas de Saint-Fond (1741-1819), geólogo y vulcanólogo francés. [4] [5]
La faujasita se presenta en vesículas dentro de lava y toba de basalto y fonolita como una alteración o mineral autigénico . Ocurre con otras zeolitas, olivina , augita y nefelina . [3]

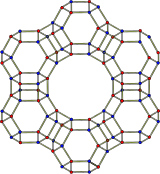
La Asociación Internacional de Zeolitas ha atribuido a la estructura de faujasita el código FAU . [6] Consiste en jaulas de sodalita que están conectadas a través de prismas hexagonales . El poro, formado por un anillo de 12 miembros, tiene un diámetro relativamente grande de 7,4 Å. La cavidad interior tiene un diámetro de 12 Å y está rodeada por 10 jaulas de sodalita. La celda unitaria es cúbica; Símbolo de Pearson cF576, simetría F d 3 m, No. 227 , [7] constante de red 24,7 Å. De los dos tipos (X e Y) de zeolitas codificadas con FAU, la zeolita Y, que es la que tiene mayor rango de contenido de sílice a alúmina, tiene una fracción de huecos del 48% y una relación Si/Al de 2,43. [ cita necesaria ] Se descompone térmicamente a 793 ° C. [8]
La faujasita se sintetiza, al igual que otras zeolitas, a partir de fuentes de alúmina como el aluminato de sodio y fuentes de sílice como el silicato de sodio . También se utilizan otros aluminosilicatos como el caolín . Los ingredientes se disuelven en un ambiente básico como una solución acuosa de hidróxido de sodio y se cristalizan entre 70 y 300 °C (normalmente a 100 °C). Después de la cristalización, la faujasita está en su forma sódica y debe intercambiarse iones con amonio para mejorar la estabilidad. El ion amonio se elimina posteriormente mediante calcinación , lo que deja la zeolita en su forma ácida. Dependiendo de la proporción de sílice a alúmina de su estructura, las zeolitas faujasita sintéticas se dividen en zeolitas X e Y. En las zeolitas X esa relación está entre 2 y 3, mientras que en las zeolitas Y es de 3 o superior. Las cargas negativas de la estructura se equilibran con las cargas positivas de los cationes (normalmente sodio de la solución de NaOH o amonio o H + después de los intercambios) en posiciones fuera de la estructura. Estas zeolitas tienen propiedades de intercambio iónico, catalíticas y de adsorción. La estabilidad de la zeolita aumenta con la relación sílice/alúmina de la estructura (regla de Lowenstein). También se ve afectado por el tipo y la cantidad de cationes ubicados en posiciones no estructurales. Para el craqueo catalítico , la zeolita Y se utiliza a menudo en una forma intercambiada de hidrógeno y tierras raras. [9]
Mediante el uso de métodos térmicos, hidrotermales o químicos, parte de la alúmina se puede eliminar de la estructura de la zeolita Y, lo que da como resultado zeolitas Y con alto contenido de sílice. Estas zeolitas se utilizan en catalizadores de craqueo e hidrocraqueo . La desaluminación completa da como resultado faujasita-sílice. [9]
La faujasita se utiliza sobre todo como catalizador en el craqueo catalítico fluido para convertir fracciones de crudo de petróleo de alto punto de ebullición en gasolina, diésel y otros productos más valiosos. La zeolita Y ha reemplazado a la zeolita X en este uso porque es más activa y más estable a altas temperaturas debido a la mayor relación Si/Al. También se utiliza en las unidades de hidrocraqueo como soporte de platino/paladio para aumentar el contenido aromático de los productos reformulados de refinería. [10]
La zeolita tipo X se puede utilizar para adsorber selectivamente CO 2 de corrientes de gas [11] y se utiliza en la prepurificación del aire para la separación del aire industrial.
Debido a su estructura, comportamiento y propiedades ampliamente conocidas, la faujasita se utiliza a menudo como estándar en estudios catalíticos y de (ad/des)sorción en zeolitas, junto con MFI, FER y CHA [12] [13] [14] [15]