La descomposición de iones unimoleculares es la fragmentación de un ion en fase gaseosa en una reacción con una molecularidad de uno. [1] Los iones con suficiente energía interna pueden fragmentarse en un espectrómetro de masas , lo que en algunos casos puede degradar el rendimiento del espectrómetro de masas, pero en otros casos, como la espectrometría de masas en tándem , la fragmentación puede revelar información sobre la estructura del ion.
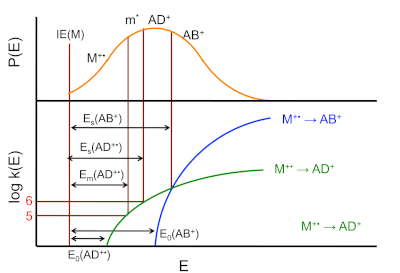
Un diagrama de Wahrhaftig (que lleva el nombre de Austin L. Wahrhaftig ) ilustra las contribuciones relativas en la descomposición de iones unimoleculares de la fragmentación directa y la fragmentación después de la reordenación. El eje x del diagrama representa la energía interna del ion. La parte inferior del diagrama muestra el logaritmo de la constante de velocidad k para la disociación unimolecular , mientras que la parte superior del diagrama indica la probabilidad de formar un ion producto particular. El trazo verde en la parte inferior del diagrama indica la velocidad de la reacción de reordenamiento dada por
y el trazo azul indica la reacción de escisión directa
Una constante de velocidad de 10 6 s −1 es suficientemente rápida para la descomposición de iones dentro de la fuente de iones de un espectrómetro de masas típico. Los iones con constantes de velocidad inferiores a 10 6 s −1 y superiores a aproximadamente 10 5 s −1 (vidas entre 10 −5 y 10 −6 s) tienen una alta probabilidad de descomponerse en el espectrómetro de masas entre la fuente de iones y el detector. Estas constantes de velocidad se indican en el diagrama de Wahrhaftig mediante las líneas discontinuas log k = 5 y log k = 6.
En el gráfico de constante de velocidad se indica la energía crítica de reacción (también llamada energía de activación ) para la formación de AD + , E0 ( AD + ) y AB + , E0 (AB + ). Estos representan la energía interna mínima de ABCD + requerida para formar los respectivos iones producto: la diferencia en la energía del punto cero de ABCD + y la del complejo activado .
Cuando la energía interna de ABCD + es mayor que Em ( AD + ), los iones son metaestables (indicado por m * ); esto ocurre cerca de log k > 5. Un ion metaestable tiene suficiente energía interna para disociarse antes de la detección. [2] [3] La energía E s (AD + ) se define como la energía interna de ABCD + que resulta en una probabilidad igual de que ABCD + y AD + abandonen la fuente de iones, lo que ocurre cerca de log k = 6. Cuando el ion precursor tiene una energía interna igual a E s (AB + ), las velocidades de formación de AD + y AB + son iguales.

Como todas las reacciones químicas, la descomposición unimolecular de iones está sujeta al control de la reacción termodinámica versus cinética : el producto cinético se forma más rápido, mientras que el producto termodinámico es más estable. [4] En la descomposición de ABCD + , la reacción para formar AD + se ve favorecida termodinámicamente y la reacción para formar AB + se ve favorecida cinéticamente. Esto se debe a que la reacción AD + tiene entalpía favorable y la AB + tiene entropía favorable .
En la reacción representada esquemáticamente en la figura, la reacción de reordenamiento forma un doble enlace B=C y un nuevo enlace simple AD, que compensa la escisión de los enlaces AB y CD. La formación de AB + requiere la escisión del enlace sin la formación de enlace compensatorio. Sin embargo, el efecto estérico hace que sea más difícil para la molécula alcanzar el estado de transición de reordenamiento y formar AD + . El complejo activado con requisitos estéricos estrictos se denomina "complejo apretado", mientras que el estado de transición sin tales requisitos se denomina "complejo laxo".