La eliminación de β-hidruro es una reacción en la que un grupo alquilo unido a un centro metálico se convierte en el hidruro correspondiente unido al metal y en un alqueno . [1] El alquilo debe tener hidrógenos en el carbono β. Por ejemplo, los grupos butilo pueden experimentar esta reacción, pero los grupos metilo no. El complejo metálico debe tener un sitio vacío (o vacante) cis al grupo alquilo para que se produzca esta reacción. Además, para una fácil escisión del enlace C–H, se necesita un par de electrones para la donación al orbital σ* del enlace C–H. Por tanto, los alquilos metálicos d0 son generalmente más estables a la eliminación de β-hidruro que los alquilos metálicos d2 y superiores y pueden formar complejos agósticos aislables , incluso si hay un sitio de coordinación vacío disponible. [2]
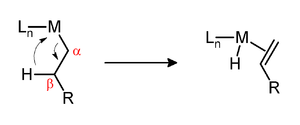
La eliminación de β-hidruro puede ser un paso vital en una reacción o una reacción secundaria improductiva . El proceso de olefinas superiores de Shell se basa en la eliminación de β-hidruro para producir α - olefinas que se utilizan para producir detergentes. Ilustrativo de una eliminación de β-hidruro a veces indeseable, la eliminación de β-hidruro en la polimerización Ziegler-Natta da como resultado polímeros de menor peso molecular. En el caso de acoplamientos catalizados por níquel y paladio de haluros de arilo con reactivos de Grignard de alquilo , la eliminación de β-hidruro puede reducir el rendimiento. La producción de polímeros ramificados a partir de etileno se basa en el recorrido de la cadena , un paso clave del cual es la eliminación de β-hidruro.
En algunos casos, la eliminación del β-hidruro es el primero de una serie de pasos. Por ejemplo, en la síntesis de RuHCl(CO)(PPh3 ) 3 a partir de tricloruro de rutenio , trifenilfosfina y 2-metoxietanol , un complejo de alcóxido intermedio sufre una eliminación del β-hidruro para formar el ligando hidruro y el aldehído unido a pi que luego se convierte en el ligando carbonilo ( monóxido de carbono ).
Existen varias estrategias para evitar la eliminación del β-hidruro. La estrategia más común es emplear ligandos de alquilo que no tengan ningún átomo de hidrógeno en la posición β. Los sustituyentes comunes incluyen metilo y neopentilo . La eliminación del β-hidruro también se inhibe cuando la reacción produciría un alqueno deformado. Esta situación se ilustra con la estabilidad de los complejos metálicos que contienen ligandos de norbornilo, donde el producto de eliminación del β-hidruro violaría la regla de Bredt . [3]
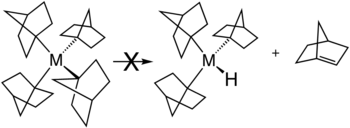
Los ligandos de alquilo voluminosos, como el terc -butilo o el trimetilsililo , pueden impedir que el átomo de hidrógeno se acerque a una configuración coplanar con respecto al metal y a los átomos α y β. Si el centro metálico no tiene sitios de coordinación vacíos, por ejemplo, si el complejo ya tiene una configuración de 18 electrones , tampoco es posible la eliminación del β-hidruro.
En algunos casos, los coligandos pueden imponer geometrías que inhiben la eliminación del β-hidruro. En el ejemplo anterior, la eliminación no deseada del β-hidruro se evita utilizando una difosfina en la que los dos átomos de fósforo están separados en el espacio. Una forma de hacerlo es utilizar un ligando que abarca el espacio trans, como Xantphos . Como estos complejos metálicos tradicionalmente forman geometrías planares cuadradas , no se puede formar ningún sitio vacante cis respecto del grupo alquilo. Por lo tanto, se evita la eliminación del β-hidruro. (Véase ligando que abarca el espacio trans ).