
En el estudio de la isomería conformacional , el efecto gauche es una situación atípica donde una conformación gauche (grupos separados por un ángulo de torsión de aproximadamente 60°) es más estable que la conformación anti (180°). [2]
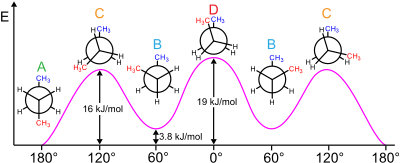
Existen efectos tanto estéricos como electrónicos que afectan la estabilidad relativa de los confórmeros. Por lo general, los efectos estéricos predominan para colocar a los sustituyentes grandes lejos unos de otros. Sin embargo, este no es el caso de ciertos sustituyentes, típicamente aquellos que son altamente electronegativos . En cambio, existe una preferencia electrónica por que estos grupos sean torpes. Los ejemplos típicamente estudiados incluyen 1,2-difluoroetano (H 2 FCCFH 2 ), etilenglicol y estructuras vecinales de difluoroalquilo.
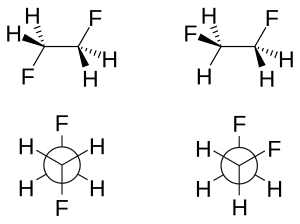
Existen dos explicaciones principales para el efecto gauche: hiperconjugación y enlaces doblados . En el modelo de hiperconjugación, la donación de densidad electrónica del orbital de enlace C−H σ al orbital antienlazante C−F σ * se considera la fuente de estabilización en el isómero gauche. Debido a la mayor electronegatividad del flúor, el orbital C−H σ es un mejor donante de electrones que el orbital C−F σ, mientras que el orbital C−F σ * es un mejor aceptor de electrones que el orbital C−H σ * . Solo la conformación gauche permite una buena superposición entre el mejor donante y el mejor aceptor.
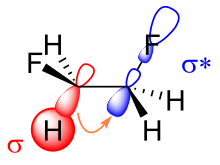
La clave para explicar el efecto gauche en el difluoroetano es el aumento del carácter orbital p de ambos enlaces C−F debido a la gran electronegatividad del flúor. Como resultado, la densidad electrónica aumenta por encima y por debajo, a la izquierda y a la derecha del enlace C−C central. La superposición orbital reducida resultante se puede compensar parcialmente cuando se supone una conformación gauche, formando un enlace doblado. De estos dos modelos, la hiperconjugación se considera generalmente la causa principal detrás del efecto gauche en el difluoroetano. [5] [6]
La geometría molecular de ambos rotámeros se puede obtener experimentalmente mediante espectroscopia infrarroja de alta resolución aumentada con trabajo in silico . [2] De acuerdo con el modelo descrito anteriormente, la longitud del enlace carbono-carbono es mayor para el antirrotámero (151,4 pm frente a 150 pm). La repulsión estérica entre los átomos de flúor en el rotámero gauche provoca un aumento de los ángulos de enlace CCF (en 3,2°) y un aumento de los ángulos diedros FCCF (de los 60° predeterminados a 71°).
En el compuesto relacionado 1,2-difluoro-1,2-difeniletano, se encontró que el isómero treo (por difracción de rayos X y a partir de las constantes de acoplamiento de RMN ) tiene una conformación anti entre los dos grupos fenilo y los dos grupos flúor y se encontró una conformación gauche para ambos grupos para el isómero eritro . [7] Según los resultados in silico , esta conformación es más estable en 0,21 kcal/mol (880 J/mol).
También se ha descrito un efecto gauche para una molécula que presenta una matriz totalmente sinérgica de cuatro sustituyentes flúor consecutivos. La reacción para instalar el cuarto es estereoselectiva : [8]

El efecto gauche también se observa en el 1,2-dimetoxietano [ cita requerida ] y algunos compuestos dinitroalquilo vecinales.
El efecto cis del alqueno es una estabilización atípica análoga de ciertos alquenos.
El efecto gauche es muy sensible a los efectos del disolvente , debido a la gran diferencia de polaridad entre los dos confórmeros. Por ejemplo, el 2,3-dinitro-2,3-dimetilbutano, que en estado sólido existe solo en la conformación gauche, prefiere el confórmero gauche en solución de benceno en una proporción de 79:21, pero en tetracloruro de carbono , prefiere el confórmero anti en una proporción de 58:42. [9] Otro caso es el trans -1,2 difluorociclohexano, que tiene una mayor preferencia por el confórmero di-ecuatorial, en lugar del confórmero anti-diaxial, en disolventes más polares. [6]