El uroporfirinógeno III es un tetrapirrol , el primer intermediario macrocíclico en la biosíntesis de hemo , clorofila , vitamina B12 y sirohema . Es un compuesto incoloro, como otros porfirinógenos . [1]
La estructura molecular del uroporfirinógeno III se puede describir como un núcleo de hexahidroporfina , donde cada anillo de pirrol tiene los átomos de hidrógeno en sus dos carbonos más externos reemplazados por un grupo de ácido acético ( −CH 2 −COOH , "A") y un grupo de ácido propiónico ( −CH 2 −CH 2 −COOH , "P"). Los grupos se unen de forma asimétrica: dando la vuelta al macrociclo, el orden es AP-AP-AP-PA.
En la vía general de biosíntesis de porfirina, el uroporfirinógeno III se deriva del preuroporfirinógeno tetrapirrol lineal (un hidroximetilbilano sustituido ) por la acción de la enzima cosintasa uroporfirinógeno-III . [2] [3]
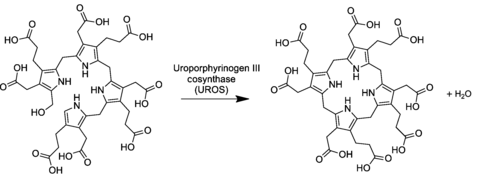
La conversión implica una inversión de la última unidad de pirrol (intercambiando así los grupos ácido acético y propiónico) y una reacción de condensación que cierra el macrociclo eliminando el hidroxilo final −OH con un átomo de hidrógeno del primer anillo.
En la biosíntesis de hemos y clorofilas, el uroporfirinógeno III se convierte en coproporfirinógeno III mediante la enzima uroporfirinógeno III descarboxilasa . En la biosíntesis de sirohemas, el uroporfirinógeno III es convertido por dos metil transferasas en dihidrosirohidroclorina , que posteriormente se oxida sirohidroclorina , un precursor del grupo protésico sirohema .
Si la uroporfirinógeno-III sintasa no está presente o está inactiva, el hidroximetilbilano se ciclará espontáneamente en el isómero estructural uroporfirinógeno I , que se diferencia del isómero III en que los grupos ácido acético ("A") y ácido propiónico ("P") están dispuestos. en un orden rotacionalmente simétrico, AP-AP-AP-AP. En este caso, el siguiente paso produjo coproporfirinógeno I , que se acumula y conduce a la condición patológica de porfiria eritropoyética congénita [3].