


En química teórica , un sistema conjugado es un sistema de orbitales p conectados con electrones deslocalizados en una molécula , que en general reduce la energía total de la molécula y aumenta la estabilidad . Se representa convencionalmente con enlaces simples y múltiples alternos . Pares libres , radicales o iones carbenio pueden formar parte del sistema, que puede ser cíclico , acíclico, lineal o mixto. El término "conjugado" fue acuñado en 1899 por el químico alemán Johannes Thiele . [1]
La conjugación es la superposición de un orbital p con otro a través de un enlace σ adyacente (en los metales de transición , pueden estar involucrados orbitales d). [2] [un]
Un sistema conjugado tiene una región de orbitales p superpuestos, uniendo las ubicaciones interyacentes que, como ilustran los diagramas simples, no tienen un enlace π. Permiten una deslocalización de electrones π a través de todos los orbitales p adyacentes alineados. [3] Los electrones π no pertenecen a un enlace simple o átomo , sino a un grupo de átomos.
Las moléculas que contienen sistemas conjugados de orbitales y electrones se denominan moléculas conjugadas , que tienen orbitales p superpuestos en tres o más átomos. Algunas moléculas orgánicas conjugadas simples son el 1,3-butadieno, el benceno y los carbocationes alílicos . [4] Los sistemas conjugados más grandes se encuentran en el grafeno , el grafito , los polímeros conductores y los nanotubos de carbono .

La conjugación es posible mediante enlaces simples y dobles alternos en los que cada átomo suministra un orbital p perpendicular al plano de la molécula. Sin embargo, esa no es la única forma en que se produce la conjugación. Siempre que cada átomo contiguo en una cadena tenga un orbital p disponible, el sistema puede considerarse conjugado. Por ejemplo, el furano es un anillo de cinco miembros con dos dobles enlaces alternos flanqueando un oxígeno . El oxígeno tiene dos pares libres , uno de los cuales ocupa un orbital p perpendicular al anillo en esa posición, manteniendo así la conjugación de ese anillo de cinco miembros por superposición con el orbital p perpendicular en cada uno de los átomos de carbono adyacentes. El otro par solitario permanece en el plano y no participa en la conjugación.
En general, cualquier carbono o heteroátomo con hibridación sp 2 o sp , incluidos los que llevan un orbital vacío o un orbital de par solitario, puede participar en sistemas conjugados, aunque los pares solitarios no siempre participan en un sistema conjugado. Por ejemplo, en la piridina, el átomo de nitrógeno ya participa en el sistema conjugado a través de un doble enlace formal con un carbono adyacente, por lo que el par solitario permanece en el plano del anillo en un orbital híbrido sp 2 y no participa en la conjugación. Un requisito para la conjugación es la superposición orbital; por tanto, el sistema conjugado debe ser plano (o casi). Como consecuencia, los pares solitarios que participan en sistemas conjugados ocuparán orbitales de carácter p puro en lugar de orbitales híbridos sp n típicos de los pares solitarios no conjugados.

Un modelo común para el tratamiento de moléculas conjugadas es un tratamiento de enlace de valencia compuesto/teoría de orbitales moleculares de Hückel (VB/HMOT), en el que la estructura σ de la molécula se separa del sistema (o sistemas) π de la molécula ( consulte la artículo sobre los modelos sigma-pi y orbitales equivalentes para este modelo y un tratamiento alternativo ). Aunque el enlace σ también se puede tratar utilizando un enfoque deslocalizado, generalmente es el enlace π el que se considera cuando se invoca el enlace deslocalizado en el contexto de moléculas orgánicas simples.
Marco sigma (σ) : El marco σ se describe mediante un esquema de enlace estrictamente localizado y consta de enlaces σ formados a partir de las interacciones entre los orbitales atómicos hibridados sp 3 -, sp 2 - y sp- en los elementos del grupo principal (y 1s átomos orbitales del hidrógeno), junto con pares solitarios localizados derivados de orbitales híbridos llenos y no enlazantes. La interacción que resulta en el enlace σ toma la forma de superposición cabeza a cabeza del lóbulo más grande de cada orbital híbrido (o el lóbulo esférico único de un orbital 1s de hidrógeno). Cada orbital atómico aporta un electrón cuando los orbitales se superponen por pares para formar enlaces σ de dos electrones, o dos electrones cuando el orbital constituye un par solitario. Estos orbitales localizados (enlazantes y no enlazantes) están todos ubicados en el plano de la molécula, con enlaces σ localizados principalmente entre núcleos a lo largo del eje internuclear.
Sistema o sistemas Pi (π) : ortogonal a la estructura σ descrita anteriormente, el enlace π se produce por encima y por debajo del plano de la molécula donde tiene lugar el enlace σ. Los sistemas π de la molécula se forman mediante la interacción de orbitales atómicos p no hibridados en átomos que emplean hibridación sp 2 - y sp. La interacción que resulta en el enlace π tiene lugar entre orbitales p que son adyacentes en virtud de un enlace σ que une los átomos y toma la forma de superposición de lado a lado de los dos lóbulos igualmente grandes que forman cada orbital p. Los átomos que tienen hibridación sp 3 no tienen un orbital p no hibridado disponible para participar en el enlace π y su presencia necesariamente termina un sistema π o separa dos sistemas π. Un orbital de base p que participa en un sistema π puede aportar un electrón (que corresponde a la mitad de un "doble enlace" formal), dos electrones (que corresponde a un "par solitario" deslocalizado) o cero electrones (que corresponde a un orbital formalmente "vacío"). El enlace para sistemas π formados a partir de la superposición de más de dos orbitales p se maneja utilizando el enfoque de Hückel para obtener una aproximación (cualitativa) de orden cero de los orbitales moleculares de simetría π que resultan del enlace π deslocalizado.

Este modelo simple de enlace químico es exitoso para la descripción de la mayoría de las moléculas de valencia normal que consisten únicamente en elementos del bloque s y p, aunque los sistemas que involucran enlaces deficientes en electrones, incluidos los carbocationes no clásicos, los grupos de litio y boro y los centros hipervalentes, requieren modificaciones significativas en las que también se permite que los enlaces σ se deslocalicen y quizás se traten mejor con orbitales moleculares canónicos que se deslocalizan en toda la molécula. Del mismo modo, los organometálicos de los bloques d y f también se describen de forma inadecuada mediante este modelo simple. Los enlaces en anillos pequeños tensos (como el ciclopropano o el epóxido) no se describen bien mediante una separación estricta σ/π, ya que los enlaces entre átomos en el anillo consisten en " enlaces doblados " o "enlaces tipo banana" que están curvados hacia afuera y son intermedios en su forma. naturaleza entre los enlaces σ y π. Sin embargo, los químicos orgánicos utilizan con frecuencia el lenguaje de este modelo para racionalizar la estructura y reactividad de compuestos orgánicos típicos.
Los electrones en los sistemas π conjugados son compartidos por todos los átomos adyacentes sp 2 y con hibridación sp que contribuyen a orbitales atómicos p paralelos y superpuestos. Como tal, los átomos y los electrones π involucrados se comportan como un gran sistema enlazado. Estos sistemas a menudo se denominan ' enlaces π de electrones k de centro n ', denotados de forma compacta por el símbolo Πkn
, para enfatizar este comportamiento. Por ejemplo, se dice que los electrones π deslocalizados en el anión acetato y el benceno están involucrados en Π4
3y Π6
6sistemas, respectivamente ( ver el artículo sobre enlace de tres centros y cuatro electrones ). Es importante reconocer que, en términos generales, estos enlaces multicéntricos corresponden a la ocupación de varios orbitales moleculares (MO) con distintos grados de carácter enlazante o no enlazante (el llenado de orbitales con carácter antienlazante es poco común). Cada uno está ocupado por uno o dos electrones de acuerdo con el principio de aufbau y la regla de Hund . Los dibujos animados que muestran orbitales p superpuestos, como el del benceno a continuación, muestran los orbitales atómicos p básicos antes de que se combinen para formar orbitales moleculares. De conformidad con el principio de exclusión de Pauli , la superposición de orbitales p no da como resultado la formación de un MO grande que contenga más de dos electrones.
La teoría de Hückel MO es un enfoque comúnmente utilizado para obtener una imagen de orden cero de orbitales moleculares π deslocalizados, incluido el signo matemático de la función de onda en varias partes de la molécula y las ubicaciones de los planos nodales. Es particularmente fácil de aplicar para hidrocarburos conjugados y proporciona una aproximación razonable siempre que se suponga que la molécula es plana con una buena superposición de orbitales p.
La estimación cuantitativa de la estabilización a partir de la conjugación es notoriamente polémica y depende de los supuestos implícitos que se hacen al comparar sistemas o reacciones de referencia. La energía de estabilización se conoce como energía de resonancia cuando se define formalmente como la diferencia de energía entre las especies químicas reales y las especies hipotéticas que presentan un enlace π localizado que corresponde a la forma de resonancia más estable . [5] Esta energía no se puede medir y probablemente seguirá siendo difícil encontrar una definición precisa aceptada por la mayoría de los químicos. Sin embargo, se pueden hacer algunas afirmaciones generales. En general, la estabilización es más significativa para los sistemas catiónicos que para los neutros. Para el buta-1,3-dieno , una medida aproximada de estabilización es la energía de activación para la rotación del enlace C2-C3. Esto sitúa la estabilización por resonancia en torno a las 6 kcal/mol. [6] La comparación de los calores de hidrogenación del 1,4-pentadieno y del 1,3-pentadieno estima un valor ligeramente más modesto de 3,5 kcal/mol. [7] A modo de comparación, el catión alilo tiene una barrera de rotación en fase gaseosa de alrededor de 38 kcal/mol, [8] una penalización mucho mayor por la pérdida de conjugación. La comparación de las afinidades del ion hidruro del catión propilo y del catión alilo, corregidas por efectos inductivos, da como resultado una estimación considerablemente menor de la energía de resonancia de 20 a 22 kcal/mol. [9] Sin embargo, está claro que la conjugación estabiliza el catión alilo en mucha mayor medida que el buta-1,3-dieno. A diferencia del efecto normalmente menor de la conjugación neutra, la estabilización aromática puede ser considerable. Las estimaciones de la energía de resonancia del benceno oscilan entre 36 y 73 kcal/mol. [10]

También existen otros tipos de interacciones que generalizan la idea de interactuar orbitales p en un sistema conjugado. El concepto de hiperconjugación sostiene que ciertos enlaces σ también pueden deslocalizarse en un orbital desocupado bajo de un sistema π o en un orbital p desocupado. La hiperconjugación se invoca comúnmente para explicar la estabilidad de los radicales y carbocationes sustituidos con alquilo. La hiperconjugación es menos importante para especies en las que todos los átomos satisfacen la regla del octeto, pero un estudio computacional reciente apoya la hiperconjugación como el origen de la mayor estabilidad de los alquenos con un mayor grado de sustitución ( regla de Zaitsev ). [11]
La homoconjugación [12] es una superposición de dos sistemas π separados por un grupo no conjugante, como CH 2 . Los ejemplos inequívocos son comparativamente raros en sistemas neutrales, debido a un beneficio energético comparativamente menor que es fácilmente anulado por una variedad de otros factores; sin embargo, son comunes en sistemas catiónicos en los que se puede derivar un gran beneficio energético de la deslocalización de la carga positiva ( consulte el artículo sobre homoaromaticidad para más detalles ). [13] Los sistemas neutrales generalmente requieren geometrías restringidas que favorezcan la interacción para producir grados significativos de homoconjugación. [14] En el siguiente ejemplo, las frecuencias de estiramiento del carbonilo de los espectros IR de los respectivos compuestos demuestran homoconjugación, o falta de ella, en las moléculas en estado fundamental neutro.
Debido al carácter π parcial de los enlaces formalmente σ en un anillo de ciclopropano, también se ha obtenido evidencia de la transmisión de "conjugación" a través de ciclopropanos. [15]
Dos sistemas π apropiadamente alineados cuyos extremos se encuentran en ángulos rectos pueden participar en espiroconjugación [16] o espiroaromaticidad [ ancla rota ] .

La vinología es la extensión de un grupo funcional a través de un sistema de enlace orgánico conjugado, que transmite efectos electrónicos . [17]


Los compuestos cíclicos pueden estar total o parcialmente conjugados. Los anulenos , hidrocarburos monocíclicos completamente conjugados, pueden ser aromáticos, no aromáticos o antiaromáticos.
Los compuestos que tienen un sistema conjugado plano monocíclico que contiene (4 n + 2) electrones π para números enteros n son aromáticos y exhiben una estabilidad inusual. El ejemplo clásico del benceno tiene un sistema de seis electrones π que, junto con el anillo plano de enlaces C-C σ que contienen 12 electrones y los enlaces radiales C-H σ que contienen seis electrones, forma el anillo de benceno termodinámica y cinéticamente estable , el común. Núcleo de los compuestos aromáticos bencenoideos. Para el benceno en sí, predominan dos estructuras de Lewis conjugadas equivalentes (las llamadas estructuras de Kekulé). [18] [19] La verdadera estructura electrónica es, por lo tanto, una combinación mecánico-cuántica (híbrido de resonancia) de estos contribuyentes, que da como resultado los enlaces C-C observados experimentalmente que son intermedios entre enlaces simples y dobles y de igual fuerza y longitud. En la imagen de los orbitales moleculares, los seis orbitales atómicos p del benceno se combinan para dar seis orbitales moleculares. Tres de estos orbitales, que se encuentran en energías más bajas que el orbital p aislado y, por lo tanto, tienen un carácter de enlace neto (un orbital molecular está fuertemente enlazado, mientras que los otros dos son iguales en energía pero se enlazan en menor medida) están ocupados por seis electrones. , mientras que tres orbitales desestabilizados de carácter antienlazante general permanecen desocupados. El resultado es una fuerte estabilización aromática termodinámica y cinética. Ambos modelos describen anillos de densidad de electrones π por encima y por debajo de la estructura de enlaces C – C σ.
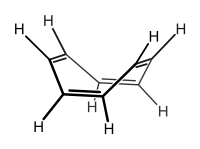
No todos los compuestos con enlaces dobles y simples alternos son aromáticos. El ciclooctatetraeno , por ejemplo, posee enlaces simples y dobles alternos. La molécula normalmente adopta una conformación de "tina" . Debido a que los orbitales p de la molécula no se alinean bien en esta molécula no plana, los enlaces π están esencialmente aislados y no conjugados. La falta de conjugación permite que la molécula de 8 electrones π evite la antiaromaticidad , un efecto desestabilizador asociado con sistemas cíclicos conjugados que contienen 4 n π ( n = 0, 1, 2, ...) electrones. Este efecto se debe a la colocación de dos electrones en dos orbitales degenerados no enlazantes (o casi no enlazantes) de la molécula, lo que, además de reducir drásticamente la estabilización termodinámica de la deslocalización, obligaría a la molécula a adoptar un carácter dirradical triplete, o hacer que sufra la distorsión de Jahn-Teller para aliviar la degeneración. Esto tiene el efecto de aumentar considerablemente la reactividad cinética de la molécula. Debido a la falta de interacciones de largo alcance, el ciclooctatetraeno adquiere una conformación no plana y de carácter no aromático, comportándose como un alqueno típico. Por el contrario, se ha descubierto experimentalmente que los derivados del dication ciclooctatetraeno y del dianión son planos, de acuerdo con la predicción de que son sistemas aromáticos estabilizados con 6 y 10 electrones π, respectivamente. Dado que la antiaromaticidad es una propiedad que las moléculas intentan evitar siempre que sea posible, se cree que sólo unas pocas especies observadas experimentalmente son antiaromáticas. Los cationes ciclobutadieno y ciclopentadienilo se citan comúnmente como ejemplos de sistemas antiaromáticos.
En un sistema pi conjugado, los electrones pueden capturar ciertos fotones a medida que los electrones resuenan a lo largo de una cierta distancia de los orbitales p, de manera similar a cómo una antena de radio detecta fotones a lo largo de su longitud. Normalmente, cuanto más conjugado (más largo) sea el sistema pi, más larga será la longitud de onda del fotón que se podrá capturar. Los compuestos cuyas moléculas contienen una cantidad suficiente de enlaces conjugados pueden absorber la luz en la región visible y, por lo tanto, aparecen coloridos a la vista, generalmente amarillos o rojos. [20]
Muchos tintes utilizan sistemas de electrones conjugados para absorber la luz visible , dando lugar a colores fuertes. Por ejemplo, la larga cadena de hidrocarburos conjugados del betacaroteno da lugar a su intenso color naranja. Cuando un electrón en el sistema absorbe un fotón de luz de la longitud de onda correcta , puede ser promovido a un nivel de energía más alto. Un modelo simple de los niveles de energía lo proporciona el problema de la mecánica cuántica de una partícula unidimensional en una caja de longitud L, que representa el movimiento de un electrón π a lo largo de una larga cadena conjugada de átomos de carbono. En este modelo, la energía de absorción más baja posible corresponde a la diferencia de energía entre el orbital molecular ocupado más alto ( HOMO ) y el orbital molecular desocupado más bajo (LUMO). Para una cadena de n enlaces C=C o 2 n átomos de carbono en el estado fundamental molecular , hay 2 n electrones π que ocupan n orbitales moleculares, de modo que la brecha de energía es [21]
Dado que la longitud de la caja L aumenta aproximadamente linealmente con el número de enlaces C=C n , esto significa que la energía Δ E de un fotón absorbido en la transición HOMO-LUMO es aproximadamente proporcional a 1/ n . La longitud de onda del fotón λ = hc /Δ E es entonces aproximadamente proporcional a n . Aunque este modelo es muy aproximado, λ en general aumenta con n (o L ) para moléculas similares. Por ejemplo, las longitudes de onda de absorción HOMO-LUMO para butadieno , hexatrieno y octatetraeno conjugados son 217 nm, 252 nm y 304 nm respectivamente. [22] Sin embargo, para una buena concordancia numérica de la partícula en un modelo de caja con el experimento, se deben tener en cuenta las alternancias de longitud de enlace simple/enlace doble de los polienos. [23] Alternativamente, se puede utilizar el método de Hückel , que también está diseñado para modelar la estructura electrónica de sistemas conjugados.
Muchas transiciones electrónicas en sistemas π conjugados son de un orbital molecular (MO) predominantemente enlazante a un MO predominantemente antienlazante (π a π * ), pero los electrones de pares libres no enlazantes también pueden promoverse a un MO de sistema π (n a π * ) como suele ocurrir en los complejos de transferencia de carga . Un electrón realiza una transición de HOMO a LUMO si lo permiten las reglas de selección para transiciones electromagnéticas . Los sistemas conjugados de menos de ocho dobles enlaces conjugados se absorben sólo en la región ultravioleta y son incoloros para el ojo humano. Con cada doble enlace agregado, el sistema absorbe fotones de longitud de onda más larga (y de menor energía), y el compuesto varía de color amarillo a rojo. Los compuestos que son azules o verdes normalmente no dependen únicamente de dobles enlaces conjugados.
Esta absorción de luz en el espectro ultravioleta a visible se puede cuantificar mediante espectroscopia ultravioleta-visible y constituye la base de todo el campo de la fotoquímica .
Los sistemas conjugados que se utilizan ampliamente para pigmentos y colorantes sintéticos son los compuestos diazo y azo y los compuestos de ftalocianina.
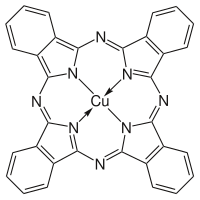
Los sistemas conjugados no sólo tienen excitaciones de baja energía en la región espectral visible sino que también aceptan o donan electrones fácilmente. Las ftalocianinas , que, como el azul de ftalocianina BN y el verde de ftalocianina G , a menudo contienen un ión de metal de transición, intercambian un electrón con el ión de metal de transición complejado que cambia fácilmente su estado de oxidación . Los pigmentos y tintes como estos son complejos de transferencia de carga .
Las porfirinas tienen sistemas de anillos moleculares conjugados ( macrociclos ) que aparecen en muchas enzimas de sistemas biológicos. Como ligando , la porfirina forma numerosos complejos con iones metálicos como el hierro en la hemoglobina que tiñe la sangre de rojo. La hemoglobina transporta oxígeno a las células de nuestro cuerpo. Los complejos porfirina-metal suelen tener colores fuertes. Una unidad de anillo estructural molecular similar llamada clorina forma un complejo similar con magnesio en lugar de hierro cuando forma parte de las formas más comunes de moléculas de clorofila , dándoles un color verde. Otra unidad de macrociclo similar es la corrina , que se compleja con el cobalto al formar parte de las moléculas de cobalamina , constituyendo la Vitamina B12 , que es de color rojo intenso. La unidad corrina tiene seis dobles enlaces conjugados pero no está conjugada en todo su anillo de macrociclo.
Los sistemas conjugados forman la base de los cromóforos , que son partes de una molécula que absorben la luz y que pueden provocar que un compuesto se coloree. Estos cromóforos suelen estar presentes en diversos compuestos orgánicos y, a veces, en polímeros que están coloreados o brillan en la oscuridad. Los cromóforos a menudo consisten en una serie de enlaces conjugados y/o sistemas de anillos, comúnmente aromáticos, que pueden incluir enlaces C-C, C=C, C=O o N=N.

Los cromóforos conjugados se encuentran en muchos compuestos orgánicos , incluidos los colorantes azoicos (también aditivos alimentarios artificiales ), compuestos en frutas y verduras ( licopeno y antocianidinas ), fotorreceptores del ojo y algunos compuestos farmacéuticos como los siguientes:

Las nanopartículas de polímeros conjugados (PDots) se ensamblan a partir de polímeros conjugados fluorescentes hidrofóbicos, junto con polímeros anfifílicos para proporcionar solubilidad en agua. Los puntos son etiquetas importantes para la microscopía de fluorescencia de molécula única , basadas en alto brillo, falta de parpadeo o fracción oscura y fotoblanqueo lento . [24] [25]
{{cite book}}: Mantenimiento CS1: falta el editor de la ubicación ( enlace )