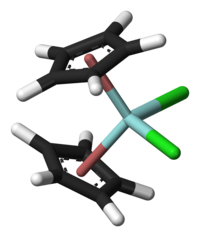
Un complejo de ciclopentadienilo es un complejo de coordinación de un metal y grupos ciclopentadienilo ( C
5h−
5, abreviado como Cp − ). Los ligandos de ciclopentadienilo casi invariablemente se unen a metales como un modo de enlace pentahapto ( η 5 -). La interacción metal-ciclopentadienilo generalmente se dibuja como una sola línea desde el centro del metal hasta el centro del anillo Cp. [1] [2]
Los complejos de bis ciclopentadienilo se denominan metalocenos . Un ejemplo famoso de este tipo de complejo es el ferroceno (FeCp 2 ), que tiene muchos análogos para otros metales, como el cromoceno (CrCp 2 ), el cobaltoceno (CoCp 2 ) y el níqueloceno (NiCp 2 ). Cuando los anillos Cp son mutuamente paralelos, el compuesto se conoce como complejo sándwich . Esta área de la química organometálica se desarrolló por primera vez en la década de 1950. Los metalocenos curvados están representados por compuestos del tipo [MCp 2 L x ]. Algunos son catalizadores para la polimerización del etileno . [3] Los metalocenos suelen ser térmicamente estables y se utilizan como catalizadores en diversos tipos de reacciones.
Complejos de Cp de ligando mixto que contienen ligando de Cp y uno o más ligandos diferentes. Son más numerosos. Un ejemplo ampliamente estudiado es el dímero Fp , (Cp 2 Fe 2 (CO) 4 ). Los compuestos monometálicos que presentan un solo anillo Cp se conocen a menudo como compuestos de medio sándwich o compuestos de taburete de piano, siendo un ejemplo el metilciclopentadienilmanganeso tricarbonilo (CpMn(CO) 3 ).
Los cinco átomos de carbono de un ligando Cp están unidos al metal en la gran mayoría de los complejos M-Cp. Este modo de enlace se llama coordinación η 5 . El enlace M-Cp surge de la superposición de los cinco orbitales moleculares π del ligando Cp con los orbitales s, p y d del metal. Estos complejos se denominan complejos π. Casi todos los metales de transición emplean este modo de coordinación. [1]
En casos relativamente raros, el Cp se une a los metales a través de un solo centro de carbono. Este tipo de interacciones se describen como complejos σ porque solo tienen un enlace σ entre el metal y el grupo ciclopentadienilo. Ejemplos típicos de este tipo de complejo son los complejos de metales del grupo 14 como CpSiMe 3 . Un ejemplo de ambos es (Cp 2 Fe(CO) 2 ). Es probable que los complejos η 1 -Cp sean intermediarios en la formación de complejos η 5 -Cp.
Aún más raro, la unidad Cp puede unirse al metal a través de tres carbonos. En estos complejos η 3 -Cp, el enlace se parece al de los ligandos alílicos . Estos complejos, a veces denominados "complejos de Cp deslizados", se invocan como intermediarios en reacciones de deslizamiento de anillos .
Además, se conocen compuestos sándwich inversos con estructuras "metal-Cp-metal". [4]
Los compuestos se preparan generalmente mediante reacciones de metátesis de sales de compuestos de ciclopentadienilo de metales alcalinos con cloruros de metales de transición. Se utilizan habitualmente el ciclopentadienuro de sodio (NaCp) y el ciclopentadienuro de litio . El trimetilsililciclopentadieno ciclopentadieniltalio (CpTl) son fuentes alternativas. [1] Para la preparación de algunos complejos particularmente robustos, por ejemplo níqueloceno, se emplea ciclopentadieno en presencia de una base convencional como KOH. Cuando solo se instala un ligando Cp, los otros ligandos suelen ser carbonilo, halógeno, alquilo e hidruro.
La mayoría de los complejos de Cp se preparan mediante sustitución de complejos de Cp preformados mediante sustitución de haluro, CO y otros ligandos simples.
Un par de ligandos de ciclopentadienilo pueden unirse covalentemente dando lugar a los llamados metalocenos ansa. El ángulo entre los dos anillos Cp es fijo. También se detiene la rotación de los anillos alrededor del eje centroide del metal. Una clase relacionada de derivadas da lugar a los complejos de geometría restringida . En estos casos, un ligando Cp está unido a un ligando no Cp. Tales complejos se han comercializado para la producción de polipropileno.
El pentametilciclopentadieno da lugar a complejos de pentametilciclopentadienilo (Cp*). Estos ligandos son más básicos y más lipófilos. La sustitución de grupos metilo por sustituyentes más grandes produce ciclopentadienos tan sobrecargados que ya no son posibles los derivados pentaalquilo. Los ligandos bien estudiados de este tipo incluyen C 5 R 4 H − (R = iso-Pr) y 1,2,4-C 5 R 3 H 2 − (R = tert -Bu).
Los complejos de geometría restringida están relacionados con ansa-metalocenos, excepto que un ligando no está relacionado con Cp.
Los complejos de metales Cp se utilizan principalmente como reactivos estequiométricos en la investigación química. Los reactivos de ferrocenio son oxidantes. El cobaltoceno es un reductor fuerte y soluble.
Los derivados de Cp 2 TiCl 2 y Cp 2 ZrCl 2 son la base de algunos reactivos en síntesis orgánica . Tras el tratamiento con aluminoxano , estos dihaluros dan catalizadores para la polimerización de olefinas . Estas especies se denominan catalizadores de tipo Kaminsky .