

En química orgánica , un carboxilato es la base conjugada de un ácido carboxílico , RCOO − (o RCO−2). Es un ion con carga negativa .
Las sales de carboxilato son sales que tienen la fórmula general M(RCOO) n , donde M es un metal y n es 1, 2,.... Los ésteres de carboxilato tienen la fórmula general RCOOR′ (también escrita como RCO 2 R′ ), donde R y R′ son grupos orgánicos.
Los iones carboxilato se pueden formar mediante desprotonación de ácidos carboxílicos. Estos ácidos suelen tener un p K a inferior a 5, lo que significa que pueden ser desprotonados por muchas bases, como el hidróxido de sodio o el bicarbonato de sodio . [1] : 271–2
Los ácidos carboxílicos se disocian fácilmente en un anión carboxilato y un ion hidrógeno cargado positivamente (protón), mucho más fácilmente que los alcoholes (en un ion alcóxido y un protón), porque el ion carboxilato se estabiliza por resonancia . La carga negativa que queda después de la desprotonación del grupo carboxilo se deslocaliza entre los dos átomos de oxígeno electronegativos en una estructura de resonancia. Si el grupo R es un grupo aceptor de electrones (como –CF 3 ), la basicidad del carboxilato se debilitará aún más. [1] : 264–5
Esta deslocalización del electrón significa que ambos átomos de oxígeno tienen una carga negativa menos fuerte: por lo tanto, el protón positivo es atraído menos fuertemente hacia el grupo carboxilato una vez que lo ha abandonado; por tanto, el ion carboxilato es más estable y menos básico como resultado de la estabilización por resonancia de la carga negativa. Por el contrario, un ion alcóxido , una vez formado, tendría una fuerte carga negativa localizada en su único átomo de oxígeno, lo que atraería fuertemente a los protones cercanos (de hecho, los alcóxidos son bases muy fuertes). Debido a la estabilización por resonancia, los ácidos carboxílicos tienen valores de p K a mucho más bajos (y por lo tanto son ácidos más fuertes) que los alcoholes . Por ejemplo, el valor p K a del ácido acético es 4,8, mientras que el etanol tiene un p K a de 16. Por lo tanto, el ácido acético es un ácido mucho más fuerte que el etanol. Esto a su vez significa que para soluciones equimolares de un ácido carboxílico o un alcohol en agua, el ácido carboxílico tendría un pH mucho más bajo . [1] : 263–7
Las sales de ácidos carboxílicos con un átomo de hidrógeno en posición alfa junto al grupo carboxilato se pueden convertir en dianiones con bases fuertes como la diisopropilamida de litio . Estos reaccionan con haluros de alquilo para dar derivados: [1] : 474
Los iones carboxilato son buenos nucleófilos . Reaccionan con haluros de alquilo para formar ésteres . La siguiente reacción muestra el mecanismo de reacción. [1] : 398–9
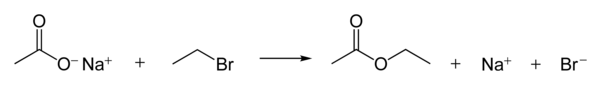
La nucleofilicidad de los iones carboxilato es mucho más débil que la de los iones hidróxido y alcóxido , pero más fuerte que la de los aniones haluro (en un disolvente aprótico polar , aunque existen otros efectos como la solubilidad del ion).
A diferencia de la reducción de éster, la reducción de carboxilato es diferente debido a la falta del grupo saliente y al átomo de carbono relativamente rico en electrones (debido a la carga negativa de los átomos de oxígeno). Con una pequeña cantidad de ácido, la reacción ocurre con hidruro de litio y aluminio al cambiar el LAH en ácido de Lewis AlH 3 en el proceso, convirtiendo el oxianión en 4 enlaces Al-O. [1] : 1212
Esta lista es para los casos en los que existe un artículo separado para el anión o sus derivados. Todos los demás ácidos orgánicos deben encontrarse en su ácido carboxílico original.