
En el sistema nervioso , una sinapsis [1] es una estructura que permite que una neurona (o célula nerviosa) pase una señal eléctrica o química a otra neurona o a la célula efectora objetivo.
Las sinapsis son esenciales para la transmisión de impulsos nerviosos de una neurona a otra, [2] desempeñando un papel clave al permitir una comunicación rápida y directa mediante la creación de circuitos. Además, una sinapsis sirve como unión donde se produce tanto la transmisión como el procesamiento de información, lo que la convierte en un medio vital de comunicación entre neuronas. [3] Las neuronas están especializadas para transmitir señales a células diana individuales, y las sinapsis son el medio por el cual lo hacen. En una sinapsis, la membrana plasmática de la neurona que pasa señales (la neurona presináptica ) entra en estrecha aposición con la membrana de la célula diana ( postsináptica ). Tanto el sitio presináptico como el postsináptico contienen una amplia gama de maquinaria molecular que une las dos membranas y lleva a cabo el proceso de señalización. En muchas sinapsis, la parte presináptica se sitúa sobre un axón y la parte postsináptica se sitúa sobre una dendrita o soma . Los astrocitos también intercambian información con las neuronas sinápticas, respondiendo a la actividad sináptica y, a su vez, regulando la neurotransmisión . [2] Las sinapsis (al menos las sinapsis químicas) se estabilizan en su posición mediante moléculas de adhesión sináptica (SAM) que se proyectan tanto desde la neurona presináptica como postsináptica y se unen donde se superponen; Los SAM también pueden ayudar en la generación y funcionamiento de sinapsis. [4] Además, los SAM coordinan la formación de sinapsis, y varios tipos trabajan juntos para lograr la notable especificidad de las sinapsis. [3] [5] En esencia, los SAM funcionan en sinapsis tanto excitadoras como inhibidoras, probablemente sirviendo como dispositivos para la transmisión de señales. [3]
Santiago Ramón y Cajal propuso que las neuronas no son continuas por todo el cuerpo, pero aun así se comunican entre sí, idea conocida como doctrina neuronal . [6] La palabra "sinapsis" fue introducida en 1897 por el neurofisiólogo inglés Charles Sherrington en el Libro de texto de fisiología de Michael Foster . [1] Sherrington luchó por encontrar un buen término que enfatizara una unión entre dos elementos separados , y el término real "sinapsis" fue sugerido por el erudito clásico inglés Arthur Woollgar Verrall , un amigo de Foster. [7] [8] La palabra se deriva del griego synapsis ( σύναψις ), que significa "conjunción", que a su vez deriva de synaptein ( συνάπτειν ), de syn ( σύν ) "juntos" y haptein ( ἅπτειν ) "sujetar" . [7] [9]
Sin embargo, si bien la brecha sináptica siguió siendo una construcción teórica, y en ocasiones se describió como una discontinuidad entre terminaciones axonales contiguas y dendritas o cuerpos celulares, los métodos histológicos que utilizaban los mejores microscopios ópticos de la época no pudieron resolver visualmente su separación, que ahora se sabe que es unos 20 nm. En la década de 1950 se necesitó el microscopio electrónico para mostrar la estructura más fina de la sinapsis con sus membranas y procesos pre y postsinápticos separados y paralelos, y la hendidura entre ambos. [10] [11] [12]
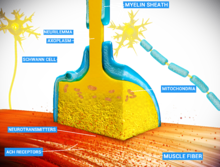
Las sinapsis químicas y eléctricas son dos formas de transmisión sináptica.
La formación de circuitos neuronales en los sistemas nerviosos parece depender en gran medida de las interacciones cruciales entre las sinapsis químicas y eléctricas. Por tanto, estas interacciones gobiernan la generación de la transmisión sináptica. [14] La comunicación sináptica es distinta de un acoplamiento efáptico , en el que la comunicación entre neuronas se produce a través de campos eléctricos indirectos. Una autapsis es una sinapsis química o eléctrica que se forma cuando el axón de una neurona hace sinapsis con las dendritas de la misma neurona.
Una entrada de Na+ impulsada por neurotransmisores excitadores abre canales catiónicos, despolarizando la membrana postsináptica hacia el umbral del potencial de acción. Por el contrario, los neurotransmisores inhibidores hacen que la membrana postsináptica se despolarice menos al abrir canales de Cl- o K+, lo que reduce la descarga. Dependiendo del lugar de liberación, de los receptores a los que se unen y de las circunstancias iónicas que encuentran, varios transmisores pueden ser excitadores o inhibidores. Por ejemplo, la acetilcolina puede excitar o inhibir según el tipo de receptores a los que se une. [18] Por ejemplo, el glutamato actúa como un neurotransmisor excitador, a diferencia del GABA, que actúa como un neurotransmisor inhibidor. Además, la dopamina es un neurotransmisor que ejerce efectos duales, mostrando impactos tanto excitadores como inhibidores al unirse a distintos receptores. [19]
El potencial de membrana impide que el Cl- entre en la célula, incluso cuando su concentración es mucho mayor en el exterior que en el interior. El potencial de reposo del Cl- en muchas neuronas es bastante negativo, casi igual al potencial de reposo. La apertura de canales de Cl- tiende a amortiguar el potencial de membrana, pero este efecto se contrarresta cuando la membrana comienza a despolarizarse, lo que permite que entren más iones de Cl- cargados negativamente a la célula. En consecuencia, resulta más difícil despolarizar la membrana y excitar la célula cuando los canales de Cl- están abiertos. Efectos similares resultan de la apertura de canales de K+. La importancia de los neurotransmisores inhibidores se desprende de los efectos de las toxinas que impiden su actividad. Por ejemplo, la estricnina se une a los receptores de glicina, bloqueando la acción de la glicina y provocando espasmos musculares, convulsiones y muerte. [18]
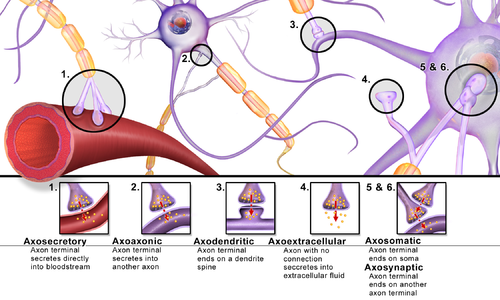
Las sinapsis se pueden clasificar por el tipo de estructuras celulares que actúan como componentes presinápticos y postsinápticos. La gran mayoría de las sinapsis en el sistema nervioso de los mamíferos son sinapsis axodendríticas clásicas (axón haciendo sinapsis sobre una dendrita); sin embargo, existe una variedad de otras disposiciones. Estos incluyen, entre otros, [ se necesita aclaración ] sinapsis axoaxónica , dendrodendrítica , axosecretora, axociliar, [20] somatodendrítica, dendrosomática y somatosomática. [ cita necesaria ]
De hecho, el axón puede hacer sinapsis con una dendrita, con un cuerpo celular o con otro axón o terminal de axón, así como con el torrente sanguíneo o de forma difusa con el tejido nervioso adyacente.
Los neurotransmisores son pequeñas moléculas de señal almacenadas en vesículas sinápticas rodeadas de membranas y liberadas mediante exocitosis. De hecho, un cambio de potencial eléctrico en la célula presináptica desencadena la liberación de estas moléculas. Al unirse a canales iónicos activados por transmisores, el neurotransmisor provoca una alteración eléctrica en la célula postsináptica y se difunde rápidamente a través de la hendidura sináptica. Una vez liberado, el neurotransmisor se elimina rápidamente, ya sea absorbido por la terminal nerviosa que lo produjo, absorbido por las células gliales cercanas o descompuesto por enzimas específicas en la hendidura sináptica. Numerosas proteínas portadoras de neurotransmisores dependientes de Na+ reciclan los neurotransmisores y permiten que las células mantengan velocidades de liberación rápidas.
En las sinapsis químicas, los canales iónicos activados por transmisores desempeñan un papel vital en la conversión rápida de impulsos químicos extracelulares en señales eléctricas. Estos canales están ubicados en la membrana plasmática de la célula postsináptica en la región de la sinapsis y se abren temporalmente en respuesta a la unión de la molécula del neurotransmisor, provocando una alteración momentánea en la permeabilidad de la membrana. Además, los canales activados por transmisores son comparativamente menos sensibles al potencial de membrana que los canales activados por voltaje, por lo que no pueden generar excitación autoamplificada por sí solos. Sin embargo, dan como resultado variaciones graduales en el potencial de membrana debido a la permeabilidad local, influenciadas por la cantidad y duración del neurotransmisor liberado en la sinapsis. [18]
Los neurotransmisores se unen a los receptores ionotrópicos de las neuronas postsinápticas, provocando su apertura o cierre. [19] Las variaciones en las cantidades de neurotransmisores liberados por la neurona presináptica pueden desempeñar un papel en la regulación de la eficacia de la transmisión sináptica. De hecho, la concentración de calcio citoplasmático participa en la regulación de la liberación de neurotransmisores de las neuronas presinápticas. [21]
La transmisión química implica varios procesos secuenciales:
La función de las neuronas depende de la polaridad celular . La estructura distintiva de las células nerviosas permite que los potenciales de acción viajen direccionalmente (desde las dendritas al cuerpo celular a lo largo del axón) y que estas señales luego sean recibidas y transmitidas por las neuronas postsinápticas o recibidas por las células efectoras. Las células nerviosas se han utilizado durante mucho tiempo como modelos de polarización celular y son de particular interés los mecanismos subyacentes a la localización polarizada de las moléculas sinápticas. La señalización PIP2 regulada por IMPase juega un papel integral en la polaridad sináptica.
Los fosfoinosítidos ( PIP , PIP2 y PIP3 ) son moléculas que se ha demostrado que afectan la polaridad neuronal. [23] Se identificó un gen ( ttx-7 ) en Caenorhabditis elegans que codifica la mioinositol monofosfatasa (IMPasa), una enzima que produce inositol mediante la desfosforilación del fosfato de inositol . Los organismos con genes ttx-7 mutantes demostraron defectos de comportamiento y localización, que fueron rescatados mediante la expresión de IMPase. Esto llevó a la conclusión de que la IMPasa es necesaria para la localización correcta de los componentes proteicos sinápticos. [24] [25] El gen egl-8 codifica un homólogo de la fosfolipasa C β (PLCβ), una enzima que escinde PIP2. Cuando los mutantes ttx-7 también tenían un gen egl-8 mutante , los defectos causados por el gen ttx-7 defectuoso se revirtieron en gran medida. Estos resultados sugieren que la señalización de PIP2 establece una localización polarizada de componentes sinápticos en neuronas vivas. [24]
La modulación de la liberación de neurotransmisores por los receptores acoplados a proteína G (GPCR) es un mecanismo presináptico destacado para la regulación de la transmisión sináptica . La activación de los GPCR ubicados en la terminal presináptica puede disminuir la probabilidad de liberación de neurotransmisores. Esta depresión presináptica implica la activación de proteínas G de tipo Gi/o que median diferentes mecanismos inhibidores, incluida la inhibición de los canales de calcio dependientes de voltaje , la activación de los canales de potasio y la inhibición directa del proceso de fusión de vesículas . Los endocannabinoides , sintetizados y liberados a partir de elementos neuronales postsinápticos , y sus receptores afines, incluido el receptor CB1 (GPCR) , ubicado en la terminal presináptica, participan en esta modulación mediante un proceso de señalización retrógrada , en el que estos compuestos se sintetizan y liberan. desde elementos neuronales postsinápticos y viaja de regreso a la terminal presináptica para actuar sobre el receptor CB1 para la depresión sináptica a corto o largo plazo, que causa una disminución corta o duradera en la liberación de neurotransmisores. [26]
Los fármacos se han considerado durante mucho tiempo objetivos cruciales para los canales iónicos activados por transmisores. La mayoría de los medicamentos utilizados para tratar la esquizofrenia, la ansiedad, la depresión y el insomnio actúan en las sinapsis químicas, y muchos de estos productos farmacéuticos funcionan uniéndose a canales activados por transmisores. Por ejemplo, algunas drogas como los barbitúricos y tranquilizantes se unen a los receptores GABA y mejoran el efecto inhibidor del neurotransmisor GABA. Por tanto, la concentración reducida de GABA permite la apertura de canales de Cl-.
Además, las drogas psicoactivas podrían potencialmente atacar muchos otros componentes de la maquinaria de señalización sináptica. De hecho, los portadores impulsados por Na+ liberan numerosos neurotransmisores y posteriormente se eliminan de la hendidura sináptica. Al inhibir dichos portadores, la transmisión sináptica se fortalece a medida que se prolonga la acción del transmisor. Por ejemplo, Prozac es uno de los medicamentos antidepresivos que actúa impidiendo la absorción del neurotransmisor serotonina. Además, otros antidepresivos actúan inhibiendo la reabsorción tanto de serotonina como de noradrenalina. [18]
En las terminales nerviosas, las vesículas sinápticas se producen rápidamente para compensar su rápido agotamiento durante la liberación de neurotransmisores. Su biogénesis implica segregar proteínas de la membrana de las vesículas sinápticas de otras proteínas celulares y empaquetar esas proteínas distintas en vesículas de tamaño apropiado. Además, implica la endocitosis de proteínas de la membrana de las vesículas sinápticas de la membrana plasmática. [27]
Sinaptoblástico y sinaptoclástico se refieren a actividades productoras y eliminadoras de sinapsis dentro de la cadena de señalización bioquímica. Esta terminología está asociada al Protocolo Bredesen para el tratamiento de la enfermedad de Alzheimer , que conceptualiza el Alzheimer como un desequilibrio entre estos procesos. En octubre de 2023, los estudios sobre este protocolo siguen siendo pequeños y se han obtenido pocos resultados dentro de un marco de control estandarizado.
Es ampliamente aceptado que la sinapsis juega un papel clave en la formación de la memoria . [28] La estabilidad de la memoria a largo plazo puede persistir durante muchos años; sin embargo, las sinapsis, la base neurológica de la memoria, son muy dinámicas. [29] La formación de conexiones sinápticas depende significativamente de la plasticidad sináptica dependiente de la actividad observada en diversas vías sinápticas. De hecho, la conexión entre la formación de la memoria y las alteraciones de la eficacia sináptica permite reforzar las interacciones neuronales entre neuronas. A medida que los neurotransmisores activan los receptores a través de la hendidura sináptica, la conexión entre las dos neuronas se fortalece cuando ambas neuronas están activas al mismo tiempo, como resultado de los mecanismos de señalización del receptor. Se cree que la fuerza de dos vías neuronales conectadas da como resultado el almacenamiento de información, lo que da lugar a la memoria. Este proceso de fortalecimiento sináptico se conoce como potenciación a largo plazo (LTP) . [28]
Al alterar la liberación de neurotransmisores, se puede controlar la plasticidad de las sinapsis en la célula presináptica. La célula postsináptica puede regularse alterando la función y el número de sus receptores. Los cambios en la señalización postsináptica se asocian más comúnmente con una LTP dependiente del receptor del ácido N-metil-d-aspártico (NMDAR) y la depresión a largo plazo (LTD) debido a la entrada de calcio en la célula postsináptica, que son las más comunes. analizaron formas de plasticidad en las sinapsis excitadoras. [30]
Además, la proteína quinasa II dependiente de Ca2+/calmodulina (CaM) (CaMKII) es mejor reconocida por sus funciones en el cerebro, particularmente en las regiones del neocórtex y el hipocampo, porque sirve como mediador ubicuo de las señales celulares de Ca2+. CaMKII es abundante en el sistema nervioso y se concentra principalmente en las sinapsis de las células nerviosas. De hecho, CaMKII ha sido identificado definitivamente como un regulador clave de procesos cognitivos, como el aprendizaje y la plasticidad neuronal. Se demostró la primera evidencia experimental concreta de la función asumida durante mucho tiempo de CaMKII en el almacenamiento de la memoria.
Si bien la unión de Ca2+/CaM estimula la actividad de CaMKII, la actividad de CaMKII autónoma independiente de Ca2+ también puede producirse mediante otros procesos. CaMKII se vuelve activo autofosforilándose tras la unión de Ca2+/calmodulina. CaMKII todavía está activo y se fosforila incluso después de que se escinde el Ca2+; como resultado, el cerebro almacena recuerdos a largo plazo mediante este mecanismo. Sin embargo, cuando la enzima CaMKII es desfosforilada por una enzima fosfatasa, se vuelve inactiva y se pierden los recuerdos. Por tanto, CaMKII desempeña un papel vital tanto en la inducción como en el mantenimiento de la LTP. [31]
Por razones técnicas, la estructura y función sinápticas se han estudiado históricamente en modelos de sinapsis inusualmente grandes, por ejemplo:
Las sinapsis funcionan como conjuntos dentro de redes cerebrales particulares para controlar la cantidad de actividad neuronal, que es esencial para la memoria, el aprendizaje y el comportamiento. En consecuencia, las alteraciones sinápticas pueden tener efectos negativos. De hecho, las alteraciones en los sistemas moleculares intrínsecos de las células o las modificaciones de los procesos bioquímicos ambientales pueden provocar una disfunción sináptica. La sinapsis es la unidad principal de transferencia de información en el sistema nervioso, y la creación correcta de contactos sinápticos durante el desarrollo es esencial para el funcionamiento normal del cerebro. Además, varias mutaciones se han relacionado con trastornos del desarrollo neurológico, y esa función comprometida en diferentes ubicaciones de sinapsis es un sello distintivo de las enfermedades neurodegenerativas.
Los defectos sinápticos están causalmente asociados con enfermedades neurológicas de aparición temprana, incluidos los trastornos del espectro autista (TEA), la esquizofrenia (SCZ) y el trastorno bipolar (BP). Por otro lado, en patologías degenerativas de aparición tardía, como las enfermedades de Alzheimer (EA), Parkinson (EP) y Huntington (HD), se cree que la sinaptopatía es el resultado final inevitable de una cascada fisiopatológica en curso. Estas enfermedades se identifican por una pérdida gradual de la función cognitiva y conductual y una pérdida constante de tejido cerebral. Además, estos deterioros se han relacionado principalmente con la acumulación gradual de agregados proteicos en las neuronas, cuya composición puede variar según la patología; todos tienen los mismos efectos nocivos sobre la integridad neuronal. Además, el elevado número de mutaciones relacionadas con la estructura y función sináptica, así como con alteraciones de la columna dendrítica en el tejido post-mortem, ha llevado a la asociación entre defectos sinápticos y trastornos del neurodesarrollo, como el TEA y la SCZ, caracterizados por anomalías conductuales o cognitivas. fenotipos.
Sin embargo, debido al acceso limitado al tejido humano en las últimas etapas y a la falta de una evaluación exhaustiva de los componentes esenciales de las enfermedades humanas en los modelos animales experimentales disponibles, ha sido difícil comprender plenamente el origen y el papel de la disfunción sináptica en los trastornos neurológicos. [33]
La palabra sinapsis apareció por primera vez en 1897, en la séptima edición del
Libro de texto de fisiología
de Michael Foster .