El ácido acetoacético ( nombre IUPAC : ácido 3-oxobutanoico , también conocido como ácido acetoncarboxílico o ácido diacético ) es el compuesto orgánico con la fórmula CH 3 COCH 2 COOH. Es el beta- cetoácido más simple y, como otros miembros de esta clase, es inestable. Los ésteres metílicos y etílicos, que son bastante estables, se producen industrialmente a gran escala como precursores de colorantes. El ácido acetoacético es un ácido débil . [3]
En condiciones fisiológicas típicas, el ácido acetoacético existe como su base conjugada , acetoacetato :
El acetoacetato libre es producido principalmente por las mitocondrias hepáticas a partir de su tioéster con coenzima A (CoA):
El propio acetoacetato-CoA se forma por tres rutas:
En los mamíferos, el acetoacetato producido en el hígado (junto con los otros dos " cuerpos cetónicos ") se libera al torrente sanguíneo como fuente de energía durante los periodos de ayuno , ejercicio o como consecuencia de la diabetes mellitus tipo 1 . [5] Primero, se le transfiere enzimáticamente un grupo CoA desde succinil CoA , convirtiéndolo nuevamente en acetoacetil CoA; Luego, la tiolasa lo rompe en dos moléculas de acetil CoA, que luego ingresan al ciclo del ácido cítrico . El músculo cardíaco y la corteza renal prefieren el acetoacetato a la glucosa. El cerebro utiliza acetoacetato cuando los niveles de glucosa son bajos debido al ayuno o la diabetes. [4] : 394
El ácido acetoacético se puede preparar mediante hidrólisis de diceteno . Sus ésteres se producen de manera análoga mediante reacciones entre diceteno y alcoholes, [3] y el ácido acetoacético se puede preparar mediante la hidrólisis de estas especies. [6] En general, el ácido acetoacético se genera a 0 °C y se utiliza in situ inmediatamente. [7]
Se descompone a una velocidad de reacción moderada en acetona y dióxido de carbono :
La forma ácida tiene una vida media de 140 minutos a 37 °C en agua, mientras que la forma básica (el anión) tiene una vida media de 130 horas. Es decir, reacciona unas 55 veces más lentamente. [8] La correspondiente descarboxilación del trifluoroacetoacetato se utiliza para preparar trifluoroacetona :
Es un ácido débil (como la mayoría de los ácidos alquilcarboxílicos), con un p K a de 3,58.
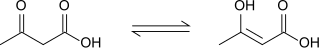
El ácido acetoacético muestra tautomerización ceto-enólica , estabilizándose parcialmente la forma enólica mediante conjugación extendida y enlaces H intramoleculares . El equilibrio depende en gran medida del disolvente; con la forma ceto dominando en solventes polares (98% en agua) y la forma enol representando 25-49% del material en solventes no polares. [9]

Los ésteres acetoacéticos se utilizan para la reacción de acetoacetilación , que se utiliza ampliamente en la producción de amarillos de arilida y tintes de diarilida . [3] Aunque los ésteres se pueden utilizar en esta reacción, la dicetena también reacciona con alcoholes y aminas para formar los correspondientes derivados del ácido acetoacético en un proceso llamado acetoacetilación . Un ejemplo es la reacción con 4-amino indano : [10]
El ácido acetoacético se mide en la orina de personas con diabetes para detectar cetoacidosis [11] y para controlar a las personas que siguen una dieta cetogénica o baja en carbohidratos . [12] [13] Esto se hace usando varillas reactivas recubiertas con nitroprusiato o reactivos similares. El nitroprusiato cambia de rosa a morado en presencia de acetoacetato, la base conjugada del ácido acetoacético, y el cambio de color se clasifica a simple vista. La prueba no mide el β-hidroxibutirato, la cetona más abundante en el cuerpo; durante el tratamiento de la cetoacidosis, el β-hidroxibutirato se convierte en acetoacetato, por lo que la prueba no es útil una vez iniciado el tratamiento [11] y puede ser falsamente baja en el momento del diagnóstico. [14]
Se utilizan pruebas similares en vacas lecheras para detectar cetosis . [15]