La tipificación de tejidos es un procedimiento en el que se analiza la compatibilidad de los tejidos de un posible donante y un posible receptor antes del trasplante . La incompatibilidad de los tejidos del donante y del receptor puede provocar el rechazo de los tejidos. Existen varios métodos de tipificación de tejidos.

Durante la tipificación de tejidos, se identifican los antígenos leucocitarios humanos (HLA) de un individuo . [1] Las moléculas de HLA se presentan en la superficie de las células y facilitan las interacciones entre las células inmunes (como las células dendríticas y las células T ) que conducen a respuestas inmunes adaptativas . [2] Si el sistema inmunológico del receptor reconoce el HLA del donante como diferente del HLA del propio receptor, se puede desencadenar una respuesta inmune contra los tejidos del donante. [3] Más específicamente, los desajustes de HLA entre donantes y receptores de órganos pueden conducir al desarrollo de anticuerpos específicos del donante anti-HLA (DSA). [4] Los DSA están fuertemente asociados con el rechazo de tejidos del donante en el receptor, y su presencia se considera un indicador de rechazo mediado por anticuerpos. [5] Cuando el HLA del donante y el receptor son compatibles, los tejidos del donante tienen significativamente más probabilidades de ser aceptados por el sistema inmunológico del receptor. [3] Durante la tipificación de tejidos, se deben tipificar varios genes HLA tanto en el donante como en el receptor, incluidos los genes HLA de clase I A , B y C , así como los genes HLA de clase II DRB1 , DRB3 , DRB4 , DRB5 , DQA1 , DQB1 , DPA1 y DPB1 . [6] La tipificación de HLA se hace más difícil por el hecho de que la región HLA es la región genéticamente más variable en el genoma humano. [7]
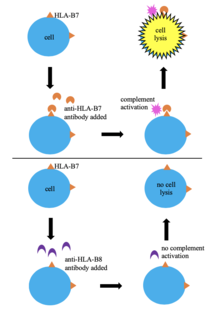
Uno de los primeros métodos de tipificación de tejidos fue la tipificación serológica. En esta técnica, las células sanguíneas de un donante se tipifican en función del HLA mezclándolas con suero que contiene anticuerpos anti-HLA . Si los anticuerpos reconocen su epítopo en el HLA del donante, se produce la activación del complemento que conduce a la lisis y muerte celular , lo que permite que las células absorban un colorante ( azul tripán ). Esto permite la identificación del HLA de las células basándose indirectamente en la especificidad de los anticuerpos conocidos en el suero. Este método se ha utilizado ampliamente porque es simple, rápido y de bajo costo; sin embargo, la enorme variabilidad en los alelos HLA significa que el suero que contiene anticuerpos específicos para el HLA de las células que se están probando puede no estar disponible. [6] [3] La tipificación serológica no proporciona una imagen clara de la región HLA y no siempre da como resultado una tipificación HLA exitosa, por lo que muchos laboratorios han dejado de usarlo en favor de métodos más efectivos. [6] [8]
Recientemente, han surgido otros enfoques más eficaces, incluido el uso de la reacción en cadena de la polimerasa ( PCR ) basada en cebadores específicos de secuencia ( SSP ) o sondas de oligonucleótidos específicos de secuencia ( SSOP ). [3 ] [6 ] Sin embargo, la SSP-PCR puede consumir tiempo y recursos. [8] La SSOP-PCR es mejor para la tipificación de HLA de un gran número de individuos, por ejemplo, un gran número de donantes para registros de médula ósea. [8] La RT-PCR es otro enfoque para la tipificación de HLA que es rápido y versátil, pero es costoso. [6]
El análisis conformacional mediado por la cadena de referencia (RSCA) es otro método utilizado para la tipificación de HLA. En este método, una muestra de HLA desconocida se mezcla con un alelo de referencia y se procesa en un gel mediante electroforesis . [8] El RSCA está limitado por la cantidad de alelos de referencia de HLA disponibles, ya que la región de HLA es muy diversa. [8]
Actualmente, la secuenciación directa de ADN se considera el mejor método de tipificación de HLA, ya sea mediante secuenciación de Sanger o secuenciación de próxima generación , aunque también puede llevar mucho tiempo y es uno de los métodos más costosos. [6] [8] También se puede utilizar la secuenciación de ARN , pero muchos laboratorios no lo hacen porque el ARN es inestable y propenso a degradarse. [8]