La lactama Ojima es un compuesto orgánico de cierta importancia en la producción comercial de Taxol . Esta lactama fue sintetizada por primera vez por Iwao Ojima . [1] La síntesis orgánica es una ilustración de la síntesis asimétrica mediante un auxiliar quiral .
La reacción se centra en una cicloadición de enolato de imina y litio . Para garantizar la estereoquímica correcta (el grupo fenilo y el éter sililo deben adoptar una configuración cis ) en la β-lactama se utiliza un auxiliar quiral en la síntesis de enolato. La síntesis de enolato parte del ácido glicólico . El grupo hidroxilo está protegido por un grupo bencilo y el ácido carboxílico se activa mediante reacción con cloruro de tionilo para formar cloruro de ácido . El cloruro de ácido reacciona con el auxiliar quiral trans-2-fenil-1-ciclohexanol . Luego se elimina el grupo bencilo y se reemplaza por un éter sililico TES mediante reacción con cloruro de trietilsililo. La reacción con fenillitio produce el enolato .

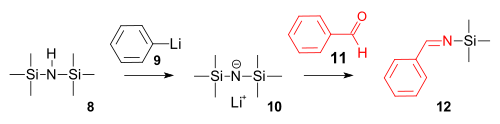
La síntesis de imina es una reacción de hexametildisilazano con fenillitio para formar una base amida fuerte seguida de una reacción de condensación con benzaldehído .
Tanto el intermedio imina como el enol se unen en una reacción de cicloadición seguida de una sustitución acilo nucleofílica intramolecular de la amina con expulsión del auxiliar quiral de la cis - lactama . El grupo trietilsililo se elimina mediante fluoruro de hidrógeno y el grupo benzoilo se añade en una reacción de Schotten-Baumann .
