El nitrosobenceno es un compuesto orgánico con la fórmula C6H5NO . Es uno de los compuestos nitrosos orgánicos prototípicos . Característico de su grupo funcional, es una especie de color verde oscuro que existe en equilibrio con su dímero de color amarillo pálido . Tanto el monómero como el dímero son diamagnéticos .
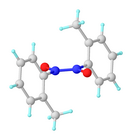
El nitrosobenceno y otros nitrosoarenos suelen participar en un equilibrio monómero-dímero. Los dímeros suelen ser los preferidos en estado sólido, mientras que los monómeros de colores intensos son los preferidos en solución diluida o a temperaturas más altas. Los dímeros pueden formularse como Ar(O − )N + =N + (O − )Ar. Existen como isómeros cis y trans debido a la presencia del doble enlace N–N. Los dímeros a veces se denominan azobencenodióxidos. La isomerización cis-trans se produce a través de la intermediación del monómero. [1]
En el caso del propio nitrosobenceno, la forma monomérica metaestable podría prepararse por sublimación sobre un dedo frío . El material monomérico se sublima selectivamente debido a su menor peso molecular y se recoge en un dedo frío como cristales brillantes de color verde oscuro. Con el tiempo, el material monomérico se dimeriza para dar el dióxido de azobenceno original como un sólido de color amarillo pálido. Como dicta el principio de Le Chatelier , el nitrosobenceno existe en la fase de solución como una mezcla de monómero y dímero en equilibrio dinámico cuya composición depende de la temperatura (el monómero se favorece a mayor temperatura) y la concentración (el monómero se favorece a baja concentración), así como de la identidad del medio (fase gaseosa o disolvente). [2]
El nitrosobenceno fue preparado por primera vez por Adolf von Baeyer mediante la reacción de difenilmercurio y bromuro de nitrosilo : [4]
Una síntesis moderna implica la reducción del nitrobenceno a fenilhidroxilamina (C 6 H 5 NHOH) que luego se oxida con dicromato de sodio (Na 2 Cr 2 O 7 ). [5]
El nitrosobenceno también se puede preparar por oxidación de anilina usando ácido peroximonosulfúrico (ácido de Caro) [6] o peroximonosulfato de potasio en condiciones bifásicas. [7] Generalmente se purifica por sublimación o por destilación al vapor, donde aparece como un líquido verde que se solidifica en un sólido incoloro.
El nitrosobenceno sufre reacciones de Diels-Alder con dienos. [8] La condensación con anilinas produce derivados de azobenceno en una reacción conocida como reacción de Mills o reacción de Baeyer-Mills . [9] La reducción del nitrosobenceno produce anilina .
Lo más característico es que el nitrosobenceno se condensa con grupos metileno activos, como los de los ésteres malónicos y el fenilacetonitrilo . El fenilacetonitrilo (PhCH2CN ) da la imina (PhC(CN)=NPh) en una reacción conocida como reacción de Ehrlich-Sachs : [10]
A veces, la condensación con compuestos de metileno activos da productos de la reacción O -nitroso-aldólica: [11]
{{cite journal}}: CS1 maint: varios nombres: lista de autores ( enlace )