Hay tres conjuntos de haluros de indio , los trihaluros, los monohaluros y varios haluros intermedios . En los monohaluros, el estado de oxidación del indio es +1 y sus nombres propios son fluoruro de indio (I), cloruro de indio (I), bromuro de indio (I) y yoduro de indio (I).
Los haluros intermedios contienen indio con estados de oxidación +1, +2 y +3.
En todos los trihaluros, el estado de oxidación del indio es +3 y sus nombres propios son fluoruro de indio (III), cloruro de indio (III), bromuro de indio (III) y yoduro de indio (III). Los trihaluros son ácidos de Lewis . El tricloruro de indio es un punto de partida en la producción de trimetilindio que se utiliza en la industria de los semiconductores.
InF 3 es un sólido blanco , pf 1170 °C. Su estructura contiene 6 coordenadas de indio.
InCl 3 es un sólido blanco, pf 586 °C. Se obtiene por oxidación del indio con cloro. [1] Es isoestructural con AlCl 3 .
InBr 3 es un sólido amarillo pálido, pf 435 °C. Es isoestructural con AlCl 3 . Se prepara combinando los elementos. [2] InBr 3 encuentra algún uso en la síntesis orgánica como ácido de Lewis tolerante al agua. [3]
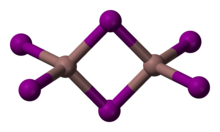
InI 3 es un sólido amarillo. Se obtiene por evaporación de una solución de indio en HI. [4] Se conocen formas distintas de color amarillo y rojo. La forma roja sufre una transición al amarillo a 57 °C. La estructura de la forma roja no ha sido determinada mediante cristalografía de rayos X , sin embargo, la evidencia espectroscópica indica que el indio puede tener seis coordenadas. [5] La forma amarilla consta de In 2 I 6 con 4 centros coordinados de indio. Se utiliza como "captador de yoduro" en el proceso de Cativa . [ cita necesaria ]
Se conoce un número sorprendente de cloruros y bromuros intermedios, pero sólo un yoduro y ningún difluoruro. En lugar del aparente estado de oxidación de +2, estos compuestos contienen indio en los estados de oxidación +1 y +3. Así, el diyoduro se describe como In I In III X 4 . Fue algún tiempo después que se conoció la existencia de compuestos que contenían el anión In 2 Br2-6Se confirmó que contiene un enlace indio-indio. Los primeros trabajos sobre los cloruros y bromuros implicaron investigaciones de los diagramas de fases binarias de los trihaluros y el monohaluro relacionado. Muchos de los compuestos fueron inicialmente identificados erróneamente ya que muchos de ellos son incongruentes y se descomponen antes de fundirse. La existencia y las estructuras de la mayoría de los cloruros y bromuros informados anteriormente ahora han sido confirmadas mediante estudios de difracción de rayos X o han sido relegados a la historia. Quizás el caso más inesperado de identidad errónea fue el sorprendente resultado de que una cuidadosa reinvestigación del diagrama de fases binario InCl/InCl 3 no encontró InCl 2 . [6]
La razón de esta abundancia de compuestos es que el indio forma 4 y 6 aniones coordinados que contienen indio (III), por ejemplo, InBr.−4, InCl3-6así como el anión In 2 Br2-6que sorprendentemente contiene un enlace indio-indio.
In 7 Cl 9 es un sólido amarillo estable hasta 250 °C que se formula en I 6 (In III Cl 6 )Cl 3 [7]
In 7 Br 9 tiene una estructura similar a In 7 Cl 9 y puede formularse como In I 6 (In III Br 6 ) Br 3 [8]
En 5 Br 7 es un sólido de color amarillo pálido. Está formulado en I 3 (En II 2 Br 6 )Br. El anión In II 2 Br 6 tiene una estructura similar al etano eclipsada con una longitud de enlace metal-metal de 270 pm. [9]
In 2 Cl 3 es incoloro y está formulado en I 3 In III Cl 6 [10] Por el contrario, In 2 Br 3 contiene el anión In 2 Br 6 presente en In 5 Br 7 , y está formulado en I 2 (In II 2 Br 6 ) con una estructura similar a Ga 2 Br 3 . [11]
En 4 Br 7 es casi incoloro con un tinte amarillo verdoso pálido. Es sensible a la luz (como TlCl y TlBr) y se descompone en InBr 2 e In metal. Es una sal mixta que contiene InBr.−4y InBr3-6aniones equilibrados por cationes In + . Está formulado en I 5 (En III Br 4 ) 2 (En III Br 6 ) Las razones de la red distorsionada se han atribuido a una combinación antienlazante entre orbitales 5s de indio no direccionales, doblemente llenos y orbitales híbridos 4p de bromo vecinos. [12]
In 5 Cl 9 se formula como In I 3 In III 2 Cl 9 . El En 2 Cl3-9El anión tiene dos átomos de indio de 6 coordenadas con 3 átomos de cloro puente, bioctaedros que comparten caras, con una estructura similar al Cr 2 Cl.2-9y Tl2Cl2-9. [13]
InBr 2 es un sólido cristalino de color blanco verdoso, que se formula en I In III Br 4 . Tiene la misma estructura que GaCl 2 . El InBr 2 es soluble en disolventes aromáticos y se han identificado algunos compuestos que contienen complejos de η 6 -areno In(I). (Ver hapticidad para una explicación del enlace en tales complejos de iones metálicos areno). Con algunos ligandos, InBr 2 forma complejos neutros que contienen un enlace indio-indio. [14]
InI 2 es un sólido amarillo que se formula en I In III I 4 .
Los monohaluros sólidos InCl, InBr e InI son todos inestables con respecto al agua y se descomponen en especies de metal e indio (III). Se encuentran entre los compuestos de galio (I), que son más reactivos, y el talio (I), que son estables con respecto al agua. InI es el más estable. Hasta hace relativamente poco tiempo, los monohaluros habían sido curiosidades científicas; sin embargo, con el descubrimiento de que pueden usarse para preparar compuestos de cadena y racimos de indio, ahora están atrayendo mucho más interés. [15]
El InF sólo se conoce como un compuesto gaseoso inestable.
La forma de InCl a temperatura ambiente es amarilla, con una estructura cúbica de NaCl distorsionada. La forma roja de alta temperatura (>390 K) tiene la estructura. [15]
InBr es un sólido cristalino rojo, pf 285 °C. Tiene la misma estructura que , con una estructura de sal gema ortorrómbica distorsionada. Puede prepararse a partir de indio metálico e InBr 3 .
InI es un sólido cristalino de color rojo púrpura intenso. Tiene la misma estructura que . Puede fabricarse mediante combinación directa de sus elementos constituyentes a alta temperatura. Alternativamente, se puede preparar a partir de InI 3 e indio metálico en xilenos a reflujo. [16] Es el más estable de los monohaluros sólidos y es soluble en algunos disolventes orgánicos. Las soluciones de InI en una mezcla de piridina/m-xileno son estables por debajo de 243 K. [15]
Los trihaluros son ácidos de Lewis y forman compuestos de adición con ligandos. Para InF 3 se conocen pocos ejemplos, sin embargo, para otros haluros se conocen compuestos de adición con geometrías de coordinación tetraédrica, trigonal, bipiramidal y octaédrica. Con iones haluro hay ejemplos de todas estas geometrías junto con algunos aniones con indio coordinado octaédricamente y con átomos de halógeno puente, En 2 X3-9con tres átomos de halógeno puente y en 2 X−7con solo uno. Además, hay ejemplos de indio con geometría plana cuadrada en el ion InX 5 2− . La geometría plana cuadrada de InCl2-5fue el primero encontrado para un elemento del grupo principal.
Sales de InCl−4, InBr−4y en yo−4son conocidos. Se ha preparado la sal LiInF 4 , [17] [18] , sin embargo, tiene una estructura de capas inusual con un centro de indio coordinado octaédricamente. Sales de InF 6 3− , InCl3-6y InBr3-6 [19] se han realizado todos.
El InCl2-5Se ha descubierto que el ion es piramidal cuadrado en la sal (NEt4) 2 InCl 5 , con la misma estructura que (NEt 4 ) 2 TlCl 5 , pero es bipiramidal trigonal en el solvato de acetonitrilo de pentacloroindato de tetrafenilfosfonio. [20]
El InBr2-5De manera similar, se ha encontrado un ion piramidal cuadrado, aunque distorsionado, en la sal de Bis(4-cloropiridinio) [21] y bipiramidal trigonal [22] en Bi 37 InBr 48 .
El En 2 X−7Los iones contienen un único átomo de halógeno puente. A partir de los espectros no se puede determinar si el puente está curvado o es lineal. El cloruro y el bromuro se han detectado mediante espectrometría de masas por electropulverización. El en 2 yo−7El ion se ha preparado en la sal CsIn 2 I 7 . [5]
Las sales de cesio de In 2 Cl.3-9y en 2 hab.3-9ambos contienen aniones binucleares con átomos de indio coordinados octaédricamente. [13]
In I X 2 − se produce cuando el ion In 2 X 6 2− se desproporciona . Sales que contienen el In I X2-3Se han fabricado iones y se ha interpretado que sus espectros vibratorios muestran que tienen simetría C 3v , geometría piramidal trigonal , con estructuras similares al isoelectrónico Sn X.−3iones.
Se han preparado sales de los iones cloruro, bromuro y yoduro (Bu 4 N) 2 En 2 X 6 . En disolventes no acuosos este ion se desproporciona para dar In I X−2y en III X−4.
Tras el descubrimiento del In 2 Br 6 2−, se han formado varios compuestos neutros relacionados que contienen el núcleo In II 2 X 4 a partir de la reacción de dihaluros de indio con ligandos neutros. [14] Algunos químicos se refieren a estos aductos, cuando se utilizan como punto de partida para la síntesis de compuestos agrupados, como 'En 2 X 4 ', por ejemplo, el aducto TMEDA . [23]