En química , el efecto mesomérico (o efecto de resonancia ) es una propiedad de los sustituyentes o grupos funcionales en un compuesto químico . Se define como la polaridad producida en la molécula por la interacción de dos enlaces pi o entre un enlace pi y un par solitario de electrones presentes en un átomo adyacente. [1] Este cambio en la disposición de los electrones da como resultado la formación de estructuras de resonancia que se hibridan en la estructura verdadera de la molécula. Los electrones pi luego se alejan o se acercan a un grupo sustituyente particular. El efecto mesomérico es más fuerte en compuestos con un potencial de ionización más bajo . Esto se debe a que los estados de transferencia de electrones tendrán energías más bajas.
El efecto se utiliza de forma cualitativa y describe las propiedades de extracción o liberación de electrones de los sustituyentes en función de las estructuras de resonancia pertinentes y se simboliza con la letra M. [2] El efecto mesomérico es negativo ( –M ) cuando el sustituyente es un grupo aceptor de electrones , y el efecto es positivo ( +M ) cuando el sustituyente es un grupo donador de electrones . A continuación se presentan dos ejemplos del efecto +M y –M . Además, a continuación se indican los grupos funcionales que contribuyen a cada tipo de resonancia.
El efecto +M, también conocido como efecto mesomérico positivo, ocurre cuando el sustituyente es un grupo donador de electrones. El grupo debe tener una de dos cosas: un par solitario de electrones o una carga negativa. En el efecto +M, los electrones pi se transfieren del grupo hacia el sistema conjugado, lo que aumenta la densidad del sistema. Debido al aumento de la densidad electrónica, el sistema conjugado desarrollará una carga más negativa. Como resultado, el sistema bajo el efecto +M será más reactivo hacia los electrófilos , que pueden quitarle la carga negativa, que un nucleófilo . [ cita requerida ]

Orden de efecto +M: [1]
El efecto -M, también conocido como efecto mesomérico negativo, ocurre cuando el sustituyente es un grupo atractor de electrones. Para que ocurra un efecto mesomérico negativo (-M), el grupo debe tener una carga positiva o un orbital vacío para atraer electrones hacia él. En el efecto -M, los electrones pi se alejan del sistema conjugado y se acercan al grupo atractor de electrones. En el sistema conjugado, la densidad de electrones disminuye y la carga total se vuelve más positiva. Con el efecto -M, los grupos y compuestos se vuelven menos reactivos hacia los electrófilos y más reactivos hacia los nucleófilos, que pueden ceder electrones y equilibrar la carga positiva. [3]
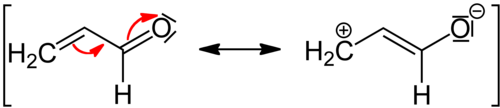
-Orden de efecto M:
El flujo neto de electrones desde o hacia el sustituyente también está determinado por el efecto inductivo . [3] El efecto mesomérico como resultado de la superposición de orbitales p (resonancia) no tiene absolutamente ningún efecto sobre este efecto inductivo, ya que el efecto inductivo tiene que ver puramente con la electronegatividad de los átomos y su topología en la molécula (qué átomos están conectados a cuáles). Específicamente, el efecto inductivo es la tendencia de los sustituyentes a repeler o atraer electrones basándose puramente en la electronegatividad y no en la reestructuración. El efecto mesomérico, sin embargo, se ocupa de la reestructuración y ocurre cuando el par de electrones de los sustituyentes se desplaza. El efecto inductivo solo actúa sobre los carbonos alfa, mientras que el mesomérico utiliza enlaces pi entre átomos. [4] Si bien estos dos caminos a menudo conducen a moléculas y estructuras de resonancia similares, el mecanismo es diferente. Como tal, el efecto mesomérico es más fuerte que el efecto inductivo. [5]
Los conceptos de efecto mesomérico, mesomerismo y mesómero fueron introducidos por Ingold en 1938 como una alternativa al concepto sinónimo de resonancia de Pauling . [6] "Mesomerismo" en este contexto se encuentra a menudo en la literatura alemana y francesa, pero en la literatura inglesa domina el término "resonancia".
El efecto mesomérico se puede transmitir a lo largo de cualquier número de átomos de carbono en un sistema conjugado . Esto explica la estabilización por resonancia de la molécula debido a la deslocalización de la carga. [7] Es importante señalar que la energía de la estructura real de la molécula, es decir, el híbrido de resonancia, puede ser menor que la de cualquiera de las estructuras canónicas contribuyentes. La diferencia de energía entre la estructura inductiva real y la peor estructura cinética (estructuras contribuyentes más estables) se denomina energía de resonancia o energía de estabilización por resonancia. [8] Para la estimación cuantitativa de la fuerza del efecto mesomérico/resonancia se utilizan varias constantes sustituyentes, es decir, la constante de resonancia de Swain-Lupton, la constante de resonancia de Taft o el parámetro pEDA de Oziminski y Dobrowolski .
Además, las estructuras de resonancia resultantes pueden otorgar a la molécula propiedades que no son evidentes de manera inherente al observar una sola estructura. Algunas de estas propiedades incluyen diferentes reactividades, apantallamiento diamagnético local en aromáticos, desprotección y resistencias ácidas y básicas. [9]
{{cite book}}: |website=ignorado ( ayuda )