
Los canales iónicos sintéticos son compuestos químicos de novo que se insertan en las bicapas lipídicas , forman poros y permiten que los iones fluyan de un lado al otro. [1] Son análogos artificiales de los canales iónicos naturales y, por lo tanto, también se conocen como canales iónicos artificiales . En comparación con los canales biológicos, suelen permitir flujos de magnitud similar, pero son
Los canales sintéticos, al igual que los canales naturales, suelen caracterizarse por una combinación de técnicas de moléculas individuales (por ejemplo, fijación de voltaje de bicapas planas [1] ) y técnicas de conjunto (flujo en vesículas [6] ). El estudio de los canales iónicos sintéticos puede conducir potencialmente a nuevas tecnologías de detección de moléculas individuales, así como a nuevas terapias.

Si bien los canales iónicos semisintéticos, a menudo basados en canales peptídicos modificados como la gramicidina , se habían preparado desde la década de 1970, el primer intento de preparar un canal iónico sintético se realizó en 1982 utilizando una β- ciclodextrina sustituida . [7]
Esta molécula, inspirada en la gramicidina, fue diseñada para ser una entidad con forma de barril que abarca una sola lámina de una membrana bicapa y se vuelve "activa" solo cuando dos moléculas en láminas opuestas se unen de extremo a extremo. Si bien el compuesto induce flujos de iones en vesículas, los datos no muestran de manera inequívoca la formación de canales (a diferencia de otros mecanismos de transporte; consulte Mecanismo).
El transporte de Na + por dichos canales fue informado por primera vez por dos grupos de investigadores en 1989-1990. [8] [9] [10]
Con la adopción de la técnica de fijación de voltaje para la investigación de canales sintéticos a principios de la década de 1990, los investigadores pudieron observar actividades eléctricas cuantificadas de moléculas sintéticas, a menudo consideradas la evidencia característica de los canales iónicos. [1] Esto condujo a un aumento sostenido de la actividad de investigación durante las siguientes dos décadas. En 2009, se publicaron más de 25 artículos revisados por pares sobre el tema, [11] y hay una serie de revisiones exhaustivas disponibles. [3] [4] [5]

El transporte pasivo de iones a través de una membrana puede tener lugar por tres mecanismos principales: por transporte, a través de defectos en una membrana rota, o a través de una trayectoria definida; estos corresponden a los transportadores de ionóforos , detergentes y canales iónicos . Si bien la investigación de canales iónicos sintéticos intenta preparar compuestos que muestren conductancia a través de una ruta definida, la elucidación del mecanismo es difícil y rara vez inequívoca. Los dos métodos principales de caracterización tienen sus desventajas y, como consecuencia, a menudo se define la función pero se presume el mecanismo.

Una línea de evidencia del transporte de iones proviene del examen macroscópico de conjuntos estadísticos . Todas estas técnicas utilizan vesículas intactas con un volumen atrapado, con actividades de canales iónicos informadas por diferentes métodos espectroscópicos . [6]
En un caso típico, un colorante queda atrapado dentro de la población de vesículas. Este colorante se selecciona para que responda colorimétrica o fluorométricamente a la presencia de un ion; este ion normalmente está ausente del interior de la vesícula pero presente en el exterior. Sin un transportador de iones, la bicapa lipídica actúa como una barrera cinética para bloquear el flujo de iones y el colorante permanece "oscuro" indefinidamente.
Como un transportador de iones permite que los iones del exterior se difundan hacia el interior, su adición afectará la propiedad de color/fluorescencia del tinte. Al monitorear macroscópicamente las propiedades del tinte a lo largo del tiempo y controlar los factores externos, se puede medir la capacidad de un compuesto para actuar como transportador de iones.
Sin embargo, la observación del transporte de iones no permite determinar con precisión el canal iónico como mecanismo. Cualquier clase de transportador puede conducir a la misma observación, y normalmente se requiere evidencia adicional que lo corrobore. Durante las últimas dos décadas se han desarrollado experimentos sofisticados destinados a investigar la selectividad, la activación de compuertas y otros parámetros del canal, que se han resumido recientemente. [6]

Una alternativa al método basado en conjuntos descrito anteriormente es el experimento de fijación de voltaje. [16] En un experimento de fijación de voltaje , dos compartimentos de electrolito se dividen por una abertura, generalmente entre 5 y 250 micrómetros de diámetro. Se pinta una bicapa lipídica a través de esta abertura, separando así eléctricamente los compartimentos; la naturaleza molecular se puede determinar midiendo su capacitancia .
Al añadir un canal iónico (ideal), se forma una ruta definida entre los dos compartimentos. A través de este poro, los iones fluyen rápidamente a través del gradiente de potencial y electroquímico (>106 / segundo), y el flujo máximo está limitado por la geometría y las dimensiones del poro. En algún momento posterior, el poro puede cerrarse o colapsar, con lo que la corriente vuelve a cero. Esta corriente de estado abierto, que se origina y se amplifica a partir de un evento de una sola molécula, es típicamente del orden de pA a nA , con una resolución temporal de aproximadamente milisegundos. Los eventos ideales o cercanos a los ideales se denominan " tapas cuadradas " en la literatura y se han considerado como una firma para un mecanismo basado en canales.
Cabe destacar que los eventos observados a esta escala son verdaderamente estocásticos , es decir, son el resultado de colisiones moleculares aleatorias y cambios de conformación. Como el área de la membrana es mucho mayor que la de un poro, múltiples copias pueden abrirse y cerrarse independientemente unas de otras, lo que da lugar a la apariencia de escalera (Panel C en la figura); estos eventos ideales a menudo se modelan como procesos de Markov .
Utilizando la notación de cuadrícula de actividad , [17] se han revisado críticamente los canales iónicos sintéticos estudiados con el método de fijación de voltaje durante el período 1982-2010. [18] Si bien los rastros ideales son los más frecuentemente analizados e informados en la literatura, muchos registros son decididamente no ideales, y se demostró que un subconjunto es fractal. [19] El desarrollo de métodos para analizar estos rastros no ideales y aclarar su relación con el mecanismo de transporte es un área de investigación contemporánea.
Se ha informado de que un conjunto amplio y diverso de moléculas sintéticas actúan como transportadores de iones en las membranas lipídicas. Aquí se describe una selección para demostrar la amplitud de las estructuras factibles y las funciones alcanzables . Se encuentran disponibles revisiones exhaustivas de la literatura hasta 2010 en una serie tripartita. [3] [4] [5]
La mayoría de los canales sintéticos (pero no todos; ver canales minimalistas) tienen estructuras químicas sustancialmente más grandes que las moléculas pequeñas típicas (pesos moleculares de ~1-5 kDa). Esto se origina en la necesidad de ser anfifílicos , es decir, tener porciones hidrofóbicas suficientes para permitir la partición en bicapa lipídica, así como "grupos de cabeza" polares o cargados para afirmar una orientación y geometría definidas con respecto a la membrana.


Se han descrito canales iónicos que contienen calixarenos de tamaño de anillo 3 y 4. Para el calix[4]areno, hay dos conformaciones accesibles y se han desarrollado ejemplos de conformación 1,3-alt y cono .


El primer canal iónico sintético se construyó mediante sustitución parcial en el borde primario de la β- ciclodextrina . [7] Desde entonces se han descrito otras β-ciclodextrinas sustituidas, incluidas las ciclodextrinas modificadas con tiol, [20] un canal de oligobutileno selectivo para aniones, [21] y varios oligómeros de estallido estelar unidos con óxido de polietileno. [22] Recientemente se han descrito las relaciones estructura-actividad de un amplio conjunto de "medios canales" de ciclodextrina preparados mediante química de "clic" . [17]

Se sabe que los macrociclos de péptidos D/L alternados se autoagregan en nanotubos, y se ha demostrado que los nanotubos resultantes actúan como canales iónicos en las membranas lipídicas. [23]
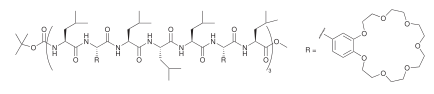
Otras arquitecturas utilizan hélices peptídicas como andamiaje para unir otras funcionalidades, como éteres corona de diferentes tamaños. La propiedad de estos canales corona peptídicos depende en gran medida de la identidad de los grupos terminales de protección.
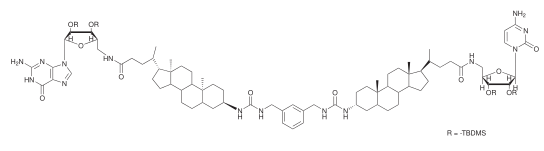
Se han construido canales biohíbridos semisintéticos construidos mediante modificaciones de canales iónicos naturales. Aprovechando la química orgánica sintética moderna , esto permite realizar modificaciones precisas de las estructuras existentes para dilucidar sus mecanismos de transporte o injertar nuevas funcionalidades.
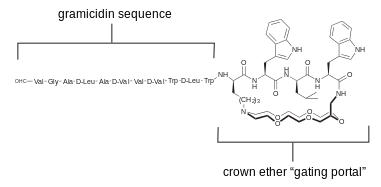
La gramicidina y la alameticina habían sido puntos de partida populares para modificaciones selectivas. [24] El diagrama anterior ilustra un ejemplo, donde se fijó un éter corona a través de la boca del portal de paso de iones. [25] Este canal muestra conductancia discreta pero selectividad iónica diferente a la de la gramicidina de tipo salvaje en experimentos de fijación de voltaje.
Si bien la modificación de grandes canales proteicos mediante mutagénesis generalmente se considera fuera del alcance de los canales sintéticos , la demarcación no es nítida, como lo demuestra la unión supramolecular o covalente de las ciclodextrinas a la alfa-hemolisina. [26]
Un canal iónico se puede caracterizar por sus características de apertura , selectividad iónica y control del flujo (activación). Muchos canales iónicos sintéticos muestran propiedades únicas en uno o más de estos aspectos.

Una molécula "formadora de canales iónicos" puede mostrar a menudo múltiples tipos de actividades de conductancia en membranas bicapa planas. Cada uno de estos modos de acción puede caracterizarse por su
Estos eventos no son necesariamente uniformes a lo largo de su duración y, como resultado, son posibles diversas formas de trazas conductoras.
La mayoría de los canales iónicos sintéticos siguen una secuencia Eisenman I (Cs + > Rb + > K + > Na + >> Li + ) [27] en su selectividad por cationes de metales alcalinos , [4] [18] lo que sugiere que el origen de la selectividad está gobernado por la diferencia de energía requerida para eliminar agua de un catión completamente hidratado. Algunos canales sintéticos muestran otros patrones de selectividad iónica, [25] y solo se ha informado de un único caso en el que un canal sintético sigue la secuencia de selectividad opuesta (Eisenman XI; Cs + < Rb + < K + < Na + << Li + ). [28]

La mayoría de los canales sintéticos tienen conductancia óhmica , es decir, la corriente que pasa (tanto individualmente como en conjunto) es proporcional al potencial a través de la membrana. Sin embargo, algunos canales poco frecuentes muestran características de corriente-voltaje que no son lineales. En concreto, se conocen dos tipos diferentes de conductancia no óhmica:
El primero requiere asimetría con respecto al plano medio de la bicapa lipídica y se logra a menudo introduciendo un dipolo molecular general. [29] [30] [31] El último, demostrado en canales naturales como la alameticina , rara vez se encuentra en canales iónicos sintéticos. Pueden estar relacionados con los canales iónicos lipídicos, pero hasta la fecha su mecanismo sigue siendo esquivo.
Ciertos canales iónicos sintéticos tienen conductancias que pueden modularse mediante la adición de sustancias químicas externas. Se conocen tanto la modulación ascendente (los canales se activan mediante ligando) como la modulación descendente (los canales se desactivan mediante ligando): diferentes mecanismos, incluida la formación de agregados supramoleculares, [32] [33] así como el bloqueo inter e intramolecular [34] .
Se conocen elementos reguladores que responden a otras señales; algunos ejemplos incluyen conductancias fotomoduladas [35] [36] [37] así como "interruptores térmicos" construidos por isomerización del grupo carbamato . [38] Hasta la fecha, no se han informado canales iónicos sintéticos mecanosensibles.